|
|
|
|
|
再灌注治疗改善缺血性卒中的长期功能预后 Engineering |
|
|
论文标题:Improving Long-Term Functional Outcomes of Ischemic Stroke in the Reperfusion Era
期刊:Engineering
DOI:https://doi.org/10.1016/j.eng.2024.04.004
微信链接:点击此处阅读微信文章

作者:吴川杰, 褚学红, 朱占伟, 吴迪, 吉训明
1 引言
伤残调整生命年(DALY)损失指标显示,卒中仍然是全球第二大疾病死亡原因,且位于致死和致残原因的第三位[1]。亚洲发展中国家和美国的“卒中带”地区承担着最重的卒中致残负担[2]。尽管循证急性治疗(如静脉溶栓和血管内治疗)取得了显著进展,但卒中负担仍然居高不下[3]。
2023年,在近端颅内动脉闭塞所致缺血性卒中的治疗方面取得重大突破,多项临床试验为血管内治疗提供了有力证据支持,特别是对于具有大面积缺血核心的患者[4]。自首个支持血管内治疗的临床试验以来,血管内治疗已进入新纪元。然而,接受血管内治疗的患者数量增加并不等同于预后改善。卒中患者会出现长期功能障碍,而大面积缺血核心患者的这一比例更高。因此,优化急性卒中治疗策略和改善康复治疗仍有大量工作要做。
中枢神经系统(CNS)传统上被视为与机体其他部分相对隔离的特殊区域。血脑屏障(BBB)最初被认为是许多蛋白质和因子的绝对屏障。近期,研究发现了可以传递神经、细胞和分子信号的众多新的功能性和解剖学通路。中枢神经系统与机体之间的这种跨系统对话为神经保护或细胞保护带来了新的希望[5]。
此外,某些因子即使无法穿过血脑屏障,但仍可通过与血脑屏障上的受体相互作用来传递信号[6]。尤为关键的是,新型蛋白质组学和单细胞RNA测序技术发现了许多介导中枢神经系统与机体之间对话的因子[7]。这些进展为我们从脑部交互的系统生物学视角重新思考潜在治疗靶点和促进卒中的康复提供了机遇。
2 卒中患者的血管再通治疗
1995年,美国国家神经疾病和卒中研究所的试验证实,在卒中发生后3 h内给予重组组织型纤溶酶原激活剂(rt-PA)可显著改善急性缺血性卒中患者的临床预后[8]。次年,美国食品药物监督管理局批准了rt-PA用于治疗急性缺血性卒中,由此开启了静脉溶栓治疗的时代。欧洲急性卒中合作研究Ⅲ期试验随后将静脉溶栓的时间窗扩展至4.5 h [9]。然而,静脉溶栓的时间窗仍然较窄,且多项禁忌症限制了适合这种治疗的人群范围。此外,约40%的急性缺血性卒中是由颅内大血管急性闭塞引起,这使6个月死亡率增加3.5倍,预后良好患者的比例减少33% [10]。新技术推动了静脉溶栓治疗新模式的发展。例如,这些治疗可在移动卒中单元启动,并对4.5 h时间窗外的患者进行治疗。新型人体组织纤溶酶原激活剂(如替奈普酶)也已进入临床应用[2,5]。
对于因颅内大血管急性闭塞导致的急性缺血性卒中患者,静脉溶栓的再通率仅约三分之一[3]。2015年,荷兰多中心随机临床试验及其他四项随机对照试验证实,6 h内的血管内治疗可显著改善前循环近端颅内动脉闭塞所致急性缺血性卒中的临床预后[11]。血管内治疗后,46.0%的患者在三个月时功能预后良好(改良Rankin量表评分0~2),而单纯药物治疗组仅为26.5%(校正比值比为2.71 [2.07~3.55];p < 0.0001)[3]。血管内治疗后,成功再通率可达70%。后续试验,如磁共振弥散加权成像(DWI)或计算机断层扫描灌注(CTP)评估试验和基于影像学评估的缺血性卒中血管内治疗试验,将治疗时间窗扩展至24 h [12-13]。因此,血管内治疗现已被公认为治疗大血管闭塞性急性缺血性卒中最有效的治疗方法,并被多个临床指南推荐[14]。然而,后循环血管内治疗的疗效直到2022年才在临床试验中得到证实。中国基底动脉闭塞血管内治疗试验以及急性基底动脉闭塞血管内治疗试验验证了血管内治疗对基底动脉急性闭塞所致急性缺血性卒中的安全性和有效性[15-16]。急性缺血性卒中的血管再通治疗已进入新纪元,血管内治疗后超过80%的患者实现了成功再通。此外,一系列随机对照试验优化了急性缺血性卒中血管内治疗的流程和方案。这种优化包括梗死体积筛查、围手术期血压控制和院前转运方案,进一步提高了血管内治疗的临床疗效[17-18]。
尽管近年来卒中治疗取得重大进展,但是在再灌注治疗时代,超过50%的卒中患者预后仍不理想,75%的患者遗留终身残疾[19]。脑血管闭塞后,缺血核心区的神经元在数分钟内即发生不可逆的细胞死亡。在侧支循环代偿不良的患者中,大面积梗死核心和小面积缺血半暗带迅速形成,限制了再通治疗的疗效。根据现行指南,血管内治疗对小梗死核心的患者有效[20]。日本大面积缺血核心急性栓塞血管内救治试验结果表明,虽然血管内治疗优于最佳药物治疗,但患者临床预后显著不佳。具体而言,血管内治疗后仅14%的患者90 d预后良好(mRS 0~2)[18]。此外,即使大血管完全再通,仍有四分之一的患者出现微血管和脑组织灌注不足,提示存在无复流现象[21]。这可能导致再灌注损伤并加重脑组织损害。血管再通治疗为急性缺血性卒中的治疗带来了新的机遇和挑战。在再灌注治疗时代,脑保护已成为亟待解决的科学问题。
3 从系统生物学角度保护大脑
卒中后的黄金时间窗至关重要。再通治疗为挽救大脑铺平了道路。神经保护和细胞保护对于挽救受损细胞至关重要。在过去几十年中,缺血性脑组织的神经保护已从单纯保护神经元转向保护神经血管单元(NVU,包括神经元、胶质细胞和血管成分),即所谓的细胞保护[22]。依达拉奉和奈立胺等神经保护剂已在临床试验中使用。尽管显示出一定的效果,但由于它们穿透血脑屏障和到达缺血半暗带的能力有限,导致药物浓度不足,其治疗缺血性卒中的效果仍然受限。解决这一挑战已成为当前研究发现更有效药物递送方法的重点[23]。因此,考虑到缺血性卒中复杂的病理机制,各种功能性纳米颗粒已被开发为有前景的药物递送平台,有望改善缺血性卒中的治疗效果[24]。此外,细胞死亡在缺血性卒中的发生和发展中起重要作用,包括细胞焦亡、凋亡、坏死性凋亡、铁死亡和泛死亡[25]。新证据表明,在缺血性卒中慢性期抑制铁死亡或靶向衰老细胞可以延缓疾病进展并进一步改善预后[26]。因此,靶向细胞死亡是治疗缺血性卒中的有效手段。干细胞治疗已成为卒中治疗中的一个具有潜力的方法,能够再生丢失的脑细胞。干细胞治疗的一些功能机制包括神经营养因子的分泌、特性恢复、细胞替代和生物桥的形成。干细胞在急性期[27?28]和慢性期[29]的神经保护和再生能力表明,干细胞移植仍然是解决卒中后缺陷的有效方法。虽然干细胞治疗的成功在很大程度上取决于所使用的干细胞类型,但移植方法同样重要,因为不同的递送途径会触发不同的治疗机制并表现出独特的功能益处。更具吸引力的策略是使用针对缺血级联多个组分(如神经肽、低温和硫酸镁[30-31])的细胞保护方法。此外,在高度再灌注时代,血管保护的概念也受到重视。许多研究发现,在小鼠模型中卒中后30 min即出现微细的血脑屏障渗漏,表明早期血脑屏障保护与更好的卒中预后密切相关[32-33]。此外,增强脑血管循环储备或内源性侧支循环对细胞保护也至关重要[34]。
神经血管单元内各种细胞类型之间的交流与卒中预后相关,例如星形胶质细胞和神经元之间的三磷酸腺苷(ATP)转移以及在神经血管单元内介导损伤向恢复转变的“求助”信号[35]。急性缺血性卒中后,小胶质细胞可以迅速激活并极化为促炎性M1型和抗炎性M2型,在组织损伤和神经保护中发挥双重作用[36]。其中,M2型小胶质细胞在髓鞘形成和重建、神经元再生和血管新生中发挥关键作用,是促进缺血性卒中后神经元再生的主要靶点[37]。因此,对于未来缺血性卒中的治疗,我们可以促进小胶质细胞向M2型极化,减少M2型向M1型的转化,延长M2型小胶质细胞的表达时间,促进神经再生和功能恢复。缺血相关的氧化稳态紊乱导致的活性氧自由基积累促进了与氧化应激相关的分子和细胞损伤。氧化应激是缺血性卒中进展中的重要病理生理机制,与缺血再灌注损伤的发生密切相关。因此,靶向氧化应激,包括抗氧化剂和寻找氧化应激生物标志物,可能是缺血性卒中的潜在治疗方法[38]。因此,在再灌注时代,针对卒中后缺血级联的多个方面并对神经血管单元所有成分有益的药物或非药物方式,具有吸引力和转化潜力。
神经修复策略通过促进血管新生、轴突重塑、神经发生和突触形成,为改善卒中后功能恢复带来了有前景的希望[39]。此前,神经修复治疗在脑损伤后的效果通常被认为较为有限。近年来,脑–肠、脑–骨、脑–肝、脑–心和脑–骨骼肌轴被发现在脑与外周器官之间的交流中发挥着关键作用(图1)。值得注意的是,临床前研究[40-41]和临床研究[42]表明,脾脏体积在缺血性卒中后显著减小,表明脾脏在卒中后的外周炎症中发挥重要作用。研究证实,切除脾脏可进一步减少梗死体积,而脾细胞回输可逆转这种治疗效果[43]。此外,放射线引起的脾功能减退也可以减少梗死体积[44]。上述证据证实,减少脾脏炎症在缺血性卒中治疗中发挥重要作用。在实验室研究和临床实践中发现,利用系统性和生活方式干预(包括限制热量、运动和预处理)后,血源性信号可以为大脑带来益处。例如,在小鼠自主跑轮运动四天后,血液中硒蛋白P上调,可以通过血脑屏障运输硒并促进海马神经发生[45]。同时,在人类和动物运动后都观察到抗炎运动因子。更重要的是,这些因子可以转移,靶向作用于脑血管,并使大脑受益[46]。越来越多的研究认识到,这些血源性信号,包括细胞因子、核酸、脂质、微生物组和代谢物,作为来自外周系统的信号促进卒中后神经修复。
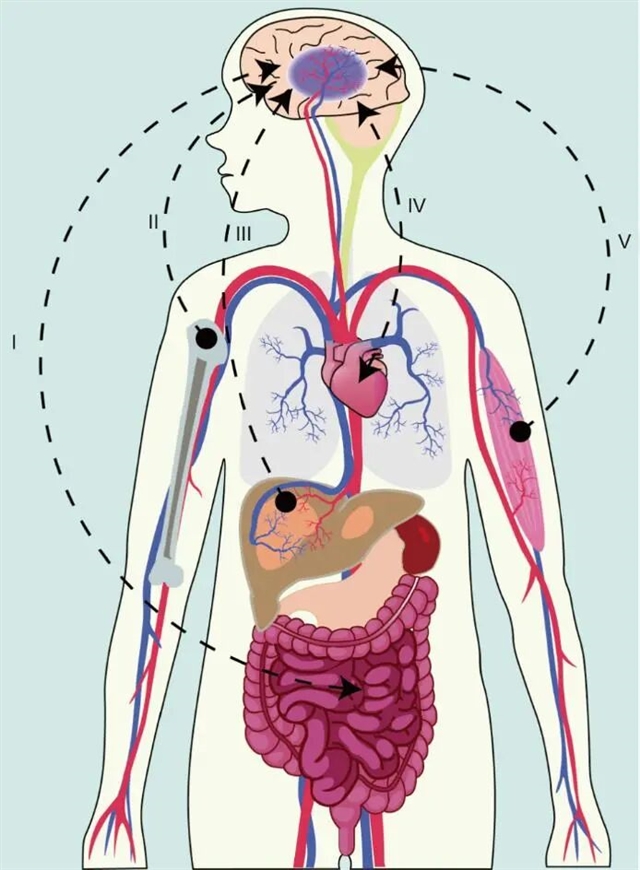
图1 大脑与外周器官的相互作用:Ⅰ:脑-肠轴;Ⅱ:脑-骨轴;Ⅲ:脑-肝轴;Ⅳ:脑-心轴;Ⅴ:脑-骨骼肌轴。
越来越多的证据表明,先天和适应性免疫系统在介导缺血/再灌注后疾病进展中发挥重要作用。卒中后的炎症反应通过高度协调的一系列事件发生,涉及中枢和外周免疫系统的各种细胞类型。一项发表为会议摘要的临床前研究显示,基于脑梗死血管再通的抗炎治疗可能发挥有益作用[47]。因此,抗炎治疗有望进一步改善此类患者的不良预后。然而,需要进一步的临床试验来验证这些初步发现。多项临床试验已尝试调节炎症反应以改善卒中后的长期功能[48]。然而,目前尚无明确的获益。此外,卒中后肠道对大脑的影响已引起广泛关注。多项证据表明,肠道微生物群不仅可以直接影响卒中后神经修复,而且通过各种方式影响大脑功能[49-50]。目前,调节肠道细菌已成为改善患者和动物模型神经修复的有前景的干预措施,包括粪菌移植治疗和益生菌、益生元或合生元治疗[5]。Bonkhoff和Grefkes [51]讨论了现有的人工智能方法和急性期、亚急性期和慢性期卒中预后研究中的单个受试者预测情况。他们概述了数据的日益丰富如何带来新的科学见解,并最终有助于改善卒中后预后[51]。总之,要将这些系统性干预措施建立为临床常规并进一步改善卒中患者的不良预后,需要更多研究来解决当前的挑战,如最佳启动时间、具体靶点和最适合患者的选择。
4 结论和展望
近几十年来,溶栓和血管内取栓技术的发展使再通治疗发生了革命性变化。由于临床证据的积累以及新型血管内材料和影像学方法的进步,适合再通治疗的候选患者数量增加。在不久的将来,人工智能方法的应用也将帮助我们为不同阶段的卒中患者做出精确的治疗选择。然而,改善高效再灌注后的长期功能预后仍然迫在眉睫。
近年来,人们普遍接受大脑是缺血性卒中后与系统生物学双向互动的重要器官。得益于蛋白质组学和转录组学分析技术的进步,中枢和外周神经系统之间的交流已被观察到。随着近期研究强调改善长期功能预后的方法,未来缺血性卒中的治疗可能需要采取多管齐下的方式。对于急性期患者,需要强调通过血管和细胞机制来保护神经血管单元。对于慢性期患者,通过增加血管新生、神经发生和突触形成来促进与大脑的有益交流,将改善卒中后的长期功能预后。
参考文献
[1]Feigin VL, Brainin M, Norrving B, Martins S, Sacco RL, Hacke W, et al. World Stroke Organization (WSO): global stroke fact sheet 2022. Int J Stroke 2022; 17 (1):18-29.
[2]Duncan PW, Bushnell C, Sissine M, Coleman S, Lutz BJ, Johnson AM, et al. Comprehensive stroke care and outcomes: time for a paradigm shift. Stroke 2021; 52(1):385-93.
[3]Goyal M, Menon BK, van Zwam WH, Dippel DWJ, Mitchell PJ, Demchuk AM, et al. Endovascular thrombectomy after large-vessel ischaemic stroke: a metaanalysis of individual patient data from five randomised trials. Lancet 2016; 387(10029):1723-31.
[4]Huo X, Ma G, Tong X, Zhang X, Pan Y, Nguyen TN, et al. Trial of endovascular therapy for acute ischemic stroke with large infarct. N Engl J Med 2023; 388 (14):1272-83.
[5]Tiedt S, Buchan AM, Dichgans M, Lizasoain I, Moro MA, Lo EH. The neurovascular unit and systemic biology in stroke—implications for translation and treatment. Nat Rev Neurol 2022; 18(10):597-612.
[6]Gao HM, Chen H, Cui GY, Hu JX. Damage mechanism and therapy progress of the blood-brain barrier after ischemic stroke. Cell Biosci 2023; 13(1):196.
[7]Bieri G, Schroer AB, Villeda SA. Blood-to-brain communication in aging and rejuvenation. Nat Neurosci 2023; 26:379-93.
[8]The National Institute of Neurological Disorders, Stroke rt-PA Stroke Study Group. Tissue plasminogen activator for acute ischemic stroke. N Engl J Med 1995; 333(24):1581-8.
[9]Hacke W, Kaste M, Bluhmki E, Brozman M, Dávalos A, Guidetti D, et al. Thrombolysis with alteplase 3 to 4.5 hours after acute ischemic stroke. N Engl J Med 2008; 359(13):1317-29.
[10]Karamchandani RR, Rhoten JB, Strong D, Chang B, Asimos AW. Mortality after large artery occlusion acute ischemic stroke. Sci Rep 2021; 11(1):10033.
[11]Berkhemer OA, Fransen PSS, Beumer D, van den Berg LA, Lingsma HF, Yoo AJ, et al. A randomized trial of intraarterial treatment for acute ischemic stroke. N Engl J Med 2015; 372(1):11-20.
[12]Albers GW, Marks MP, Kemp S, Christensen S, Tsai JP, Ortega-Gutierrez S, et al. Thrombectomy for stroke at 6 to 16 hours with selection by perfusion imaging. N Engl J Med 2018; 378(8):708-18.
[13]Nogueira RG, Jadhav AP, Haussen DC, Bonafe A, Budzik RF, Bhuva P, et al. Thrombectomy 6 to 24 hours after stroke with a mismatch between deficit and infarct. N Engl J Med 2018; 378(1):11-21.
[14]Powers WJ, Rabinstein AA, Ackerson T, Adeoye OM, Bambakidis NC, Becker K, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke 2019; 50(12):e344-418.
[15]Jovin TG, Li C, Wu L, Wu C, Chen J, Jiang C, et al. Trial of thrombectomy 6 to 24 hours after stroke due to basilar-artery occlusion. N Engl J Med 2022; 387 (15):1373-84.
[16]Tao C, Nogueira RG, Zhu Y, Sun J, Han H, Yuan G, et al. Trial of endovascular treatment of acute basilar-artery occlusion. N Engl J Med 2022; 387 (15):1361-72.
[17]Nam HS, Kim YD, Heo J, Lee H, Jung JW, Choi JK, et al. Intensive vs conventional blood pressure lowering after endovascular thrombectomy in acute ischemic stroke: the OPTIMAL-BP randomized clinical trial. JAMA 2023; 330(9):832-42.
[18]Yoshimura S, Sakai N, Yamagami H, Uchida K, Beppu M, Toyoda K, et al. Endovascular therapy for acute stroke with a large ischemic region. N Engl J Med 2022; 386(14):1303-13.
[19]Wu S, Wu B, Liu M, Chen Z, Wang W, Anderson CS, et al. Stroke in China: advances and challenges in epidemiology, prevention, and management. Lancet Neurol 2019; 18(4):394-405.
[20]Kleindorfer DO, Towfighi A, Chaturvedi S, Cockroft KM, Gutierrez J, Lombardi- Hill D, et al. 2021 guideline for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline from the American Heart Association/American Stroke Association. Stroke 2021; 52(7):e364-467.
[21]Zhang Y, Jiang M, Gao Y, Zhao W, Wu C, Li C, et al. ‘‘No-reflow” phenomenon in acute ischemic stroke. J Cereb Blood Flow Metab 2024; 44(1):19-37.
[22]Wu D, Li M, Fisher M, Ji X. Brain cytoprotection of ischemic stroke in the era of effective reperfusion. Sci Bull 2022; 67(23):2372-5.
[23]Lapchak PA. A critical assessment of edaravone acute ischemic stroke efficacy trials: is edaravone an effective neuroprotective therapy? Expert Opin Pharmacother 2010; 11(10):1753-63.
[24]He W, Zhang Z, Sha X. Nanoparticles-mediated emerging approaches for effective treatment of ischemic stroke. Biomaterials 2021; 277:121111.
[25]Gong Z, Guo J, Liu B, Guo Y, Cheng C, Jiang Y, et al. Mechanisms of immune response and cell death in ischemic stroke and their regulation by natural compounds. Front Immunol 2023; 14:1287857.
[26]El Hadri K, Smith R, Duplus E, El Amri C. Inflammation, oxidative stress, senescence in atherosclerosis: thioredoxine-1 as an emerging therapeutic target. Int J Mol Sci 2021; 23(1):77.
[27]Ishikawa H, Tajiri N, Shinozuka K, Vasconcellos J, Kaneko Y, Lee HJ, et al. Vasculogenesis in experimental stroke after human cerebral endothelial cell transplantation. Stroke 2013; 44(12):3473-81.
[28]Tuazon JP, Castelli V, Borlongan CV. Drug-like delivery methods of stem cells as biologics for stroke. Expert Opin Drug Deliv 2019; 16(8):823-33.
[29]Kondziolka D, Steinberg GK, Wechsler L, Meltzer CC, Elder E, Gebel J, et al. Neurotransplantation for patients with subcortical motor stroke: a phase 2 randomized trial. J Neurosurg 2005; 103(1):38-45.
[30]Eren F, Yilmaz SE. Neuroprotective approach in acute ischemic stroke: a systematic review of clinical and experimental studies. Brain Circ 2022; 8 (4):172-9.
[31]Li F, Gao J, Kohls W, Geng X, Ding Y. Perspectives on benefit of early and prereperfusion hypothermia by pharmacological approach in stroke. Brain Circ 2022; 8(2):69-75.
[32]Huang L, Chen Y, Liu R, Li B, Fei X, Li X, et al. P-glycoprotein aggravates blood brain barrier dysfunction in experimental ischemic stroke by inhibiting endothelial autophagy. Aging Dis 2022; 13(5):1546-61.
[33]Qi L, Wang F, Sun X, Li H, Zhang K, Li J. Recent advances in tissue repair of the blood-brain barrier after stroke. J Tissue Eng 2024; 15:20417314241226551.
[34]Xiong Y, Wakhloo AK, Fisher M. Advances in acute ischemic stroke therapy. Circ Res 2022; 130(8):1230-51.
[35]Sato Y, Falcone-Juengert J, Tominaga T, Su H, Liu J. Remodeling of the neurovascular unit following cerebral ischemia and hemorrhage. Cells 2022; 11(18):2823.
[36]Mo Y, Xu W, Fu K, Chen H, Wen J, Huang Q, et al. The dual function of microglial polarization and its treatment targets in ischemic stroke. Front Neurol 2022; 13:921705.
[37]Liu B, Gu Y, Pei S, Peng Y, Chen J, Pham LV, et al. Interleukin-1 receptor associated kinase (IRAK)-M-mediated type 2 microglia polarization ameliorates the severity of experimental autoimmune encephalomyelitis (EAE). J Autoimmun 2019; 102:77-88.
[38]Kamal FZ, Lefter R, Jaber H, Balmus IM, Ciobica A, Iordache AC. The role of potential oxidative biomarkers in the pognosis of acute ischemic stroke and the exploration of antioxidants as possible preventive and treatment options. Int J Mol Sci 2023; 24(7):6389.
[39]Xiong Y, Mahmood A, Chopp M. Neurorestorative treatments for traumatic brain injury. Discov Med 2010; 10:434-42.
[40]Marcet P, Santos N, Borlongan CV. When friend turns foe: central and peripheral neuroinflammation in central nervous system injury. Neuroimmunol Neuroinflamm 2017; 4(5):82-92.
[41]Das M, Mohapatra S, Mohapatra SS. New perspectives on central and peripheral immune responses to acute traumatic brain injury. J Neuroinflammation 2012; 9(1):236.
[42]Ajmo CT Jr, Collier LA, Leonardo CC, Hall AA, Green SM, Womble TA, et al. Blockade of adrenoreceptors inhibits the splenic response to stroke. Exp Neurol 2009; 218(1):47-55.
[43]Ajmo CT Jr, Vernon DO, Collier L, Hall AA, Garbuzova-Davis S, Willing A, et al. The spleen contributes to stroke-induced neurodegeneration. J Neurosci Res 2008; 86(10):2227-34.
[44]Jin R, Zhu X, Liu L, Nanda A, Granger DN, Li G. Simvastatin attenuates strokeinduced splenic atrophy and lung susceptibility to spontaneous bacterial infection in mice. Stroke 2013; 44(4):1135-43.
[45]Leiter O, Zhuo Z, Rust R, Wasielewska JM, Grönnert L, Kowal S, et al. Selenium mediates exercise-induced adult neurogenesis and reverses learning deficits induced by hippocampal injury and aging. Cell Metab 2022; 34(3):408-23.
[46]De Miguel Z, Khoury N, Betley MJ, Lehallier B, Willoughby D, Olsson N, et al. Exercise plasma boosts memory and dampens brain inflammation via clusterin. Nature 2021; 600(7889):494-9.
[47]Hudobenko J, Chauhan A, McCullough L; Jacob Hudobenko RVaLM. Abstract 128: amelioration of ischemic stroke damage through inhibition of interleukin-6 signaling with tocilizumab requires sex specific dosing. Stroke 2019; 50:Suppl_1.
[48]Boczar KE, Shin S, Bezzina KA, Geejo A, Pearson AL, Shahab S, et al. Examining anti-inflammatory therapies in the prevention of cardiovascular events: protocol for a systematic review and network meta-analysis of randomised controlled trials. BMJ Open 2022; 12(6):e062702.
[49]Khan R, Di Gesù CM, Lee J, McCullough LD. The contribution of age-related changes in the gut-brain axis to neurological disorders. Gut Microbes 2024; 16 (1):2302801.
[50]Kingsbury C, Shear A, Heyck M, Sadanandan N, Zhang H, Gonzales-Portillo B, et al. Inflammation-relevant microbiome signature of the stroke brain, gut, spleen, and thymus and the impact of exercise. J Cereb Blood Flow Metab 2021; 41(12):3200-12.
[51]Bonkhoff AK, Grefkes C. Precision medicine in stroke: towards personalized outcome predictions using artificial intelligence. Brain 2022; 145(2):457-75.
引用本文:
Chuanjie Wu, Xuehong Chu, Zhanwei Zhu, Di Wu, Xunming Ji. Improving Long-Term Functional Outcomes of Ischemic Stroke in the Reperfusion Era. Engineering, 2024, 40(9): 15-19 DOI:10.1016/j.eng.2024.04.004
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。