|
|
|
|
|
Life Med | 李晶/舒文杰等揭示小鼠卵巢全生命周期中基质细胞间相互作用与调控机制 |
|
|
论文标题:Single-cell RNA sequencing reveals the intercellular crosstalk and the regulatory landscape of stromal cells during the whole life of the mouse ovary
期刊:Life Medicine
作者:Wan Jiang, , Wenya Sun, , Yue Peng, , Hao Xu, , Haonan Fan , Xin Jin , Yue Xiao, Yuxiang Wang , Pin Yang , Wenjie Shu , Jing Li
发表时间:15 Dec 2024
DOI:10.1093/lifemedi/lnae041
微信链接:点击此处阅读微信文章
如何延缓卵巢衰老、提高高龄女性生育力是生殖领域当前亟待解决的问题之一。在哺乳动物中,卵巢的基本单位是卵泡,而卵巢的非卵泡部分则被统称为卵巢间充质(mesenchyme)或卵巢基质(stroma)。卵巢基质由多种细胞构成,近年来,随着对卵巢基质的理解逐步加深,研究者发现卵泡膜细胞与基质细胞之间存在着密切的关系,基质细胞的类型与分布可能会根据其在卵巢中的具体位置而有所差异。这些细胞不仅受到卵泡生长、排卵和黄体形成过程的影响,也与卵巢衰老有密切关联。目前,对于卵巢基质细胞如何在组织重塑过程中与其他细胞类型协调合作,以及其在调节卵巢功能中的作用机制的认识并不完全。尤其在涉及卵巢整个生命周期内体细胞类型的多样性及细胞、基因表达的动态变化方面,现有的研究并不能提供全局性的视图。因此,深入探究卵巢基质细胞如何通过细胞间相互作用影响卵泡发育,并探讨这一过程如何引发卵巢衰老,是当前研究的重点之一。
单细胞scRNA-seq方法能在单细胞分辨率下探索卵巢体细胞类型组成,转录本动态,基因调控网络和细胞间相互作用,是研究卵巢发育中动态变化和关键事件的重要工具。通过对不同发育时期的卵巢单细胞测序数据进行整合分析,可以全面解析卵巢全生命周期中生殖细胞和体细胞的分化发育轨迹、各阶段的功能特征以及关键基因的表达模式。该方法不仅有助于探究卵巢基质细胞在卵巢发育中的作用和调控机制,也为揭示卵巢衰老的分子机制并提出延缓卵巢衰老的策略提供了新的视角和解决方案。

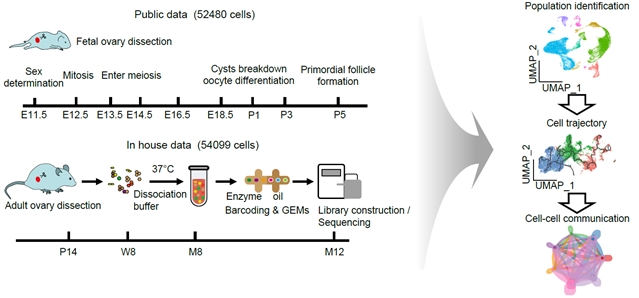
近日,南京医科大学生殖医学与子代健康全国重点实验室李晶教授团队和军事医学研究院生物信息中心舒文杰研究员团队合作在Life Medicine杂志在线发表了题为“Single-cell RNA sequencing reveals the intercellular crosstalk and the regulatory landscape of stromal cells during the whole life of the mouse ovary” 的研究论文,整合并发表了从E11.5(胚胎期11.5天)到M12(12个月)卵巢的单细胞RNA测序数据,探索了小鼠卵巢发育过程中的细胞类型、信号通路和调节机制,重建了从性腺分化到原始卵泡形成直到卵巢衰老的细胞图谱,并描绘了卵巢体细胞,特别是基质细胞在卵巢整个生命周期中的调节作用。
研究人员利用公共数据,收集了采用10xGenomics技术测序的来源于同一品系小鼠(C57BL/6)的单细胞RNA测序数据(从E11.5至P5)。此外,他们还对P14(出生后14天)、W8(8周)、M8(8月)和M12(12月)的小鼠卵巢进行了相同技术的测序,从而补全了小鼠从E11.5原始生殖细胞迁移至生殖嵴开始,直至12个月时卵泡闭锁和生殖储备耗尽的整个卵巢衰老过程。通过分析这一完整的卵巢发育周期,研究者对生殖细胞和体细胞进行了高精度的分类,并分别探究了这些细胞的分化发育轨迹、各阶段的功能以及关键基因。这项研究不仅为理解卵巢发育提供了重要的实验数据,还进一步加深了对卵巢体细胞,尤其是间充质细胞在卵巢发育和衰老中发挥功能的理解。
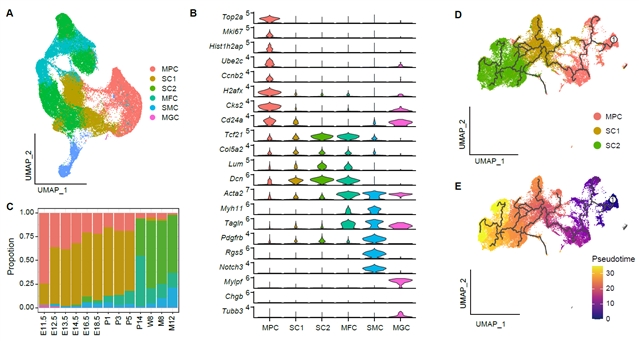
在对单细胞数据经过批次校正后,研究人员将高质量的单细胞数据整合到一个统一的数据集中,使用均匀流形近似和投影(UMAP)对所有细胞进行了聚类,并根据标记基因的表达获得了7种主要细胞类型和31个细胞簇。为了深入了解卵巢间充质细胞的发育过程,研究人员根据典型标志物的表达将其中间充质细胞类群分为6个不同的细胞亚群,包括肌源性细胞(MGC)、肌成纤维细胞(MFC)、平滑肌细胞(SMC)和三个基质细胞亚群。这些间充质细胞组成也显示出沿发育线的动态变化。在基质细胞的三个亚组中,一组细胞命名为间充质祖细胞(mesenchymal progenitor cells, MPCs),它们高度表达细胞表面干细胞标志物CD24和DNA复制相关基因,如Top2a,Ccnb2等。另外两种基质细胞,1型基质细胞(SC1)主要存在于胎儿和新生儿卵巢(E11.5-P5),2型基质细胞(SC2)主要存在于P14-M12卵巢。研究人员通过伪时间分析发现了胎儿和新生小鼠卵巢从MPC到SC1的发育路线,然后在P14继续分化为SC2,直到卵巢衰老。
然后,研究人员评估了不同细胞类型在每个发育时间点之间的细胞通讯,并重点比较了W8和M12卵巢间质亚群、免疫亚群和颗粒细胞建立的细胞间通讯网络。总体而言,M12卵巢细胞间通讯的强度下降,随着MPC的减少,SC2基质细胞与其他细胞的相互作用增加。与先前的报道一致,在衰老过程中,通过Masson染色可以发现卵巢间质中胶原纤维的沉积。受体-配体分析发现,CD44和Sdc4是主导受体,它们主要参与8W至12M卵巢之间的胶原信号网络,表明CD44或Sdc4介导的胶原蛋白信号可能在卵巢衰老过程中的细胞通讯中起重要作用。
总之,研究人员发现,CD24+ 的MPC是卵巢结构建立过程中,特别是在原始卵泡形成时,引导基质细胞从SC1向SC2分化的祖细胞。此外,MPC作为一种重要的调节细胞类型,通过胶原信号通路中的特定配体-受体对,影响与其他细胞类型的相互作用。随着卵巢年龄的增长,MPC的数量显著下降。然而,卵巢可以通过MPC的激活实现再年轻化,这种激活可以由卵巢损伤诱导,也可以通过间充质干细胞(MSC)移植来实现。这项全面的分析不仅增强了对卵巢发育背后的细胞动力学的理解,而且还为与年龄相关的卵巢衰退提供了潜在的治疗策略。
南京医科大学生殖医学与子代健康全国重点实验室李晶教授和军事医学研究院生物信息中心舒文杰研究员为该论文的共同通讯作者。军事医学研究院生物信息中心研究生蒋琬、徐浩;南京医科大学生殖医学与子代健康全国重点实验室研究生孙文亚、彭悦为该论文共同第一作者。该研究得到了科技部国家重点研发计划的经费支持。
英文全文链接:
https://doi.org/10.1093/lifemedi/lnae041
引用本文:
Wan Jiang, Wenya Sun, Yue Peng, Hao Xu, Haonan Fan, Xin Jin, Yue Xiao, Yuxiang Wang, Pin Yang, Wenjie Shu, Jing Li, Single-cell RNA sequencing reveals the intercellular crosstalk and the regulatory landscape of stromal cells during the whole life of the mouse ovary, Life Medicine, Volume 3, Issue 6, December 2024, lnae041, https://doi.org/10.1093/lifemedi/lnae041
作者简介

李晶
南京医科大学
李晶,南京医科大学生殖医学与子代健康全国重点实验室教授,主要从事哺乳动物卵巢卵泡发育机制以及卵巢相关疾病发病机制的研究,所做的研究发表于Nature Cell Biology、Advanced Science、Journal of Extracellular Vesicles、 Autophagy、Molecular Therapy等。曾承担国家自然科学基金、科技部重大研究计划、“973”等项目的研究课题。建立了原始卵泡体外激活技术(以下简称IVA技术),证明卵巢内静息卵泡可以通过人工手段调节其发育进程。2013年10月,IVA技术在临床上成功应用治疗女性卵巢早衰,2018年,团队自主研发的二代IVA技术成功应用于临床,已有多名婴儿出生。

舒文杰
军事医学研究院生物信息中心
舒文杰,军事医学研究院生物信息中心研究员,主要从事生物信息学和人工智能研究,以共同第一或通讯作者在Nature Genetics、Cell Research、Nature Machine. Intelligence、Molecular Cell等期刊发表SCI论文40余篇。

《前沿》系列英文学术期刊
由教育部主管、高等教育出版社主办的《前沿》(Frontiers)系列英文学术期刊,于2006年正式创刊,以网络版和印刷版向全球发行。系列期刊包括基础科学、生命科学、工程技术和人文社会科学四个主题,是我国覆盖学科最广泛的英文学术期刊群,其中12种被SCI收录,其他也被A&HCI、Ei、MEDLINE或相应学科国际权威检索系统收录,具有一定的国际学术影响力。系列期刊采用在线优先出版方式,保证文章以最快速度发表。
中国学术前沿期刊网
http://journal.hep.com.cn

特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。