2025年9月19日,中国科学院上海有机所施世良课题组在Nature Synthesis期刊上发表了一篇题为“Selective dynamic kinetic asymmetric aldehyde–alkyne reductive coupling”的研究论文。作者实现了一种手性氮杂环卡宾-镍催化的醛和炔烃的动态动力学不对称还原偶联反应,高效合成具有连续手性中心烯丙醇结构。论文通讯作者为施世良;第一作者是陈光、刘佳明。
复杂分子的精准合成是药物与材料科学发展的重要驱动力。实现这一目标的关键,在于对化学反应中多种选择性的高效控制。传统合成方法多聚焦于单一选择性控制,而能在同一转化中同时调控多种选择性的策略仍较为稀缺。动态动力学拆分(DKR)作为一种新兴的不对称合成策略,能够以消旋底物为原料,一步构建含有连续手性中心的产物。然而,DKR过程的高效运转需要几个关键条件:底物对映异构体之间能快速互变;一种构型反应速率显著高于另一种;且外消旋化速率需远大于反应速率。近年来,羰基化合物的DKR氢化反应已较为成熟,但DKR碳碳成键反应的发展仍相对受限,尤其在醛参与的反应中,目前报道多集中于有机催化羟醛缩合反应,其他类型反应亟待拓展。
含有连续手性中心的烯丙醇结构广泛存在于活性分子中,但其高效不对称合成仍有待发展。通过醛与炔的DKR还原偶联反应,可一步构建此类骨架,但反应面临多重难点:醛的外消旋化常需碱催化,而碱易引发羟醛缩合副反应;体系中存在多种过渡金属催化的副反应,影响化学选择性;更关键的是,反应需同时控制对映、非对映、区域和顺反选择性,对反应体系的设计提出了极高要求。
在这项研究中,施世良研究团队通过设计氮杂环卡宾-镍催化体系对反应中同时存在的多种选择性进行了精准控制。反应在温和的条件下即可实现高效转化,具有高收率(高达99%)、高立体选择性(高达>99% e.e., 20:1 d.r.)、高区域选择性(高达20:1 r.r.)、100%顺式加成(高达99:1 E/Z)以及广阔的底物范围(86个例子)。
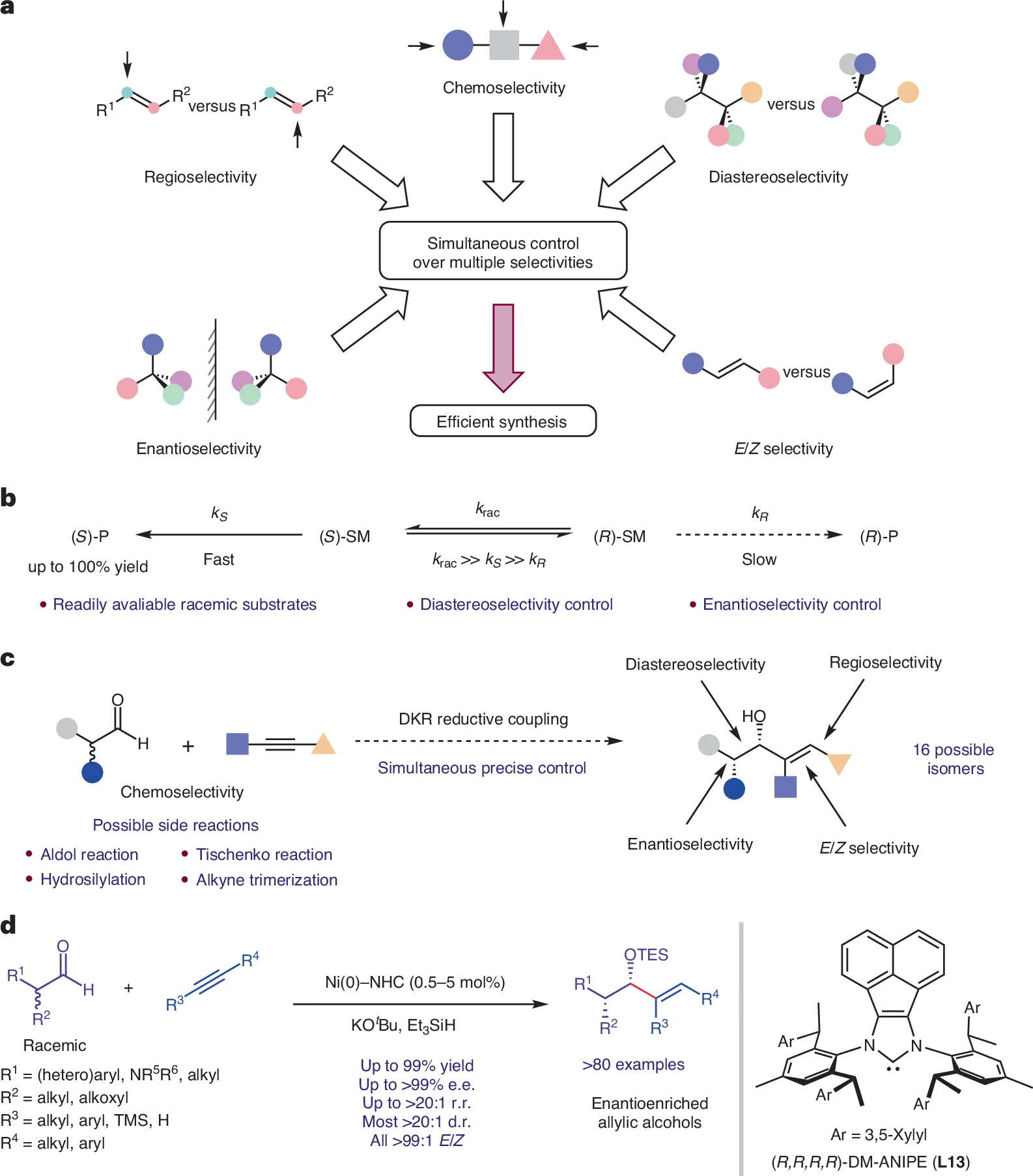
图1:背景介绍。
作者首先对消旋α-芳基醛的对映汇聚式还原偶联反应的底物范围进行探索。反应具有优秀的官能团和杂环兼容性,一系列具有给电子、吸电子取代基的α-芳基醛以及多种不同类型的对称、非对称底物均能够实现优秀的结果。其中包括在醛-炔不对称还原偶联中难以兼容的二芳基炔烃和末端炔烃。
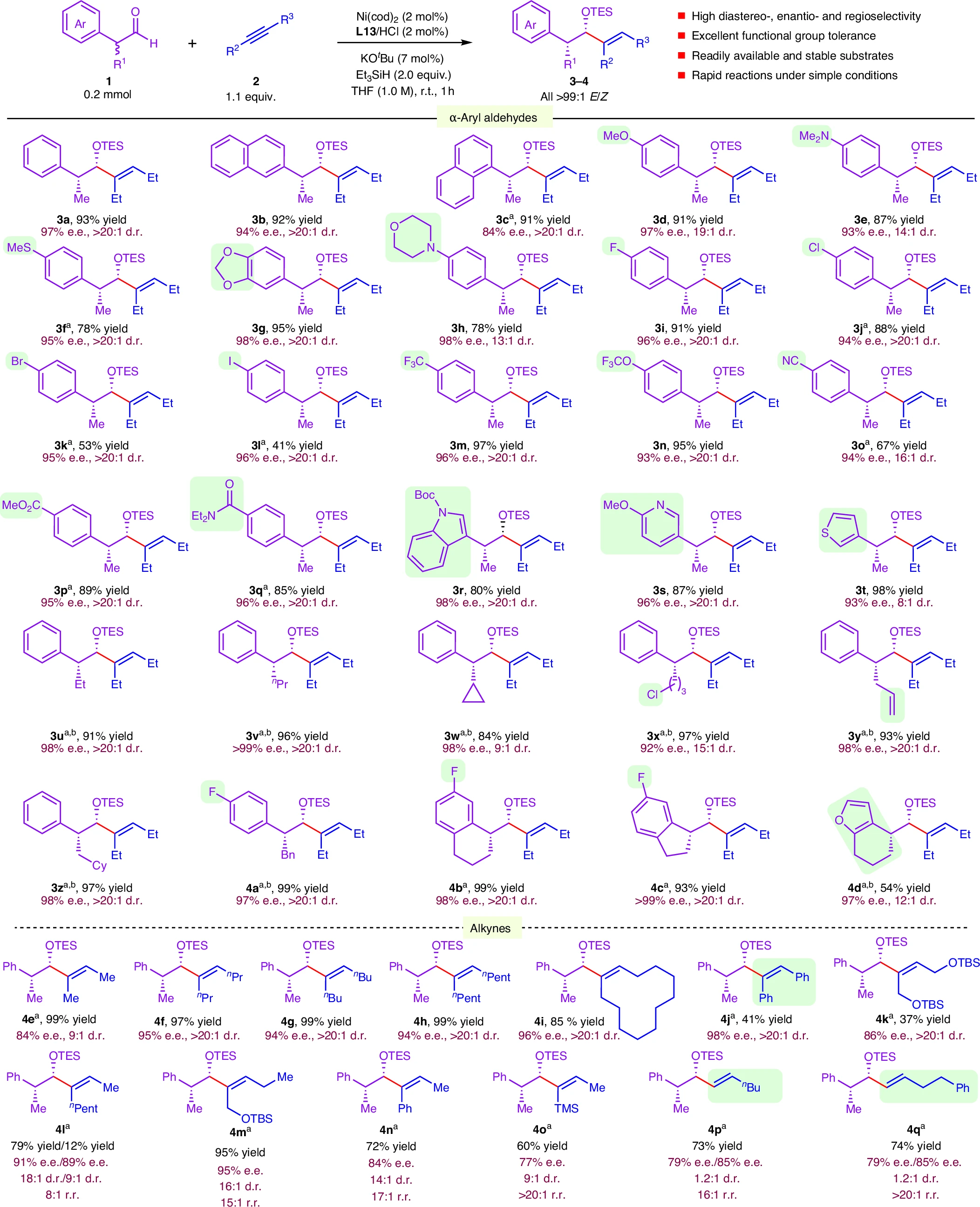
图2:α-芳基醛和炔烃的DKR还原偶联反应。
利用α-胺基醛和炔烃的对映汇聚式还原偶联反应,能够合成具有烯丙醇结构的手性1,2-氨基醇产物。一系列具有链状及环状结构的α-胺基醛和多种不同类型的对称、非对称底物均能够取得优秀的反应结果。反应还能扩展至α-烷氧基醛底物并合成具有手性1,2-二醇结构的产物。
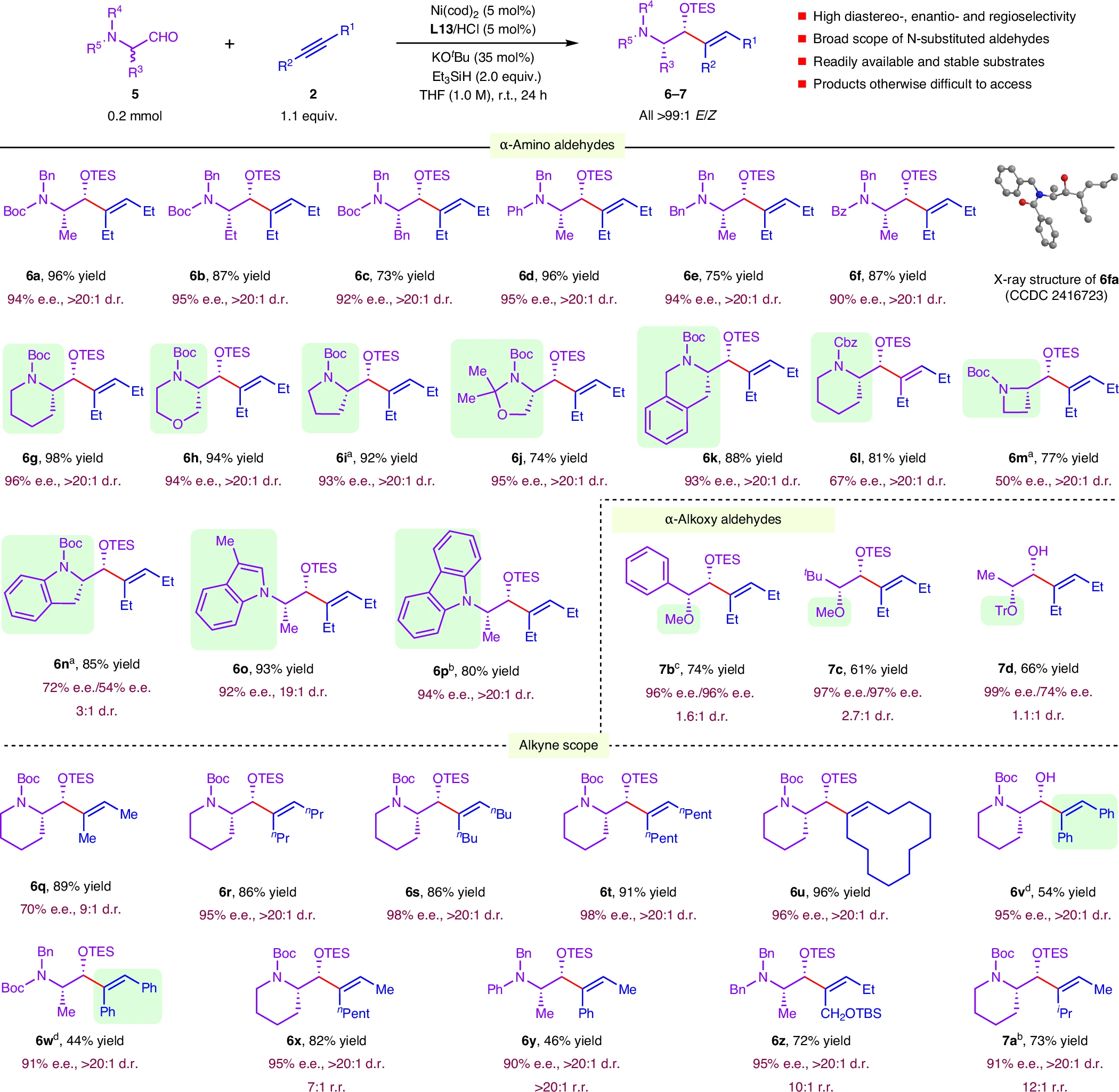
图3:α-胺基醛和炔烃的DKR还原偶联反应。
作者还成功将该策略拓展至挑战性的α,α-二烷基醛底物。这类底物因构象灵活且α-H酸性更低,其快速消旋化与立体控制难度极大。实验表明,多种α,α-二烷基醛与两种非对称炔烃均具有优秀的反应结果。
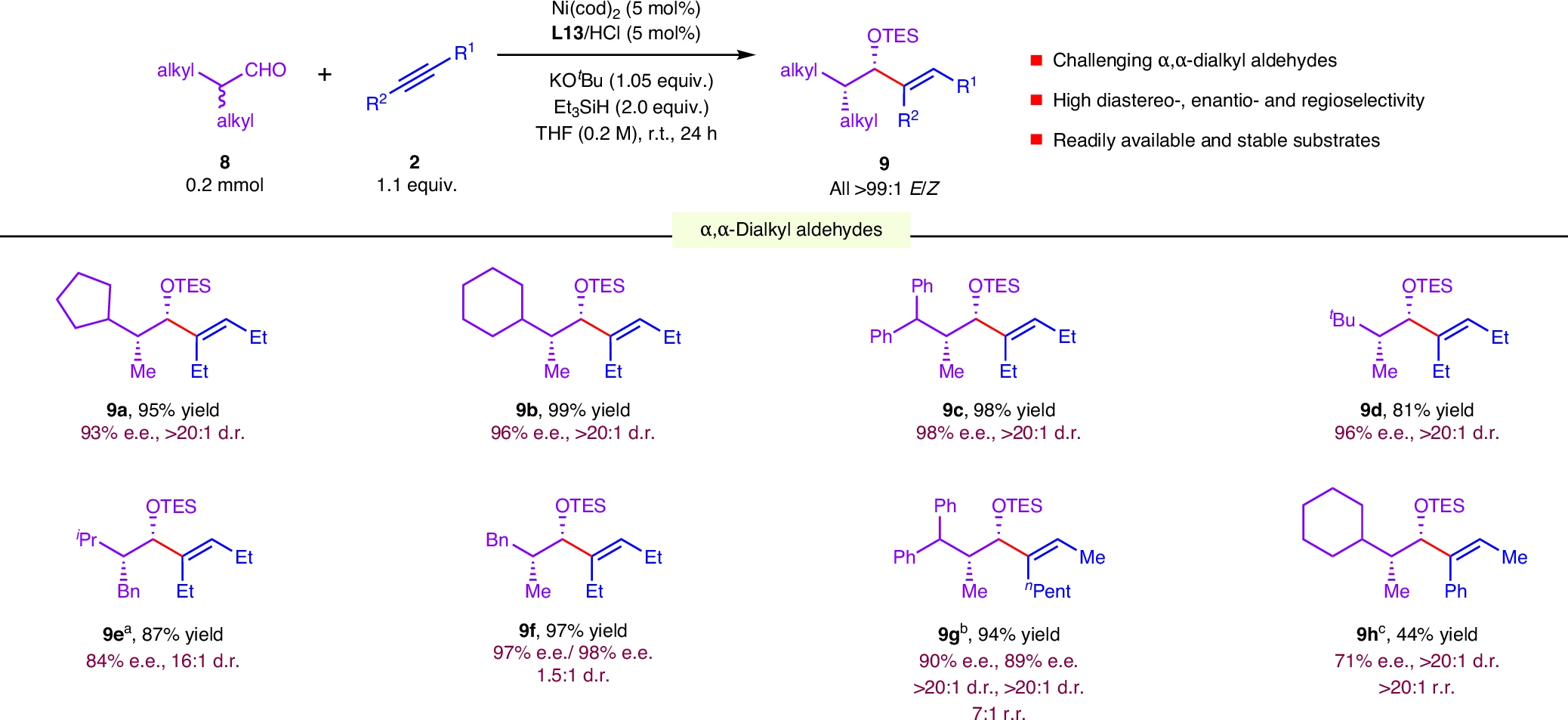
图4:α,α-二烷基醛和炔烃的DKR还原偶联反应。
该反应具有良好的应用潜力。在克级规模实验中,仅需千分之五的催化剂负载量即可实现高效转化。所得烯丙醇产物可进一步转化为环氧、酮等多种产物,并能通过分子内环化或烯烃复分解反应构建更复杂结构。此外,该策略还成功应用于布洛芬家族药物的衍生化,以及生物活性分子鞘氨醇的形式合成之中。
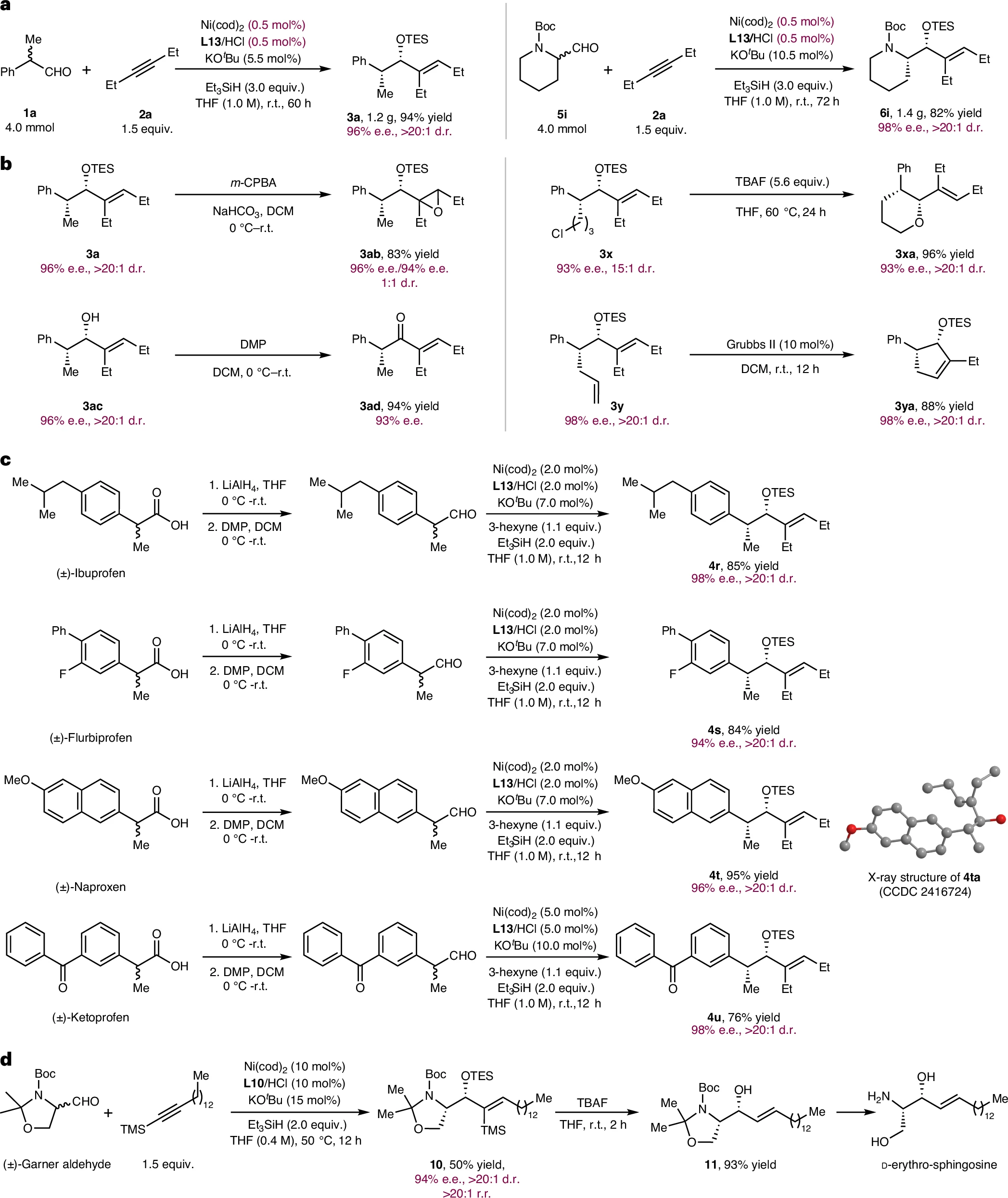
图5:应用研究。
机理实验表明,底物的快速消旋是实现高立体选择性的关键。增加碱可加快消旋化,确保DKR过程高效进行。同时,S-构型底物与催化剂手性匹配,R-构型通过消旋化转化为S-构型,最终实现产物的对映汇聚,且产物绝对构型完全由手性配体决定。
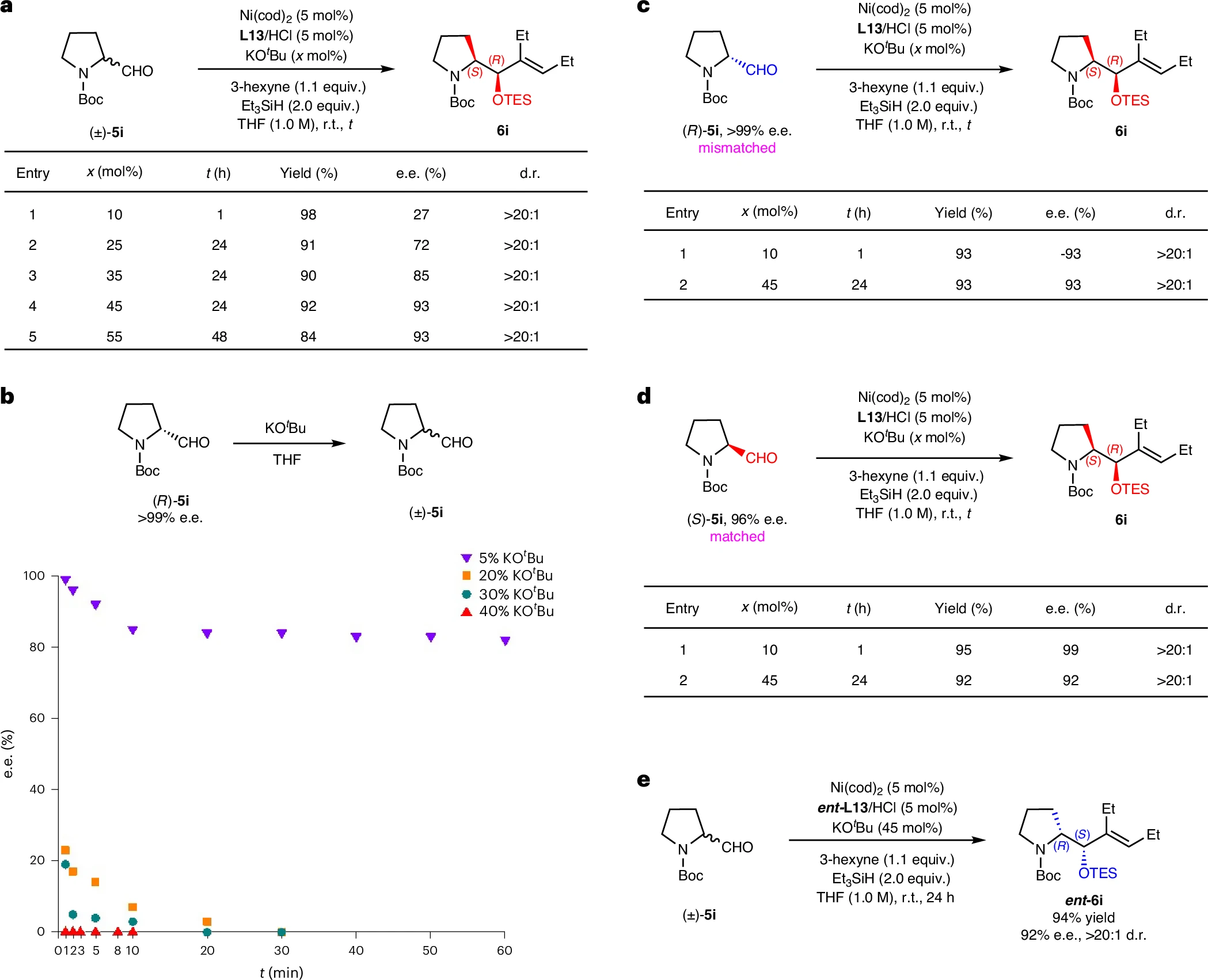
图6:机理研究
该研究为复杂烯丙醇结构提供了高效的合成策略并拓展了羰基化合物动态动力学拆分反应的类型。(来源:科学网)
相关论文信息:https://doi.org/10.1038/s44160-025-00887-4