|
|
|
|
|
肝移植中的移植免疫学、排斥反应和耐受性| MDPI Livers |
|
|
论文标题:Transplant Immunology in Liver Transplant, Rejection, and Tolerance
论文链接: https://www.mdpi.com/2673-4389/4/3/31
期刊名:Livers
期刊主页: https://www.mdpi.com/journal/livers
文章导读:
肝移植是终末期肝病的最有效治疗手段,尽管外科技术与免疫抑制手段不断进步,移植排斥仍是临床面临的重要难题,而肝脏因独特微环境、细胞间相互作用及双重血供等特征成为免疫特惠器官,其移植后的同种免疫反应机制具有特殊性。T细胞与抗原提呈细胞介导的同种免疫反应是移植排斥的核心,可通过直接、间接、半直接三种同种抗原识别途径引发急性细胞排斥、慢性排斥等不同类型的排斥反应,且肝脏的免疫特惠性虽使急性抗体介导的排斥反应发生率低于其他实体器官,但一旦发生往往进展迅猛。深入解析排斥反应与免疫耐受的发生机制,明确调节性T细胞、肝树突状细胞等各类细胞在其中的作用,对优化肝移植治疗方案、诱导免疫耐受、降低排斥反应发生率、提升移植物长期存活率至关重要,本文也正是围绕肝脏移植后排斥与耐受的独特倾向,聚焦各类细胞在该过程中的作用展开综述,为相关研究与临床实践提供理论参考。
肝移植术后排斥反应的主要类型与临床特征
肝移植排斥反应主要分为四类,且各有其独特的临床特征与发生机制。超急性排斥极为罕见,通常发生于 ABO 血型不合的情况,由预先存在的抗体介导导致剧烈移植物损伤;急性细胞排斥最为常见,多发生在移植后早期,由 T 细胞识别供体抗原引发,预后通常较好,对激素治疗敏感;急性抗体介导排斥发生率较低但危害较大,由供体特异性抗体(DSA)介导,常与 T 细胞排斥共存,进展迅速且治疗难度较高;慢性排斥则发生于移植后数月至数年,表现为不可逆的移植物损伤与纤维化,是导致移植物失功的重要原因。这四类排斥反应共同构成了肝移植后主要的免疫攻击形式,其精准分型与鉴别是改善患者预后的关键。
肝移植排斥反应机制:
肝移植排斥反应的核心诱因是供体MHC/HLA分子与受者免疫系统的不匹配,由细胞免疫和体液免疫共同介导、多细胞多途径协同参与;同时肝脏也具备独特的解剖和生理特征(双重血供、HLA-II低表达、有效清除DSA等)构成其免疫特惠性的基础。T细胞是细胞免疫的核心,可通过直接、间接、半直接三种途径识别同种抗原,活化后分泌TNF-α、IFN-γ等细胞因子,激活效应CD4+T细胞和细胞毒性CD8+T细胞,后者通过表达颗粒酶、穿孔素直接损伤肝移植物;记忆T细胞是诱导免疫耐受的重要屏障,而供体来源的组织驻留记忆T细胞(TRM)则可能与降低排斥风险相关。体液免疫以供体特异性抗体(DSA)为关键,其介导的排斥遵循"二次打击"假说,初始损伤使HLA-II类抗原上调,促进DSA结合并激活补体经典途径,通过调理作用、过敏毒素释放、膜攻击复合物形成损伤移植物,同时招募中性粒细胞、巨噬细胞等固有免疫细胞加重损伤。此外,细胞排斥与抗体排斥常相互叠加,T细胞介导的排斥为体液免疫提供辅助,过客白细胞、抗原提呈细胞等也参与推动排斥反应的发生发展。
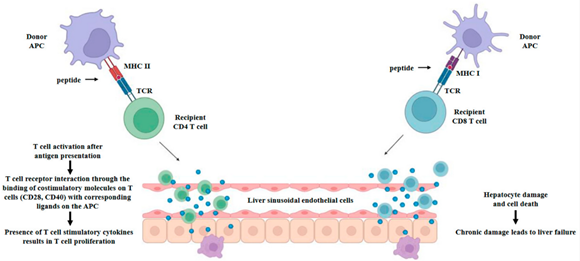
图1. T细胞介导排斥的免疫学基础
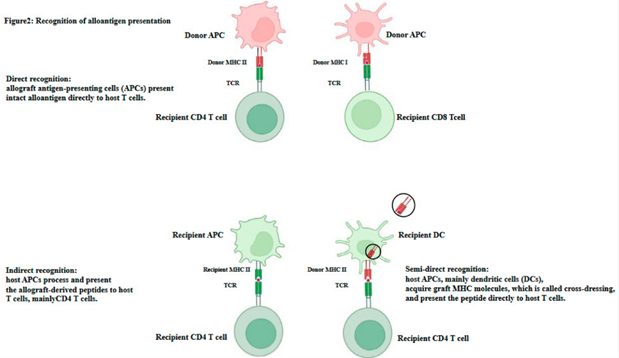
图 2. 同种异体抗原呈递的识别
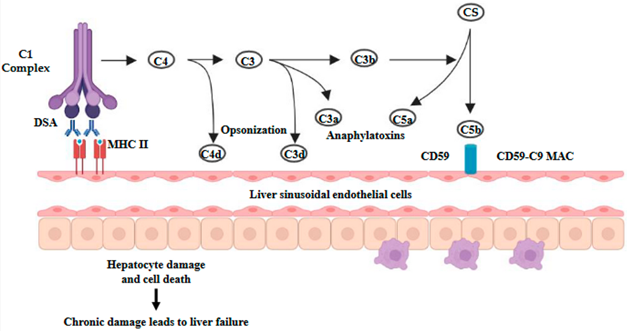
图 3. 抗体介导的排斥反应途径
肝移植免疫耐受的调控机制:
肝移植免疫耐受的调控依托肝脏作为免疫特惠器官的独特解剖结构、血供特点与微环境,由固有免疫细胞、适应性免疫细胞及肝脏特异性实质 / 非实质细胞协同作用实现多维度调控;肝脏 75% 的门静脉血供富含微生物产物和抗原,为免疫耐受奠定微环境基础,肝窦内皮细胞作为肝免疫 “守门人” 介导免疫监视与负调控,库普弗细胞通过分泌抗炎因子、表达免疫抑制配体诱导 T 细胞凋亡和调节性 T 细胞分化,还能通过吞噬凋亡细胞强化抗炎微环境;调节性 T 细胞是适应性免疫中耐受调控的核心,尤其是记忆性调节性 T 细胞,可通过分泌 IL-10、TGF-β 及抑制树突状细胞抗原提呈功能,推动肝免疫平衡向耐受倾斜,肝树突状细胞则具有双重功能,静息 / 未成熟状态下分泌 IL-10、表达 PD-L1 诱导耐受,其功能还受 DAP12、CD39 等分子调控;肝细胞作为非专职抗原提呈细胞,因共刺激分子低表达诱导同种反应性 T 细胞凋亡,其表面 MHC-I 的直接识别是诱导耐受的必要条件,肝星状细胞兼具抗原提呈与免疫抑制功能,可在特定条件下优先诱导调节性 T 细胞,同时自然杀伤 T 细胞、供体来源自然杀伤细胞等也能通过诱导免疫反应偏移、表达免疫抑制分子等方式参与耐受调控,各类细胞间的相互作用共同维持肝脏移植后的免疫耐受平衡。
总结与展望:
研究结论表明,肝脏作为免疫特惠器官,其独特的解剖结构、血管供应与细胞组成造就了特殊的免疫微环境,使肝移植后同时存在排斥与耐受的双重潜在倾向。其中,T 细胞与抗原提呈细胞介导的同种免疫反应是移植排斥的核心驱动因素,而调节性 T 细胞、库普弗细胞、肝树突状细胞等免疫细胞,与肝窦内皮细胞、肝细胞、肝星状细胞等肝脏特异性细胞的相互作用,又共同调控着肝内免疫耐受的建立与维持。这类复杂的细胞间相互作用直接决定了肝移植的最终预后与移植物存活情况。
未来研究需进一步深入解析肝移植中同种免疫反应与免疫耐受的深层细胞和分子机制,尤其应重点关注以下几个方面:一是探索肝组织驻留记忆 T 细胞在排斥与耐受中的具体作用及其调控机制;二是阐明树突状细胞交叉修饰(半直接识别途径)在移植免疫应答中的功能与意义;三是深入解析供体特异性抗体在慢性排斥反应中的致病机制及其干预靶点;四是挖掘 DAP12、CD39 等关键免疫调控分子的治疗潜力,探索其在诱导免疫耐受中的应用价值;五是推动免疫抑制方案的个体化调整与撤药策略研究,识别可实现操作性耐受的受者人群。通过上述研究,为开发更高效、靶向性更强的免疫抑制治疗方案,以及诱导肝移植特异性免疫耐受提供新的靶点与策略,最终实现优化终末期肝病肝移植临床治疗、提升移植物长期存活率、改善患者预后的目标。
Livers期刊主题涵盖肝炎 所有形式;酒精性肝病;非酒精性脂肪性肝病和非酒精性脂性肝炎;肝硬化;胆道疾病;药物性肝损伤;遗传性和代谢性肝病及其并发症;癌症与药物代谢;肝细胞癌;肝纤维化;肝病免疫学;肝病学营养;肝病病理学;肝病的诊断和治疗,为肝病学多学科领域的基础、转化和高级临床研究提供平台。目前已被 ESCI(Web of Science)、Scopus 等国际权威数据库收录。
|
|
主编: Prof. Dr. Hartmut W. Jaeschke
University of Kansas Medical Center, Kansas City, KS 66160, USA
|
|
|
副主编:Prof. Dr. Ralf Weiskirchen
RWTH University Hospital Aachen, D-52074 Aachen, Germany
|
|
2024 Impact Factor
|
2.4
|
|
2024 CiteScore
|
3.2
|
|
Time to First Decision
|
27
|
|
Time to Publication
|
6.7
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。