|
|
|
|
|
FMD | 精彩荐读:单细胞RNA测序揭示神经母细胞瘤肿瘤进展与转移的潜在转录程序 |
|
|
论文标题:Single-cell RNA-seq reveals the transcriptional program underlying tumor progression and metastasis in neuroblastoma
期刊:Frontiers of Medicine
作者:Zhe Nian, Dan Wang, Hao Wang, Wenxu Liu, Zhenyi Ma, Jie Yan, Yanna Cao, Jie Li, Qiang Zhao, Zhe Liu
发表时间:29 May 2024
DOI: 10.1007/s11684-024-1081-7
微信链接:点击此处阅读微信文章
导 读
天津医科大学基础医学院刘喆、天津医科大学肿瘤医院赵强等在Frontiers of Medicine发表研究论文《单细胞RNA测序揭示神经母细胞瘤肿瘤进展与转移的潜在转录程序》(Single-cell RNA-seq reveals the transcriptional program underlying tumor progression and metastasis in neuroblastoma)。本研究通过单细胞RNA测序分析了8个神经母细胞瘤样本的15 447个细胞,识别出具有转移起始能力的“起始”亚群,其高表达细胞周期相关基因经历部分上皮间质转化,该亚群的转录特征可作为独立预后指标且与TGFβ信号通路调控相关。
神经母细胞瘤是儿童最常见的颅外实体肿瘤,约占儿童癌症相关死亡的15%,其起源于神经嵴细胞异常发育,具有高度异质性,从局部无症状肿瘤到广泛转移的恶性疾病不等。60%的患者在诊断时已处于高危状态并伴随转移,尽管过去二十年儿科癌症治疗取得显著进展,但高危神经母细胞瘤患者的5年生存率仍低于50%。目前,虽然通过动物模型发现了一些与转移相关的分子机制,但转移起始细胞的特性及原发与转移灶之间的转录组差异在单细胞水平上仍不明确,这限制了对转移机制的深入理解和靶向治疗策略的开发。
天津医科大学基础医学院刘喆、天津医科大学肿瘤医院赵强等通过单细胞RNA测序技术分析了8个神经母细胞瘤样本,共15 447个细胞,旨在揭示肿瘤进展和转移的转录程序,识别转移起始细胞亚群及其分子特征。通过整合单细胞转录组数据、进化轨迹分析和功能验证,系统探讨了神经母细胞瘤转移的关键机制。
研究首先构建了神经母细胞瘤的单细胞表达图谱。通过流式细胞术分离CD45-DAPI-肿瘤细胞,利用10x Genomics平台进行单细胞测序,经质量控制后保留高质量细胞。采用Seurat进行聚类分析,识别出11个具有不同转录特征的集群,并通过推断染色体拷贝数变异区分恶性与非恶性细胞,发现17q拷贝数增益在恶性细胞中频繁出现,且同一肿瘤的原发与转移灶具有共同染色体拷贝数变异模式,支持单克隆起源(图1)。进一步分析显示,恶性细胞与正常神经母细胞或交感母细胞转录相似,验证了肿瘤细胞的起源。
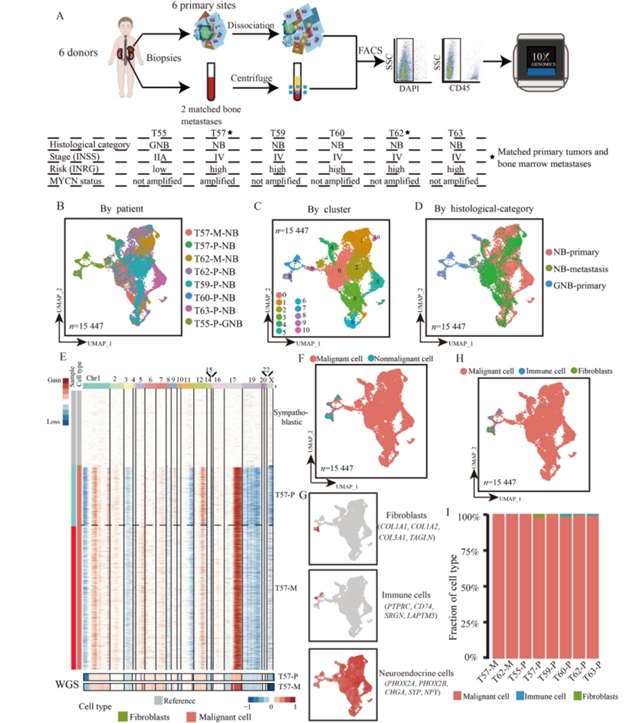
图1 神经母细胞瘤细胞的单细胞RNA测序
为探究转移的进化轨迹,研究聚焦于包含原发和转移灶匹配样本的T57和T62病例,排除非恶性细胞后进行整合UMAP分析。结果显示,恶性细胞主要按肿瘤起源聚类,但Cluster 3在两个病例中均匀分布,且包含原发和转移灶细胞,提示了其在转移中的保守性(图2)。通过RNA速率分析、Monocle2和Slingshot轨迹推断,发现Cluster 3位于轨迹起始点,具有更高的干细胞特性(信号熵和转录多样性),被命名为“起始”亚群。结合单细胞突变分析(T57病例),构建系统发育树显示Cluster 3具有最多样化的突变,骨髓转移灶突变数量多于原发肿瘤,且与原发Cluster 3共享相似突变模式,支持转移起始细胞来源于原发灶Cluster 3(图3)。
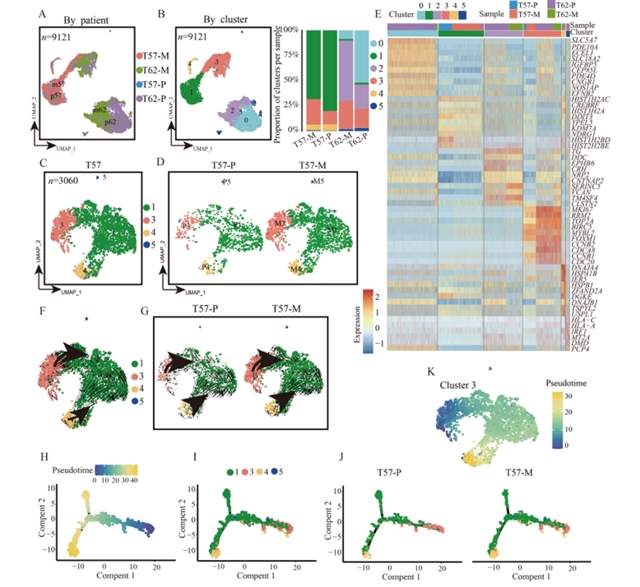
图2 恶性神经母细胞瘤细胞的轨迹建模识别出T57中的“起始”亚群
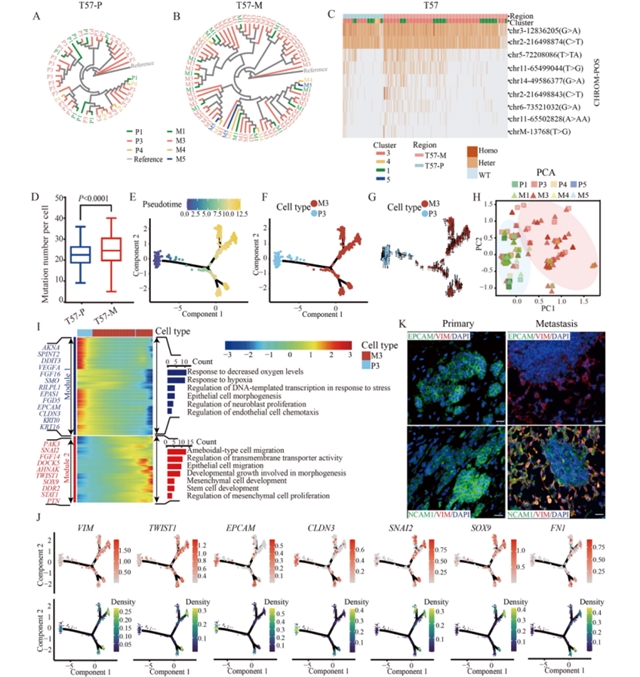
图3 T57中Cluster 3细胞的追踪
对“起始”亚群的分子特征分析显示,其高表达细胞周期相关基因(如MKI67、TOP2A、FOXM1),GSEA富集通路包括DNA复制、有丝分裂检查点等,且多数细胞处于S或G2/M期,提示细胞周期上调在转移起始中的关键作用。转录因子活性分析发现E2F1、FOXM1、MYBL2和TFDP1在Cluster 3中活性显著升高,且沿轨迹逐渐下调,这些转录因子与细胞增殖和DNA修复相关,临床数据显示其高表达与不良预后相关。此外,轨迹分析发现从原发Cluster 3(P3)到转移Cluster 3(M3)存在部分上皮间质转化(p-EMT)程序:上皮标志物EPCAM下调,间质标志物VIM、TWIST1上调,上皮间质转化转录因子SNAI2、SOX9及细胞外基质基因FN1表达增加,免疫荧光验证显示原发灶EPCAM细胞富集,转移灶VIM细胞富集。
细胞通讯分析揭示,“起始”细胞与微环境间的信号交互强于其他肿瘤细胞,其中TGFβ信号通路贡献最大,涉及TGFβ1-TGFβR1/2配受体对。“起始”细胞高表达TGFβ受体及下游SMAD2/3,提示TGFβ信号可能通过诱导部分上皮间质转化促进转移。最后,基于“起始”亚群top150差异基因构建的特征在公共数据集(GSE137804、E-MTAB-8248等)中验证显示,高特征表达与MYCN扩增、INSS 4期、TERT重排及远处转移显著相关,且是独立预后因素,高表达组无事件生存率和总生存率显著降低。
本研究通过单细胞转录组分析识别出具有转移起始能力的“起始”亚群,揭示了细胞周期上调和部分上皮间质转化在转移中的核心作用,阐明了TGFβ信号通路的调控机制,并建立了具有预后价值的转移起始细胞特征。这些发现为理解神经母细胞瘤转移生物学提供了新视角,“起始”细胞特征可作为潜在预后标志物和治疗靶点,为开发抑制转移起始的策略奠定基础。
原文信息
标题
Single-cell RNA-seq reveals the transcriptional program underlying tumor progression and metastasis in neuroblastoma
作者
Zhe Nian1, Dan Wang1, Hao Wang1, Wenxu Liu1, Zhenyi Ma2, Jie Yan3, Yanna Cao3, Jie Li3, Qiang Zhao3, Zhe Liu1,2,4
机构
1. Department of Immunology, School of Basic Medical Sciences, Tianjin Medical University, Tianjin 300070, China
2. Zhejiang Key Laboratory of Medical Epigenetics, Department of Cell Biology, School of Basic Medical Sciences, Hangzhou Normal University, Hangzhou 311121, China
3. Department of Pediatric Oncology, Tianjin Medical University Cancer Institute and Hospital, National Clinical Research Center for Cancer, Key Laboratory of Cancer Prevention and Therapy, Tianjin’s Clinical Research Center for Cancer, Tianjin 300060, China
4. Collaborative Innovation Center for Cancer Personalized Medicine, Nanjing Medical University, Nanjing 211166, China
通讯作者
Qiang Zhao, Zhe Liu
引用这篇文章
Zhe Nian, Dan Wang, Hao Wang, Wenxu Liu, Zhenyi Ma, Jie Yan, Yanna Cao, Jie Li, Qiang Zhao, Zhe Liu. Single-cell RNA-seq reveals the transcriptional program underlying tumor progression and metastasis in neuroblastoma. Front. Med., 2024, 18(4): 690-707
https://doi.org/10.1007/s11684-024-1081-7
https://journal.hep.com.cn/fmd/EN/10.1007/s11684-024-1081-7
https://link.springer.com/article/10.1007/s11684-024-1081-7
感谢作者对Frontiers of Medicine的信任和支持。
期刊简介
Frontiers of Medicine (2026年起更名为MedScience)是中国工程院院刊,由教育部主管,高等教育出版社、中国工程院与上海交通大学医学院附属瑞金医院共同主办。期刊聚焦医学前沿领域的学术进展,关注国际研究热点与中国优秀研究成果,主编为陈赛娟院士、张伯礼院士和王小凡院士。主要报道领域涵盖临床医学、基础医学、转化医学、流行病学、公共卫生、中医药学和人工智能医学等,刊载文章类型包括Research Article、Review、Perspective、Editorial、Case Report、Comment、Letter等。
期刊已被SCI、PubMed、Scopus、中国科技核心期刊、中国科学引文数据库(CSCD)核心库、第三批临床医学领域高质量科技期刊分级目录T1级、化学文摘数据库(CAS)等权威数据库收录,在2025中国科学院文献情报中心期刊分区表医学大类中位列二区。
在线浏览
https://journal.hep.com.cn/fmd
https://link.springer.com/journal/11684
投稿
https://mc.manuscriptcentral.com/fmd
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。