|
|
|
|
|
从更精准的诊断到更早的治疗:阿尔茨海默病的快速发展 | MDPI Medicina |
|
|
论文标题:From Better Diagnostics to Earlier Treatment: The Rapidly Evolving Alzheimer’s Disease Landscape
论文链接:https://www.mdpi.com/1648-9144/61/8/1462
期刊名:Medicina
期刊主页:https://www.mdpi.com/journal/medicina
研究背景:
阿尔茨海默病(AD)是全球 65 岁以上人群痴呆的主要类型,患者会逐渐出现记忆衰退、执行功能受损,最终丧失日常活动能力,且临床诊断准确性受疾病阶段、合并症等影响较大 —— 约 39% 临床诊断为 AD 的患者,死后病理检查仅确认存在 AD 病理,30% 为非 AD 病理,存在较高误诊风险。同时,AD 带来沉重经济负担,全球年花费约 1 万亿美元,且病例数呈指数增长,对医疗系统构成严峻挑战。传统 AD 诊断依赖临床症状,难以在治疗窗口期(无症状或轻度认知障碍阶段)识别疾病;而治疗领域长期受 “淀粉样蛋白假说” 主导,但靶向 Aβ 的临床研究(如单抗 gantenerumab)多次失败,且血脑屏障(BBB)阻碍 98% 小分子药物、近 100% 大分子药物进入脑组织,导致多数潜在疗法无法起效。
这篇由多位来自不同国家的专家共同撰写的综述同时结合神经心理测试分析认知与影像标志物的关联,总结 AD 诊疗进展并指出当前挑战。
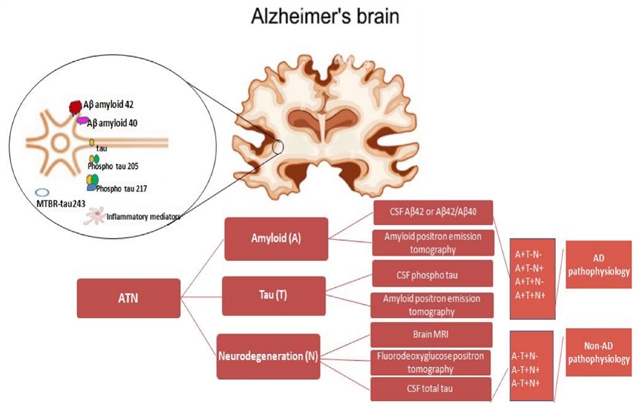
图 1. ATN 概况及相应的生物标志物类别。
研究过程与结果
以表格与示意图结合形式,标注 A(β 淀粉样蛋白,如 Aβ42/Aβ40)、T(病理性 tau,如 p-tau217)、N(神经退行性变,如脑 MRI 萎缩)三大类生物标志物,明确 “A+T+N+” 为 AD 典型病理组合,同时区分非 AD 病理(如路易体痴呆)的标志物模式,帮助理解 AD 的生物学诊断标准。Aβ42/Aβ40 比值因其卓越的诊断工具而备受青睐。血浆 Aβ42/Aβ40 水平在症状出现前阶段会发生改变,从而能够早期发现认知正常人群的 Aβ 病理,其准确度与认知异常人群相当。P-tau217 是 p-tau 标志物中最强的,是一种强大的诊断工具,能够以更高的准确度区分 AD 与其他痴呆症。目前认为,最强的诊断性 p-tau 生物标志物是 P-tau217(与 p-tau181、p-tau231 和 p-tau205 相比)。受试者工作特征曲线下面积 (AUC) 分别为 0.943 和 0.914,p = 0.026,表明脑脊液 (CSF) p-tau217 是比 p-tau181 更有效的诊断工具。同时,脑脊液 p-tau217 水平能够可靠地区分 AD 与其他痴呆症,其准确度优于 p181。血浆 p-tau181 和 p-tau217 水平可准确预测未来(2 至 6 年内)轻度认知障碍进展为 AD 痴呆的时间。然而,p-tau217 在无症状期升高,并随着 AD 的进展而变化,从而可以早期发现和预测 AD;而较高的 p-tau217 水平则提示认知能力快速下降。鉴于外周 A-T-N-X 框架中的 T,p-tau217 凭借上述优势,是一个合适的生物标志物。
脑脊液 p-tau231 在确诊 Aβ 病理之前就已经显著升高,并且与 Aβ PET 信号在 AD 早期通常受损的脑区中的定位有关。虽然脑脊液 p-tau231 在临床前期提前终止了 Aβ 的改变,但脑脊液 p-tau217 在疾病症状期表现出最大的倍数变化增幅。本研究的一个重要发现是,即使没有明确的 Aβ 病理,脑脊液 p-tau231 仍然显著升高。在认知功能未受损的患者中,脑脊液 p-tau231 与 Aβ PET 定位密切相关,这些定位在阿尔茨海默症早期经常受到影响的脑区,例如后扣带皮层、楔前叶和内侧眶额叶。这些生物标志物有助于识别非典型或混合病例中的“阿尔茨海默症神经化学指纹”,这已通过 PET 成像得到证实。
分子机制:
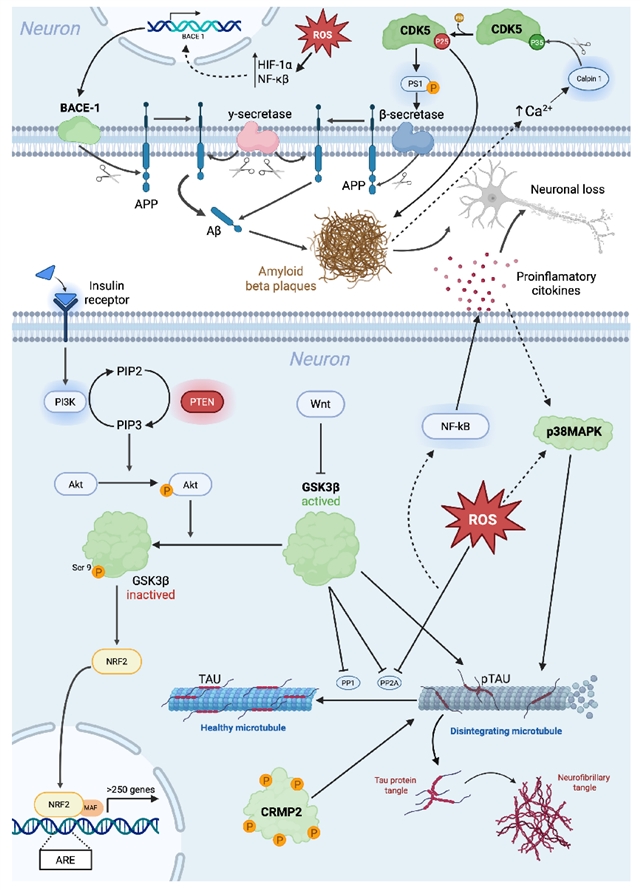
图 2. 阿尔茨海默病所涉及的分子机制示意图
AD 的主要神经病理学特征包括细胞外 β-淀粉样蛋白 (Aβ) 沉积形成淀粉样斑块,以及细胞内神经原纤维缠结 (NFT) 内过度磷酸化的 tau 蛋白积聚。此外,AD 还与血管功能障碍、神经炎症、氧化应激以及脂质和鞘脂 (SL) 代谢失调等病理过程有关,涉及多种分子机制。
研究总结
本文明确 AD 诊疗已从 “单一 Aβ 靶向” 转向 “多维度干预”:生物标志物(如血浆 p-tau217、ATN 框架)实现 AD 早期精准识别,为提前干预奠定基础;分子机制研究揭示 AD 的多因素本质,提示需同时调控 Aβ、tau、神经炎症等病理环节;BBB 递送技术(如聚焦超声、靶向纳米粒)突破药物脑内递送瓶颈,为疗法起效提供关键支撑;新型疗法(如 Lecanemab、基因编辑)虽显示潜力,但仍需大样本长期研究验证疗效。
未来研究需聚焦三方面:一是优化生物标志物联合应用策略,提高 AD 早期诊断的特异性;二是开发多靶点疗法,结合 BBB 递送技术提升脑内药物浓度;三是推进个体化治疗,基于患者 APOE 基因型、病理亚型制定精准方案,最终实现 AD 从 “对症治疗” 向 “疾病修饰” 的突破。
Medicina 期刊介绍
主编:Prof. Dr. Edgaras Stankevicius, Lithuanian University of Health Sciences, Kaunas, Lithuania
期刊涵盖心脏病学和心血管内科、肺病学、妇产科、神经科、骨科和运动医学、牙科、外科等领域。目前已被 DOAJ、Scopus、SCIE (Web of Science)、PubMed、MEDLINE、PMC、Embase 等数据库收录。
|
2024 Impact Factor
|
2.4
|
|
2024 CiteScore
|
4.1
|
|
Time to First Decision
|
17.5 Days
|
|
Acceptance to Publication
|
2.6 Days
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。