|
|
|
|
|
miR-29调控代谢开关 助力肠道干细胞再生修复 Engineering |
|
|
论文标题:The Regeneration of Intestinal Stem Cells Is Driven by miR-29-Induced Metabolic Reprogramming
期刊:Engineering
DOI:https://doi.org/10.1016/j.eng.2024.08.008
微信链接:点击此处阅读微信文章

肠道上皮作为人体重要的屏障组织,其损伤后的高效再生修复对维持肠道功能至关重要。中国农业大学郭慧媛教授团队联合中原食品实验室、中国科学院生物物理所等机构的研究人员,在中国工程院院刊《Engineering》发表了题为“The Regeneration of Intestinal Stem Cells Is Driven by miR-29-Induced Metabolic Reprogramming”的研究论文,林莹莹、陆瑶、王宇琦为共同第一作者。研究团队揭示了miR-29a/b通过调控代谢重编驱动Lgr5?肠道干细胞再生的新机制,为肠道损伤修复的临床干预提供了新的潜在靶点。
研究团队首先分析了癌症基因组图谱(TCGA-COAD/READ)的miRNA测序数据,发现hsa-miR-29a-3p与hsa-miR-29b-1-3p在结直肠腺瘤组织中高于配对正常组织,且这两种分子高表达的患者放疗后总生存期更短。为进一步明确miR-29a/b在肠道中的表达特征,研究人员通过原位杂交实验观察到,miR-29a/b集中分布在小肠隐窝底部,与肠道干细胞标志物Lgr5-GFP存在共定位。在12 Gy全身辐照损伤模型中,miR-29a/b的表达呈现明显的时序变化:在凋亡高峰的24小时保持低水平,修复期第2至3天显著升高,第5天隐窝分化完成后恢复至基线水平,这一表达窗口与肠道再生过程高度同步。
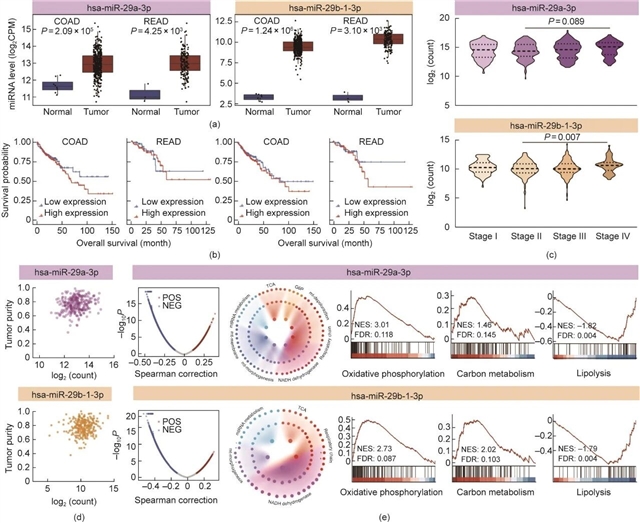
图1 MiR-29a/b与肠道肿瘤及代谢相关。
为验证miR-29a/b的功能,研究团队构建了两种基因敲除小鼠模型——Mir29ab1全身敲除小鼠(Mir29ab1-/-)和肠上皮特异条件敲除小鼠(Mir29ab1villin-KO)。辐照处理后,敲除小鼠的体重下降百分比明显大于野生型小鼠,Kaplan-Meier生存曲线显示其生存状况显著变差。HE染色结果显示,敲除小鼠肠道的新生隐窝数量稀疏,Ki67+增殖细胞在每个隐窝中的数量减少,Olfm4+再生干细胞数量同步下降,修复终点时PAS+杯状细胞与溶菌酶+潘氏细胞的数量也显著不足。体外隐窝培养实验中,来自Mir29ab1-/-小鼠的类器官出芽率降低,在Wnt3a撤除后无法由囊泡再形成隐窝;EdU掺入实验显示其G0/G1期细胞占比升高,Lgr5-GFP+细胞比例下降,阿利新蓝阳性分化细胞增多,表明miR-29a/b缺失会导致肠道干细胞从自我更新状态向分化状态倾斜。
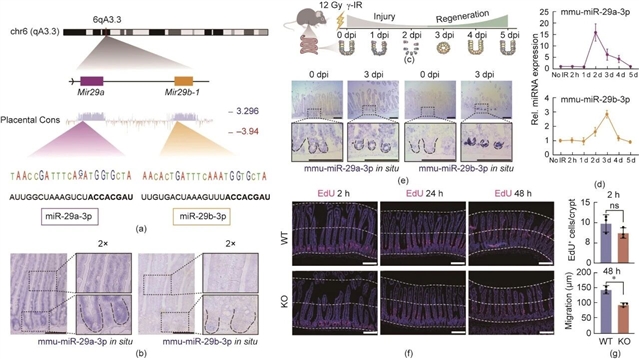
图2 MiR-29a/b在肠道隐窝中表达最高,并在损伤后修复阶段变化。
Seahorse细胞能量代谢分析为上述表型提供了代谢层面的解释:Mir29ab1-/-类器官的基础耗氧率、最大呼吸能力及ATP相关呼吸均高于野生型。[U-¹³C]棕榈酸示踪实验发现,敲除小鼠隐窝中(M+2)乙酰肉碱与(M+2)柠檬酸丰度增加,提示脂肪酸氧化(FAO)通量升高。透射电镜观察与mtDNA拷贝数检测排除了线粒体数量差异的影响,表明代谢流改变源于底物选择的变化。进一步实验显示,使用FAO抑制剂etomoxir抑制CPT1A后,敲除类器官的耗氧率下降幅度更大,证实其对FAO的依赖增强。而用FAO激活剂GW501516处理LGR5+ LS174T细胞,可提升基础耗氧并促进阿利新蓝阳性分化,联用氧化磷酸化(OXPHOS)抑制剂UK5099则能削弱这一促分化效应,说明FAO通过升高OXPHOS驱动肠道干细胞分化。
转录组与代谢组联合分析显示,Mir29ab1-/-隐窝中“脂肪酸β-氧化”“长链脂肪酸进入细胞”等GO条目显著富集,Cpt1a、Acadm、Hmgcs2等FAO关键酶在Lgr5high分选干细胞中特异性上调,而在Lgr5-分化细胞中未见一致变化,提示miR-29a/b的作用具有细胞类型选择性。通过TargetScan、miRD8、PicTar交叉预测,研究人员锁定转录因子Hnf4g为miR-29a/b的直接靶点,其3′-UTR区域携带保守的miR-29种子结合序列。双荧光素酶报告实验证实,miR-29a/b模拟物可降低野生型Hnf4g 3′-UTR的荧光强度,突变种子序列后该作用消失;抑制miR-29a/b则会使Hnf4g mRNA及核蛋白水平升高。
人结直肠息肉活检样本检测显示,MIR29A/B与HNF4G表达呈负相关。功能验证实验表明,过表达HNF4G的LS174T细胞会重现敲除miR-29的表型,包括FAO相关蛋白上调、基础耗氧与OXPHOS升高、阿利新蓝阳性分化细胞增加;而siRNA敲低HNF4G可逆转miR-29抑制引起的FAO增强、OXPHOS上升及促分化趋势。
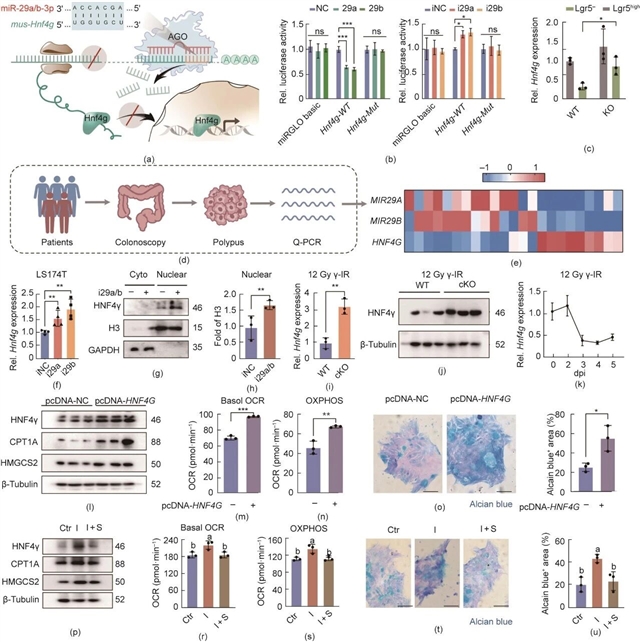
图3 Hnf4g是miR-29a/b调控Lgr5+细胞代谢和干性的靶基因。
此项研究对ISCs在再生过程中的代谢可塑性提供了全面的探究。研究发现暂时抑制FAO和OXPHOS水平对于ISCs的快速自我更新不可或缺,这也挑战了之前基于稳态和长期影响研究的观点。研究团队揭示了miR-29a/b是在损伤状况下调控ISCs代谢可塑性的重要因子,靶向作用miR-29a/b或Hnf4γ有望用于治疗炎症性肠病、克罗恩病等疾病,或用于改善衰老的肠道更新,还有潜力用于防止肿瘤的愈后复发,但这需要更多的研究来证明。
论文信息:
Yingying Lin,Yao Lu,Yuqi Wang,Cong Lv,Juan Chen,Yongting Luo,Heng Quan,Weiru Yu,Lining Chen,Ziyu Huang,Yanling Hao,Qingyu Wang,Qingfeng Luo,Jingyu Yan,Yixuan Li,Wei Zhang,Min Du,Jian He,Fazheng Ren,Huiyuan Guo. The Regeneration of Intestinal Stem Cells Is Driven by miR-29-Induced Metabolic Reprogramming. Engineering, 2024, 42(11): 43-62 DOI:10.1016/j.eng.2024.08.008
更多内容
Engineering 2024年11月刊目录 | 精准营养与健康专题
精准营养与工程学的交叉融合及协同创新展望
中原食品实验室研究发现:个性化维生素D补充,有益心脏健康
抗衰老新发现:年轻小鼠粪菌移植让老年小鼠皮肤年轻化
第十三届全国环境化学大会《Engineering》期刊专场会议议程
Engineering征稿启事:人工智能赋能工程科技
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。