近年来,新辅助免疫化疗(nICT)在局部晚期胃癌治疗中取得突破性进展,显著提高了病理缓解率和手术切除率。然而,仍有接近一半的的患者无法从联合治疗中获益,耐药问题成为制约疗效的关键瓶颈。如何精准筛选获益人群、破解耐药机制,成为胃癌精准治疗领域亟待解决的科学问题。
2月19日,中国工程院院士、中山大学肿瘤防治中心教授徐瑞华团队在《癌细胞》(Cancer Cell)发表了一项重要研究成果。该研究依托其团队前期开展的NEOSUMMIT-01前瞻性随机对照试验,通过对研究队列进行深度多组学检测与动态分析,系统揭示了胃癌新辅助免疫化疗的疗效预测标志物与耐药机制。
多维生物标志物预测疗效
胃癌是全球第五大常见恶性肿瘤,也是癌症相关死亡的第四大原因。
论文共同第一作者、中山大学肿瘤防治中心研究员赵齐指出,肿瘤微环境的异质性是导致治疗反应差异的核心因素。既往研究多局限于单一组学、单臂设计或治疗前静态样本,缺乏对免疫化疗过程中基因组与免疫微环境动态演变的系统性解析。
为此,研究团队依托NEOSUMMIT-01随机对照临床试验,创新性地开展了多组学转化研究,通过整合全外显子测序、转录组、蛋白质组及单细胞测序数据,绘制了胃癌免疫化疗响应的“动态全景图”。
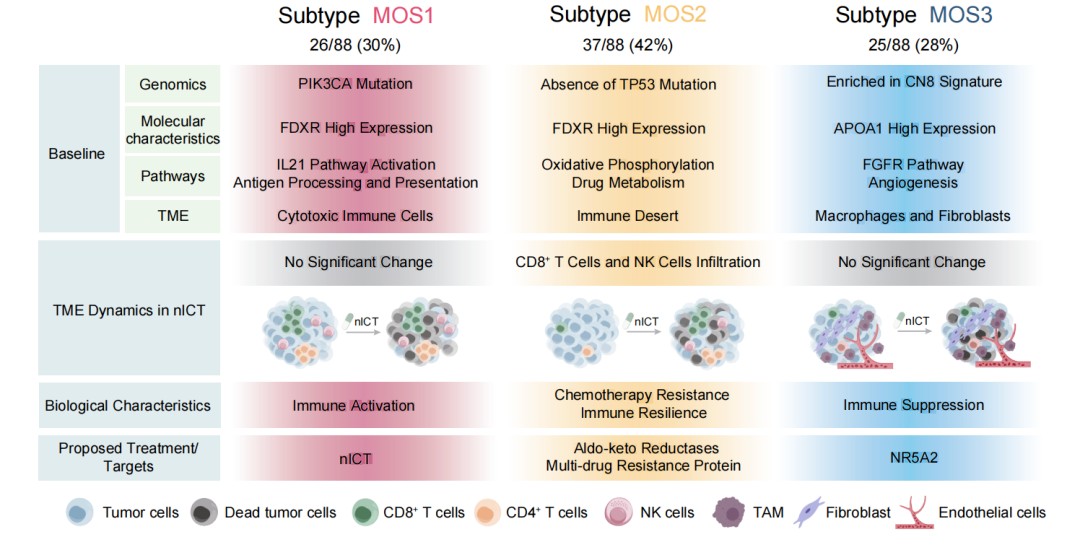 胃癌多组学治疗分型特征。研究团队供图
胃癌多组学治疗分型特征。研究团队供图
研究团队创新建立交互选择模型,系统筛选出特异性预测nICT疗效的分子标志物体系。在基因组层面,突变特征SBS19富集与免疫抑制通路激活相关、提示不良预后,该发现在独立食管癌队列中得到验证;HLA分型方面,HLA-B*15:02阳性患者抗原呈递功能缺陷,表现为NK细胞活化、TCR信号及干扰素反应通路全面抑制,单细胞水平证实其肿瘤浸润CD8+T细胞细胞毒性显著减弱。
在转录和蛋白组层面,FDXR高表达患者铁死亡调控活跃、免疫治疗生存获益明确,该标志物在其他三个独立胃癌免疫治疗队列中均显示预测价值;相反,FGFR通路激活则通过促进免疫抑制信号传导导致耐药,与患者不良预后相关。
“上述标志物覆盖了DNA修复、抗原呈递、细胞死亡及信号通路等多个生物学维度,既可独立指导敏感人群的筛选,亦可整合构建复合预测模型,为临床制定个体化治疗决策提供依据。”论文共同通讯作者、中山大学肿瘤防治中心教授袁庶强表示。
鉴定五种肿瘤微环境生态型
研究团队基于单细胞测序数据,鉴定出五种肿瘤微环境生态型(EC1-EC5),系统阐明了不同免疫景观对nICT的治疗响应特征:
EC1(免疫激活型):以组织驻留记忆T细胞和细胞毒性T细胞富集为特征,对nICT治疗响应最佳。
EC2(三级淋巴结构型):富含成熟B细胞及三级淋巴结构,nICT可诱导其显著扩增。
EC3(血管正常化型):以促血管生成髓系细胞为标志,nICT可抑制其免疫抑制功能。
EC4(细胞外基质型):基质成分富集,对nICT反应中等。
EC5(代谢抑制型):以TREM2+巨噬细胞富集和脂质代谢活跃为特征,对nICT耐药。
多色免疫组化验证显示,EC1型肿瘤富含CD8+效应T细胞和GZMB+细胞,而EC5型则以TREM2+巨噬细胞为主,形成“冷肿瘤”微环境。研究深入解析了EC5型耐药的细胞互作机制,发现一群具有肠上皮样特征的APOA1+肿瘤细胞是介导免疫抑制的关键“推手”。
机制研究表明,APOA1+肿瘤细胞通过分泌载脂蛋白APOA1/APOB,与TREM2+巨噬细胞表面的TREM2受体结合,激活PI3K-SYK信号通路,诱导巨噬细胞向免疫抑制表型分化。小鼠实验证实,联合TREM2阻断可有效逆转APOA1过表达所介导的免疫化疗耐药,恢复抗肿瘤免疫应答。研究还发现,转录因子NR5A2是调控APOA1表达的核心驱动因子。
多组学分型模型优化临床决策
“我们系统鉴定了预测胃癌新辅助免疫化疗疗效的关键分子标志物,揭示了APOA1+肿瘤细胞与TREM2+巨噬细胞相互作用介导耐药的免疫微环境重塑机制,并构建了整合基因组特征与肿瘤免疫微环境的多组学分型(MOS)框架。”论文共同通讯作者徐瑞华向《中国科学报》表示。
据介绍,基于基因组、转录组及微环境特征,研究团队构建了三种多组学亚型(MOS1-3),实现患者精准分层:
MOS1(免疫激活型,30%):富集PIK3CA突变、FDXR高表达,基线期即存在细胞毒性免疫细胞浸润,nICT响应率高达88%(对比化疗组的29%)。
MOS2(免疫可塑型,42%):以TP53野生型为主,基线呈免疫“荒漠”表型,但nICT可诱导CD8+ T细胞和NK细胞显著浸润。
MOS3(免疫抑制型,28%):富集CN8拷贝数异常、APOA1高表达、FGFR通路激活,并有TREM2+巨噬细胞及成纤维细胞浸润,对nICT无显著获益。该模型在三个抗PD-1单药队列和两个单纯化疗队列中得到了验证,显示出良好的预后预测价值和跨治疗场景的适用性。
该研究全面描绘了影响胃癌免疫联合化疗反应的核心基因组变异与细胞图谱,为克服耐药及优化临床决策提供了新靶点和新策略。“通过精准筛选获益人群、破解耐药机制,有望推动胃癌精准治疗迈向新台阶,为更多胃癌患者带来长期生存的希望。”(来源:中国科学报 朱汉斌)
相关论文信息:https://doi.org/10.1016/j.ccell.2026.01.015