|
|
|
|
|
睡眠不足对饥饿相关激素的影响:荟萃分析与系统评价| MDPI Obesities |
|
|
论文标题:The Impact of Sleep Deprivation on Hunger-Related Hormones: A Meta-Analysis and Systematic Review
论文链接:https://www.mdpi.com/2673-4168/5/2/48
期刊名:Obesities
期刊主页:https://www.mdpi.com/journal/obesities
在现代快节奏的生活中,睡眠不足已成为许多人的常态。长期以来,普遍观点认为,睡眠时间短与体重指数(BMI)升高存在关联,而其背后的机制很可能与调节食欲的激素——瘦素(Leptin)和生长激素释放肽(Ghrelin)——的紊乱有关。大量先前研究声称,仅仅一晚睡眠不足就可能导致“饥饿激素” Ghrelin 水平上升,而“饱腹感激素” Leptin 水平下降,从而增强食欲,最终可能导致体重增加和肥胖。
然而,发表在MDPI旗下期刊《Obesities》上的一篇题为《睡眠剥夺对饥饿相关激素的影响:一项荟萃分析与系统评价》(The Impact of Sleep Deprivation on Hunger-Related Hormones: A Meta-Analysis and Systematic Review)的文章,通过对现有高质量随机对照试验进行严格汇总分析,得出了与此前观点不尽相同的结论:短期内,睡眠剥夺并未一致性地改变循环中的瘦素和生长激素释放肽水平。
研究背景:睡眠、激素与食欲的复杂关系
睡眠远不止是休息,它是一个对大脑功能、身体健康至关重要的恢复性过程,深刻参与新陈代谢、食欲调节、免疫、激素功能和心血管系统调节。据统计,美国有三分之一的成年人日常睡眠时间低于推荐量。
睡眠剥夺指的是“表现出睡眠数量、结构和/或质量不足的异常睡眠状况”。部分睡眠剥夺(24小时内睡眠少于6小时)和完全睡眠剥夺(24小时内睡眠0小时)都被认为对食欲调节和饥饿激素产生负面影响。
食欲的调控核心在于两种关键激素:
1.瘦素 (Leptin):主要由脂肪细胞分泌,被称为“饱腹感激素”。其水平升高会向大脑(下丘脑)发出信号,减少能量摄入并增加能量消耗。
2.生长激素释放肽 (Ghrelin):主要由胃部分泌,被称为“饥饿激素”。其水平升高会刺激食欲,增加食物摄入。
这两者像一个反馈回路,共同工作以控制能量平衡和维持体重。理论认为,睡眠不足会破坏这个精密回路,导致激素水平变化,从而增加肥胖风险。但过去实验室研究的结果并不一致,可能源于研究设计上的差异。
研究方法:严谨的系统评价与Meta分析
为了更清晰地回答睡眠剥夺究竟是否会影响这些饥饿激素,研究采用了最系统、严谨的方法:
1.文献检索与筛选:研究人员遵循PRISMA指南,系统检索了PubMed、CINAHL和Google Scholar等数据库(图1)。筛选过程极其严格。
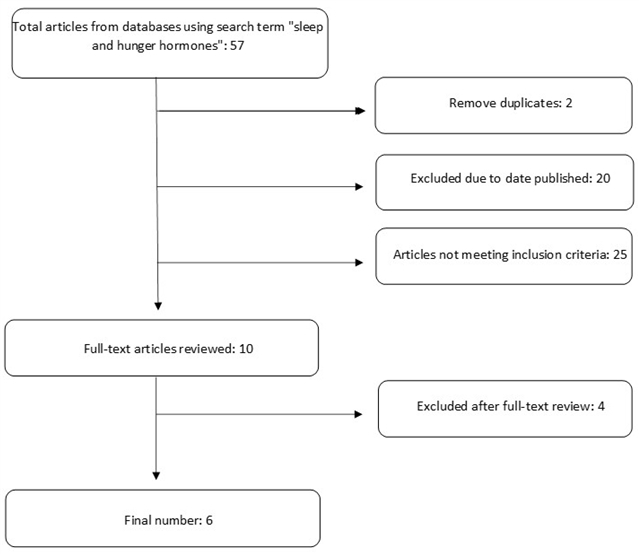
图 1. 搜索选择。
2.纳入与排除标准:只纳入符合以下条件的随机对照试验(RCT):
•研究对象为18岁及以上成年人。
•发表于2013-2023年间经同行评审的英文期刊。
•每个实验组至少10名参与者。
•实验性地操纵了参与者的睡眠时间(通常限制睡眠4-5小时或保持24小时清醒)。
•通过血液样本测量了瘦素和Ghrelin的水平。
•排除了有睡眠障碍、使用睡眠药物或有其他急慢性疾病的参与者,以避免混淆因素。
3.质量评估:使用专业的质量标准检查表(QCC)对纳入研究进行偏倚风险评估,确保最终分析只包含高质量的研究。
4.数据分析:最终,共有6项RCT研究(总计141名参与者)被纳入最终的Meta分析。研究人员使用随机效应模型来计算睡眠剥夺对两种激素影响的标准化均值差(SMD)和95%置信区间(CI)。
研究结果:出乎意料的发现与显著的异质性
分析结果挑战了传统的认知:
•对Ghrelin(饥饿激素)的影响:汇总分析显示,睡眠剥夺后,Ghrelin水平未发生显著变化(SMD: -0.27, 95% CI: -1.00, 0.46, p = 0.4712)(图2)。
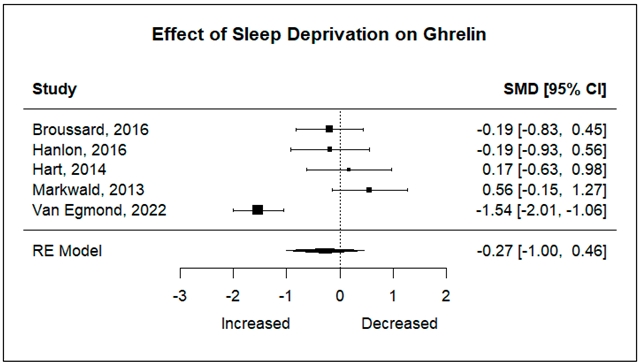
图2: 睡眠不足对生长素释放肽水平影响的森林图
•对Leptin(饱腹感激素)的影响:同样,睡眠剥夺后,Leptin水平也未发生显著变化(SMD: 0.10, 95% CI: -0.22, 0.42, p = 0.5266)(图3)。
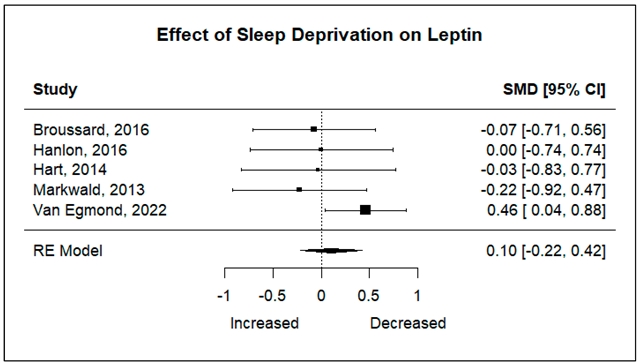
图3: 睡眠不足对瘦素水平影响的森林图
然而,一个关键发现是显著的异质性。特别是在Ghrelin的分析中,异质性非常高(I² = 83.83%, p < 0.001),这意味着不同研究之间的结果差异巨大,远超出随机误差可解释的范围。而Leptin的异质性则不显著(I² = 21.86%, p = 0.4049),说明各研究结果相对一致。
讨论:为何结果不一致?
为什么这项Meta分析的结果与许多先前研究的主张相反?作者在讨论中指出了几个可能解释结果变异性的关键因素:
1.研究设计存在巨大差异:
•采血时间点:这是导致异质性的一个重要原因。有的研究在早晨某一固定时间点(如7:30)采血;有的研究则在24小时内每15-30分钟或每小时频繁采血,并取其平均值作为分析数据。测量时间点的不同直接影响了激素水平的可比性。
•干预持续时间:有的研究只干预一晚(急性睡眠剥夺),而有的研究则让参与者连续多天(如4晚)处于睡眠限制状态。干预时长不同,身体的生理反应也可能不同。
2.参与者基线特征(特别是BMI):
•血液中的瘦素水平与体脂率直接相关,肥胖者(BMI高)的基线瘦素水平本就显著高于体重正常者。纳入的研究中,有的参与者平均BMI在健康范围(18-24.9),而有的研究则包含了超重或肥胖的参与者(平均BMI分别为27.4和31.0)。这种基线水平的差异可能影响了他们对睡眠剥夺的反应程度,从而混淆了整体结果。
结论与展望
本研究的主要结论是:基于当前纳入的短期、实验室控制的随机对照试验证据,没有显著的证据表明睡眠剥夺会直接、一致性地改变循环中的瘦素或生长激素释放肽水平。 因此,睡眠不足导致肥胖的机制,可能并非简单地通过这两种饥饿激素的急性变化来实现。
当然,这并不意味着睡眠与肥胖无关。大量流行病学证据依然支持睡眠时间短与肥胖风险增加存在关联。其背后的机制可能更为复杂,可能涉及:
•其他激素或神经通路(如内源性大麻素系统)。
•睡眠不足对大脑前额叶皮层活动的影响,导致决策能力下降、对高热量食物的渴望增加等行为学改变。
•因疲劳导致的日间活动量减少。
作者强调,未来研究需要采用更标准化、更统一的研究设计,包括控制采血时间、明确干预时长、仔细匹配参与者的基线特征(如BMI),并探索更精确的测量方法,才能最终阐明睡眠剥夺影响食欲调节和体重的精确神经内分泌机制。
在此之前,虽然这项研究对“睡眠不足直接改变饥饿激素”的简单模型提出了挑战,但它无疑推动了该领域向更严谨、更深入的方向发展。保证充足、高质量的睡眠,对于整体健康而言,依然是一个毋庸置疑的良好建议。
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。