|
|
|
|
|
干扰素信号通路在新冠病毒感染和疫苗接种初期的动态演化 | MDPI Viruses |
|
|
论文标题:Distinctive Temporal Profiles of Interferon-Stimulated Genes in Natural Infection, Viral Challenge, and Vaccination
论文链接: https://www.mdpi.com/1999-4915/17/8/1060
期刊名:Viruses
期刊主页:https://www.mdpi.com/journal/viruses
研究背景
干扰素信号通路是人体对抗病毒入侵的第一道免疫防线,但是干扰素信号通路在新冠病毒感染中的作用众说纷纭。有一些研究指出干扰素信号通路在新冠病毒感染中被抑制了,从而导致无法在第一时间控制病毒的复制,并由此引发重症。干扰素信号通路的一些遗传缺陷以及相关自抗体的发现证实了这个观点,还有研究通过动物模型对干扰素信号通路的抑制验证了这一观点。但是,另有一些研究发现对于特定干扰素信号通路的激活有利于重症患者康复。还有一些更复杂的关于干扰素信号通路激活程度和重症的相关性结论。在干扰素治疗一类的众多临床试验中,结论各不相同,总体来说似乎没有明显效果。其实,干扰素信号通路有三种已知类型,包含数百个基因,其在病毒感染中的作用可能需要更细致深入的研究。
内容概要
本研究专注于对I型和II型干扰素信号通路的人体外周血转录组数据分析。我们分析了三组干扰素刺激基因(interferon stimulated genes, ISGs),包括一组I型干扰素信号通路基因(ISGa)和两组II型干扰素信号通路基因(GBPs和HLAd)。分析发现这三组基因在自然感染、主动感染(viral challenge)和疫苗接种之后有着错综复杂的动态演化规律。在自然感染的住院患者中,GBPs和ISGa是显著激活的(其中ISGa激活更显著),并且其激活程度在轻症患者中跟入院时PCR测得的Ct值有一定反向相关性。与此相反,另一组基因HLAd是显著抑制的,而且其抑制程度跟重症高度关联。另外,在一些脓毒症患者和接受ECMO治疗的患者中,也发现了GBPs的抑制现象。这三组基因在感染后的动态演化则更为复杂。总体来说,HLAd的抑制在重症患者中恢复的特别慢。需要强调的是,患者不一定明确的感染时间给这方面的研究带来了不小的挑战
有幸的是,主动感染试验能绘制出清晰的动态演化模型。在主动感染之后(轻症),ISGa的激活程度也显著高于GBPs的激活程度(图中上部)。GBPs的激活一般在一周之后开始回归正常,而ISGs则需要在两周之后开始回归正常,而且ISGa的激活时间跟症状的持续时间有更强的相关性。HLAd在该试验中未发现抑制现象,反而有短暂的弱激活,类似于在一些非住院轻症患者中发现的特征。在疫苗接种之后,GBPs和ISGa的激活程度类似(图中下部),其激活的时间跨度也更短(4-6天),并且HLAd也有短暂的弱激活现象。另外,这三组基因的基线水平和激活程度能预示后续的接种效果。此外,在突破性感染(breakthrough infection)之后,ISGa和GBPs的激活程度在未接种的患者中要显著高于已接种的患者,显示出疫苗接种后干扰素信号通路的激活更温和一些。
本研究对治疗新冠病毒感染和类似疾病有一定的启示作用。在病毒感染之初激活HLAd可能有保护作用,在1-2周之后控制GBPs和ISGa的激活可能会避免后续的细胞因子风暴(cytokine storm)。另外,本研究对疫苗研发也有一定启示作用。监控这三组基因可以预判疫苗接种效果,并考虑是否需要寻求其它的保护措施。同时,上述观察到的现象可能指示肌肉疫苗接种和鼻腔疫苗接种会给人体带来不同的免疫反应,这是开发鼻腔疫苗需要考虑的问题之一。
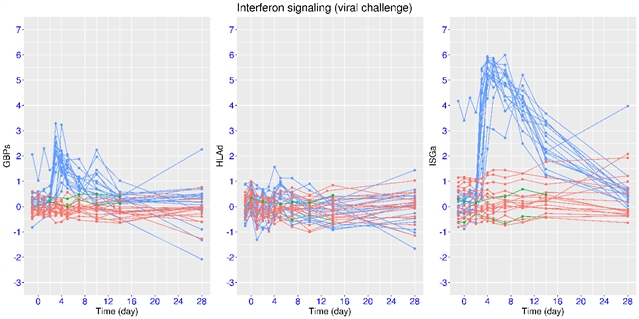
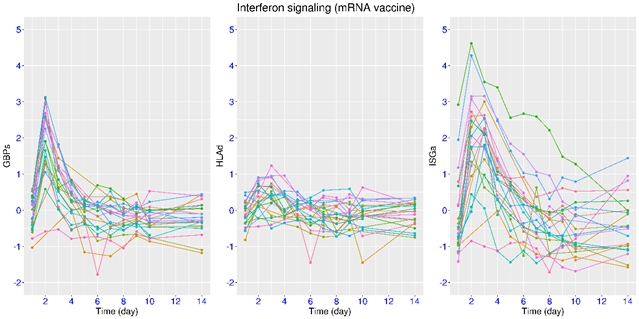
图一,干扰素信号通路在主动感染和疫苗接种初期的动态演化。A)主动感染。B)疫苗接种。
作者简介
雷红星研究员现任职于中国科学院北京基因组研究所(国家生物信息中心),并任中国科学院大学医学院岗位教授。雷红星研究员本科毕业于华中理工大学(现华中科技大学)生物医学工程专业,曾任职于军事医学科学院,后续在美国Kansas State University生物化学系取得计算生物学专业博士学位,并在University of Delaware和UC Davis从事博士后研究。本研究得到国家重点研发计划和中国科学院先导专项等基金的支持。
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。