|
|
|
|
|
多组学整合:开辟新疗法与生物标志物识别的新天地 | MDPI Proteomes |
|
|
论文标题:Multi-Omics Integration for the Design of Novel Therapies and the Identification of Novel Biomarkers
论文链接:https://www.mdpi.com/2227-7382/11/4/34
期刊名:Proteomes
期刊主页:https://www.mdpi.com/journal/proteomes
一、研究背景:为什么需要多组学整合?
现代生物医学研究中,单一组学数据虽然提供了宝贵信息,但常常无法全面描绘复杂的生物系统及其运行规律。不同分子层次之间存在错综复杂的相互作用——从基因到 RNA,再到蛋白、代谢物以及表观遗传修饰——单独观察任何一个层次都可能遗漏关键线索。
多组学整合(Multi-Omics Integration)正是在这一背景下应运而生。通过同时分析不同层面的生物数据,它可以提供系统性、全景式的视角,帮助科研人员识别疾病关键分子、发现潜在药物靶点,并为个性化治疗提供科学依据。
在癌症、神经系统疾病、免疫相关疾病等领域,多组学方法已显示出改变研究模式的潜力,为疾病机制解析、药物发现以及疗效预测带来了前所未有的机会。
二、多组学整合的方法
根据数据的类型、质量和可用性,以及生物学问题和假设,整合多组学数据用于药物发现的方法和策略各不相同。
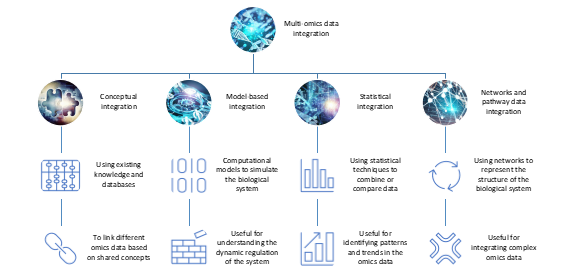
图 1. 整合不同组学数据用于药物研发。
下面是几类主流的数据整合策略,每种方法各有特点,适用于不同类型的研究问题:
1.概念整合(Conceptual Integration)
利用现有数据库和知识库(如基因本体 GO、通路数据库),将不同组学数据按共享概念或实体进行关联。
应用示例:STATegra 和 OmicsON,可检测不同组学数据之间的重叠特征,辅助生成研究假设。
2.统计整合(Statistical Integration)
通过相关性分析、回归建模、聚类或分类,将不同组学数据中的模式和趋势提取出来。
应用示例:识别基因与蛋白质在不同条件下的共表达关系,为药物响应预测提供依据。
3.模型化整合(Model-Based Integration)
利用网络模型或药物动力学/药效学模型(PK/PD)模拟生物系统行为。
优势:可理解系统动态调控机制,但需要对参数和系统结构有较多先验知识。
4.网络与通路整合(Networks & Pathways Integration)
构建蛋白-蛋白相互作用网络(PPI)或代谢通路,将多组学数据在不同层级进行整合。
优势:可同时处理多种组学数据,揭示分子间复杂的交互网络。
三、多组学分析的核心目标
多组学的主要应用之一是识别和验证各种疾病的新药物靶点。药物靶点可以是参与疾病发生或发展的蛋白质、基因、代谢物或表观遗传标记。
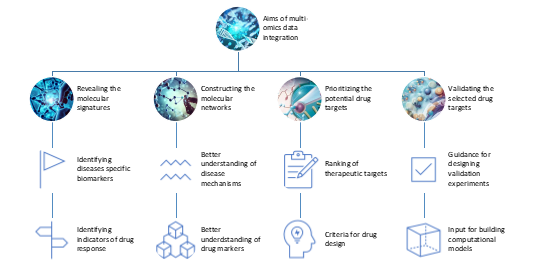
图 2. 整合不同组学数据用于药物研发的目的。
多组学可通过以下方式帮助发现和验证药物靶点:
1.新药靶点和生物标志物发现
•通过整合基因、蛋白、代谢物及表观遗传信息,识别疾病相关关键分子。
•构建疾病及药物作用机制网络,优先筛选潜在靶点,并通过实验或计算模型验证其可行性。
2.药物反应预测与优化
•分析个体间药物反应差异,识别影响疗效和毒副作用的遗传、转录、蛋白及代谢因素。
•利用机器学习模型(如随机森林、SVM、神经网络)预测个体化疗效及安全剂量,推动精准医疗发展。
四、典型应用案例
1.神经疾病
•利用多组学分析自闭症谱系障碍(ASD)和帕金森病脑组织,解析风险基因功能,发现潜在治疗靶点。
2.微生物组研究
•整合宿主组织与微生物组数据,揭示微生物如何影响宿主代谢、免疫及行为。
3.癌症研究
•通过肿瘤浸润免疫细胞的多组学数据,开发深度学习模型预测乳腺癌患者的生存率和药物反应。
•对脑膜瘤样本进行多组学分析,解析 TRAF7 和 KLF4 基因在肿瘤发生中的作用。
五、可用于多组学分析的不同类型的蛋白质组学数据
蛋白质组学是多组学研究中不可或缺的层次。文章重点介绍了几类关键蛋白组学数据:
•蛋白质组(Proteome):指蛋白质的鉴定、表达水平和修饰。
•磷酸化蛋白质组(Phosphoproteome):关注蛋白的磷酸化修饰,是细胞信号传导的重要调控层面。
•泛素化组(Ubiquitinome):研究蛋白泛素化,涉及蛋白降解、细胞周期及DNA修复等核心过程。
•糖蛋白组(Glycoproteome):分析糖基化修饰,影响癌症进展、免疫识别及药物靶向。
•乙酰化组(Acetylome):通过分析蛋白乙酰化,揭示代谢、信号和蛋白稳定性调控机制。
这些数据与基因组、转录组及代谢组结合,可提供疾病机制及药物作用的全景式理解。
六、面临的挑战与未来展望
多组学在药物研发中的应用是一个非常令人兴奋且前景广阔的领域,然而也面临着诸多挑战,需要逐步完善:
•数据复杂性:来自基因、RNA、蛋白质和代谢物的数据层次多、类型复杂,整合与分析难度大。
•工具与方法:现有分析工具透明性和可审计性有限,需开发更可靠的计算方法和验证手段。
•数据质量与标准化:测量方法存在变异与不完整性,数据格式和标准不统一,可能影响分析结果的准确性。
•伦理与隐私:多组学数据涉及个人敏感信息,需要严格保护隐私并获得知情同意。
•公平共享:不同科研机构或利益相关者在获取和使用数据上存在不平衡,亟需建立合理的数据共享政策和激励机制。
七、结语
多组学整合不仅为疾病机制解析提供了新视角,也为新药研发和个性化疗法设计开辟了新的通道。通过解析蛋白组复杂性,科研人员能够更深入理解疾病发生机制并优化治疗策略。尽管在数据标准化、算法可解释性和伦理隐私等方面仍存在挑战,但多组学整合无疑是未来精准医疗和药物发现的重要方向。
Proteomes 期刊介绍
主编:Jens R. Coorssen, Brock University, Canada; Matthew P. Padula, The University of Technology Sydney, Australia
期刊专注于蛋白质组分析的各个方面,特别关注蛋白质组在蛋白质形式(proteoforms)和典型氨基酸序列的功能生物单元水平上的定量和表征。目前已被Scopus、ESCI (Web of Science)、PubMed等数据库收录。
2024 Impact Factor: 3.6
2024 CiteScore: 7.2
Time to First Decision: 28.2 Days
Acceptance to Publication: 4.8 Days
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。