|
|
|
|
|
纽约州立大学Christopher Hellen教授团队——禽类杯状病毒基因组中2型IRES促进的重叠开放阅读框架的翻译 | MDPI Viruses |
|
|
论文标题:Translation of Overlapping Open Reading Frames Promoted by Type 2 IRESs in Avian Calicivirus Genomes
论文链接:https://doi.org/10.3390/v16091413
期刊名:Viruses
期刊主页:https://www.mdpi.com/journal/viruses
研究背景
病毒能进化出各种策略,利用细胞翻译装置来合成病毒蛋白,利用翻译装置的能力最大限度地利用病毒mRNA的编码能力,并在感染期间抑制细胞mRNA的翻译,尤其是那些作为先天免疫反应一部分而诱导的mRNA的翻译。。禽杯状病毒通过一项巧妙的分子策略,在有限的基因组空间里实现了蛋白质生产的最大化——近日,纽约州立大学Christopher Hellen教授团队于Viruses 发表了相关研究性文章。该研究揭示了这类病毒利用Ⅱ型内部核糖体进入位点 (IRES) 驱动重叠开放阅读框 (ORF) 翻译的独特机制 (图1),为理解病毒基因组的高效利用提供了新视角。
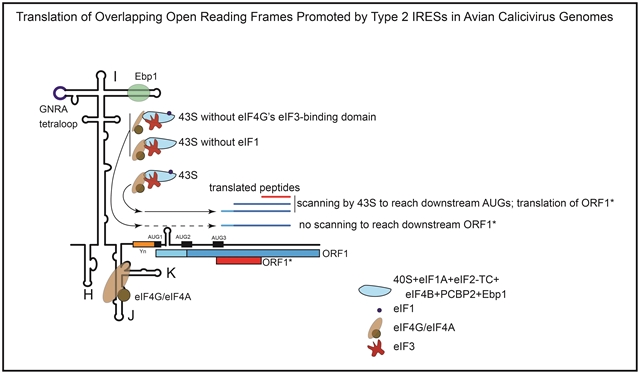
图1. 2型IRES驱动禽杯状病毒基因组中重叠开放阅读框的翻译机制。
研究发现
1.重叠ORF的发现
杯状病毒通常拥有正链RNA基因组,其5非翻译区 (5UTR) 较短,紧接长开放阅读框ORF1。研究发现,在禽杯状病毒中部分病毒的5UTR异常延长,其中嵌入了类似小核糖核酸病毒的IRES元件,而这些基因组中竟暗藏着一个长度约200-300个密码子的重叠ORF (命名为ORF1*),与ORF1的5端区域重叠。
通过分析灰水鸭杯状病毒 (GTCV) 和红冠鹤杯状病毒 (RaCV1) 等代表性病毒,研究团队证实:这些Ⅱ型IRES不仅能驱动ORF1的翻译,还能通过核糖体在mRNA上的跳跃和扫描,启动ORF1*的独立翻译。这样的模式,让病毒仅用一段基因组序列就能合成两种功能蛋白,堪称基因表达的效率典范。
2.从核糖体招募到翻译调控
Ⅱ型IRES作为病毒基因组中的分子机器,其核心功能在于招募核糖体并启动翻译。研究发现,GTCV和RaCV1的IRES通过保守结构域 (如GNRA四环、C-rich环)与真核起始因子eIF4G、eIF4A结合,形成核糖体起始复合物。有趣的是,IRES的3边界区域成为关键枢纽——核糖体不仅能从ORF1的起始密码子启动翻译,还能在ORF1*的起始位点组装,甚至识别ORF1内部的AUG密码子。
值得注意的是,这种翻译灵活性依赖于特定的辅助因子:Ebp1和PTB (或PCBP2)通过结合IRES的顶端结构域,增强核糖体与mRNA的结合效率。而eIF1和eIF1A则通过调控扫描过程,帮助核糖体跨越mRNA二级结构,选择最优起始位点。
3. IRES的水平转移证据
禽杯状病毒的IRES不依赖PABP,不依赖eIF4G-eIF3互作,受4E-BP去磷酸化激活,但VPg-eIF4E依赖的翻译被4E-BP抑制。这些特性提示IRES的获得(可能通过水平基因转移)使病毒在胁迫条件下维持翻译优势。序列比对显示,其IRES与小核糖核酸病毒的Ⅱ型IRES具有高度同源性,尤其是保守功能基序的保留,暗示了跨病毒家族的遗传物质交换。
这样的分子机制带来了显著的生存优势:在宿主细胞翻译系统受损时 (如感染引发的应激反应),依赖帽子结构的宿主mRNA翻译被抑制,而病毒通过IRES驱动的非帽依赖翻译,仍能持续生产蛋白。重叠ORF的存在进一步确保了病毒在有限基因组容量下的功能多样性,可能与其致病性和宿主适应性密切相关。
4. ORF1*的功能猜想
尽管揭示了翻译机制,ORF1*的具体功能仍是待解之谜。序列分析显示,其编码的蛋白缺乏已知功能结构域,推测可能通过与宿主或病毒蛋白相互作用发挥功能。类似现象在其他病毒 (如鼠诺如病毒的ORF4)中也有报道,提示重叠ORF可能是病毒应对宿主免疫压力的普遍策略,例如通过干扰宿主RNA降解途径或调控细胞信号通路促进感染。
结语:从基础研究到抗病毒启示
这项研究不仅拓展了我们对病毒基因组复杂性的认知,也为抗病毒药物开发提供了潜在靶点。例如,干扰IRES与宿主因子的相互作用 (如抑制Ebp1或PTB),可能阻断病毒的翻译程序;而针对重叠ORF的保守区域设计抑制剂,或许能实现对病毒的双重打击。
Viruses 期刊介绍
主编:Eric O. Freed, Center for Cancer Research, National Cancer Institute, USA
涵盖人类病毒和病毒疾病,动物病毒,植物病毒,病毒免疫、疫苗和抗病毒药物以及朊病毒等各方面研究,目前已被 SCIE (Web of Science)、MEDLINE (PubMed) 等数据库收录。
|
2024 Impact Factor
|
3.5
|
|
2024 CiteScore
|
7.7
|
|
Time to First Decision
|
17.1 Days
|
|
Acceptance to Publication
|
2.7 Days
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。