|
|
|
|
|
西尼罗河病毒和乌苏图病毒在欧洲的传播: 概述与挑战 | MDPI Viruses |
|
|
论文标题:Circulation of West Nile Virus and Usutu Virus in Europe: Overview and Challenges
论文链接:https://doi.org/10.3390/v16040599
期刊名:Viruses
期刊主页:https://www.mdpi.com/journal/viruses
研究背景
西尼罗河病毒 (West Nile Virus, WNV) 和乌苏图病毒 (Usutu Virus, USUV) 都是黄病毒科的嗜神经性蚊媒病毒,主要通过蚊媒传播,鸟类为主要扩增宿主,但人类和其他哺乳动物也可通过蚊虫叮咬感染。近年来,由于气候变化等因素,这两种病毒在欧洲传播的分布范围有所扩大,导致人类感染机会增多。虽然它们具有相似的生物学特性、生态学和流行病学特征,但其致病性以及对人类和动物健康的影响存在显著差异。西尼罗河病毒的研究更为广泛,且在许多地区已成为重大公共卫生问题。USUV因在欧洲出现感染及其循环系谱的多样性,最近也越来越受到关注。因此了解这两种病毒的病理生理学、生态学和传播动力学对于实施有效的监测和控制措施至关重要。本文章发表在Viruses 期刊,简要概述了这两种病毒在欧洲的现状,以及未来几年需要应对的重大挑战。
综述内容
近几十年来,全球新发蚊媒病毒的数量大幅增加。某些蚊媒病毒的地理分布范围特别扩大,导致人类疫情爆发次数增加,从而对人类健康构成了新威胁。其中,西尼罗河病毒和乌苏图病毒是两种密切相关的嗜神经性蚊媒病毒,都是有包膜的单链RNA病毒,属于黄病毒科正黄病毒属的日本脑炎病毒血清复合体。WNV于1937年首次从乌干达西尼罗河地区的一名妇女体内分离出来,而乌苏图病毒则于1959年在斯威士兰从野外捕获的尼氏库蚊体内首次发现。这两种病毒在嗜鸟蚊中以相似的传播周期维持,留鸟或候鸟则作为扩增宿主。
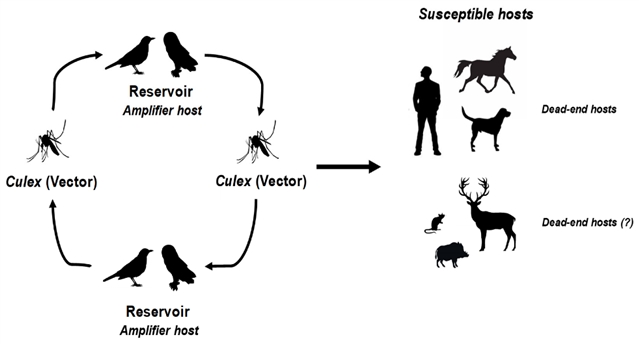
图1 WNV与USUV的传播周期
近年来,两种病毒在欧洲多地呈地方性流行,并逐步向欧洲北部扩张。尽管两者在生物学特性、生态学及传播模式上存在显著重叠,但其对人类与动物健康的影响及防控挑战各有不同,且共循环现象进一步加剧复杂性。
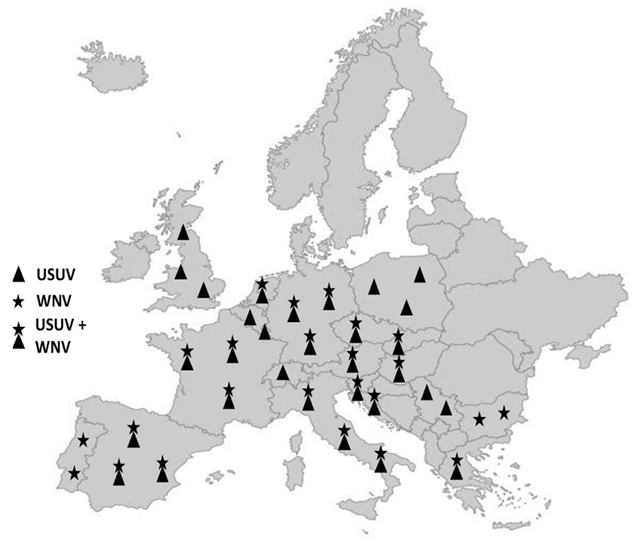
图2 欧洲WNV和USUV的分布情况
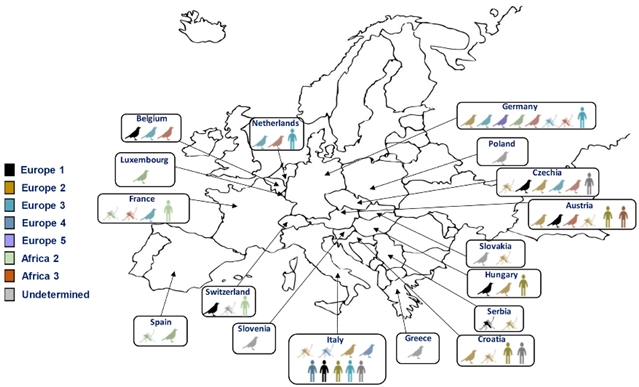
图3 欧洲不同谱系的USUV在人类、蚊子和鸟类中的分布情况
诊断工具:主要依赖血液或脑脊液 (CHF) 中特异性抗体或病毒基因的检测,尿液样本的分子检测可能后期扩大检测范围。但受限于检测时效,血清学方法 (如ELISA) 仍是主要手段。两种病毒因抗原结构相似存在交叉反应,需通过中和试验 (如PRNT) 进一步区分。诊断能力的不足导致误诊,尤其在缺乏标准化检测的欧洲地区,亟需开发特异性更高的检测方法,并加强病毒谱系监测以评估潜在致病性差异。
血液和器官安全:WNV因短暂病毒血症仍可通过极低病毒浓度的血液传播,欧洲一些WNV流行国家对血液与器官捐献者进行WNV感染检测,且采取季节性预防措施。欧盟仅报告过一例输血传播案例,表明现有措施有效。然而,WNV扩散导致高暴露地区血液管理压力增大。USUV在献血者中发现感染,尚无输血传播报道。然而,WNV流行国家不强制筛查病毒RNA,可能导致WNV检测结果混淆USUV感染。两种病毒共流行及未知的临床风险要求更新血液安全法规,并推动更精准的筛查策略。
治疗和疫苗:在人上,两种病毒目前尚无针对性特效药,仅可支持性对症治疗。马用WNV疫苗接种率低,人用WNV疫苗未完成III期临床试验;USUV疫苗仍处实验阶段。研究显示,WNV与USUV存在交叉免疫可能,但抗体依赖增强 (ADE) 风险仍需评估。
防控:WNV与USUV的时空共存显著增加监测防控难度,致病性及健康危害差异需依托区域性监测网络深入研究。强化监测体系与诊断能力是精准防控的关键,需基于“One Health”原则整合蚊媒、鸟类、兽医及人类监测数据。
总体而言,WNV与USUV的共循环既是生态学现象,亦是公共卫生挑战。二者在共享宿主与媒介中的竞争可能重塑传播格局。未来防控需四维突破:一是革新诊断技术;二是动态优化血液安全政策;三是加速广谱黄病毒疫苗研发;四是深化“One Health”网络,通过跨国协作共享病毒基因组数据与生态监测结果。唯有融合分子生物学、流行病学及生态学视角,方能破解这两种病毒在气候变化与全球化背景下的传播密码,为虫媒蚊媒病毒防控提供新范式。
作者介绍
Yannick Simonin是博士蒙彼利埃大学病毒学教授。研究领域为emerging viruses。the INSERM CSS5 and CNU 65 Committees委员。负责“感染生物学”硕士课程和微生物学学士课程。
Viruses 期刊介绍
主编:Eric O. Freed, Center for Cancer Research, National Cancer Institute, USA
涵盖人类病毒和病毒疾病,动物病毒,植物病毒,病毒免疫、疫苗和抗病毒药物以及朊病毒等各方面研究,目前已被 SCIE (Web of Science)、MEDLINE (PubMed) 等数据库收录。
|
2024 Impact Factor
|
3.5
|
|
2024 CiteScore
|
7.7
|
|
Time to First Decision
|
17.1 Days
|
|
Acceptance to Publication
|
2.7 Days
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。