导读
随着精准医学的飞速发展,细胞检测技术已成为疾病早期诊断、个性化医疗、病情监测及疗效评估的重要工具。其中,成像流式细胞检测以“快而准”的特性备受关注,尤其在面对海量细胞样本时,展现出巨大的应用潜力。然而,传统成像流式细胞仪(IFC)通常使用CCD/CMOS图像传感器,吞吐量仅为每秒1,000个细胞,无法满足现代精准医疗对高通量检测的需求。光流控时域拉伸成像流式细胞仪(OTS-IFC)理论上能实现每秒百万级细胞检测,是目前最具潜力的解决方案之一,但其带来的海量数据在实时传输和处理上提出了严峻挑战,成为技术进一步发展的主要瓶颈。
为突破这一技术瓶颈,实现“更快更准”的细胞分析,武汉大学刘胜院士、雷诚教授、王度教授团队与华中科技大学王亮教授团队联合攻关,通过协同设计光学时域拉伸成像系统、三维聚焦微流控芯片及在线数据采集与处理系统,并结合高性能图像分析算法,成功研发出新一代智能光流控时域拉伸成像流式细胞仪。该系统的实时检测通量突破性地达到每秒超过1,000,000个细胞,创下了目前世界上实时细胞检测通量的新纪录。相比现有高通量技术,该系统性能提升了2~3个数量级,同时实现了780 nm的高空间分辨率。在此基础上,研究团队首次在高通量条件下实现了稀有事件的精准识别,并成功应用于临床癌症检测任务,展现出广阔的应用前景。
近日,该研究以“Imaging flow cytometry with a real-time throughput beyond 1,000,000 events per second”为题,发表Light: Science & Applications。武汉大学博士生周杰华和湖北工业大学青年教师梅礼晔为论文共同第一作者,武汉大学雷诚教授、王度教授,华中科技大学王亮教授为该论文的共同通讯作者。
研究背景
成像流式细胞仪(IFC)近年来已成为生物学、微生物学、药理学、血液学和免疫学等领域的核心工具,革新了细胞分析的方法。它能够快速、准确地捕捉大量细胞图像,提供详细的形态学数据,并以高统计可靠性分析复杂的细胞群体。然而,传统的成像流式细胞仪通常使用CCD或CMOS图像传感器,由于其曝光时间长、像素读出速度慢,检测吞吐量仅为每秒1000个事件(eps),难以满足大规模细胞检测的实际需求,限制了其在精准医疗中的应用。
人体中细胞数量庞大,例如成年男性体内约有36万亿个细胞,成年女性体约28万亿个细胞。以血液样品为例,每毫升的血液大约含有5.4亿个血细胞,使用传统的IFC对一毫升的血液样品进行全面分析需要150小时,这远远无法满足当今精准医疗对于高通量细胞分析的需求。
光学时域拉伸成像(OTS)技术是最有潜力实现高通量成像流式细胞检测的技术之一。凭借其超短的脉冲时间,OTS能够对流速高达几十米的细胞进行逐行扫描式成像,实现高精度、无运动模糊的检测。与传统显微成像技术不同,OTS采用高速光电探测器采集信号,从而突破了成像速度的瓶颈。结合微流控技术,研究人员提出了光流控时域拉伸成像流式细胞仪(OTS-IFC),其理论检测吞吐量可达每秒百万级细胞,展现了在精准医疗和细胞分析中的巨大应用潜力。然而,OTS-IFC高通量检测能力所带来的海量数据对系统的实时传输与处理提出了严峻挑战,大数据问题成为制约技术进一步发展和实际应用的关键难题。
研究亮点
为了应对这一挑战,研究团队创新性地联合设计了光学时域拉伸成像系统、三维聚焦微流控芯片,并结合在线ADC和FPGA的数据采集与处理系统,通过高性能的在线图像识别、处理和分析算法,成功研发了新一代智能光流控时域拉伸成像流式细胞仪(如图1所示)。这一系统首次实现了每秒超过1,000,000个事件(eps)的实时检测通量,远超现有技术2~3个数量级。同时,其空间分辨率可达780 nm, 为成像流式细胞仪的实时性能设定了新的基准。
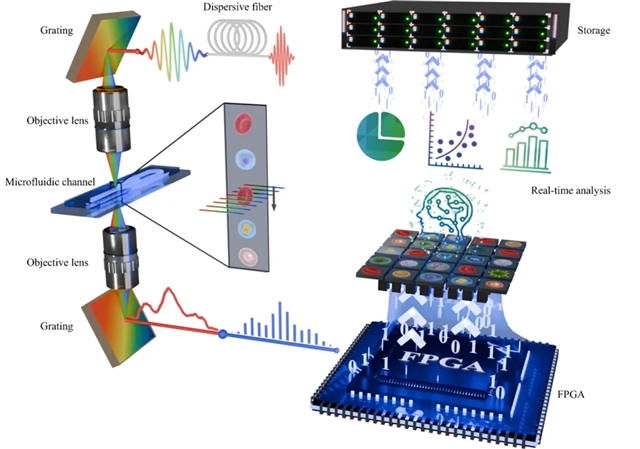
图1:光流控时域拉伸成像流式细胞仪
图2展示了OTS-IFC和传统IFC在流动细胞成像中的性能差异。传统IFC在对流速超过1 m/s的细胞进行成像时,由于高速运动导致显著的运动模糊,从而产生伪影,严重影响图像质量和后续分析的精度。而OTS-IFC凭借光学时域拉伸成像技术的优势,能够对流速高达15 m/s的细胞进行清晰成像,显著提升了对高速流动样本的检测能力。

图2:OTS-IFC与传统IFC成像质量对比
如图3(a)所示,研究团队通过在现场可编程逻辑门阵列(FPGA)上采用并行和流水线处理方式,部署了高效的事件识别、去冗余、图像重建及分析算法。其中,去冗余算法专为优化OTS成像信号的特点而设计,该算法可以将前端生成的原始数据流从20 GB/s成功压缩至5 GB/s以下。这一创新设计确保了系统在超高吞吐量(每秒超过100万个细胞)下,仍能通过PCI-E 3.0 x8接口实现数据的实时传输,从而满足高通量实时成像的需求。最终,利用如图3(b)所示的数据调度算法,在基于生产者与消费者的模型上,实现大流量数据的高效连续存储。
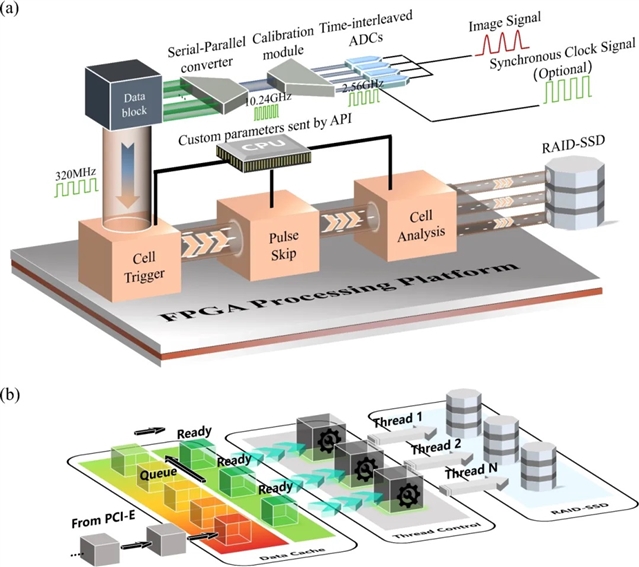
图3:信号实时处理和存储原理图
如图4(a)、(b)和(c)所示,通过多次测试稀释后的全血样品,系统成功实现了每秒1,000,000个事件(eps)的连续检测吞吐量,并能够精准触发每张单细胞图像并进行实时在线分析。通过将获取到的图像数量与样品浓度进行对比,系统可以实现几乎无损的检测。此外,系统还具备独特的高通量检测下稀有事件识别能力(稀有事件定义为占总事件比例低于0.01%的特殊情况),这一功能是现有其他系统无法实现的。如图4(d)所示,在单次的全血样品检测中,在没有任何标记的情况下,系统可以识别到如单核细胞、高流速高压力下裂解的细胞、聚集的细胞群、以及导致血栓形成的聚集血小板等现象。这一独特的功能为生物学研究和临床医学诊断提供了全新的可能性,拓宽了应用场景和研究领域的大门。

图4:系统的实时吞吐量和在线分析识别能力
最后,研究团队将该系统应用于实际临床场景,对10个结直肠临床样品进行检测,采集到共计1,281,496张细胞图像。针对临床样品的细胞复杂性和多样性,团队设计了一种多通道卷积神经网络(CNN),如图5(a)所示。该模型将单个癌细胞的识别任务转化为判断分组图像是否共同表现出肿瘤特征,从而实现对结直肠肿瘤组织与正常组织的无标签高精度分类。实验结果表明,该系统对肿瘤样品和正常组织样品的分类准确率高达100%。这一研究不仅进一步验证了系统的有效性,还表明其能够与现有的临床需求无缝衔接,为高通量、无标记的病理检测提供了一种创新性的解决方案,展现出广阔的应用前景。
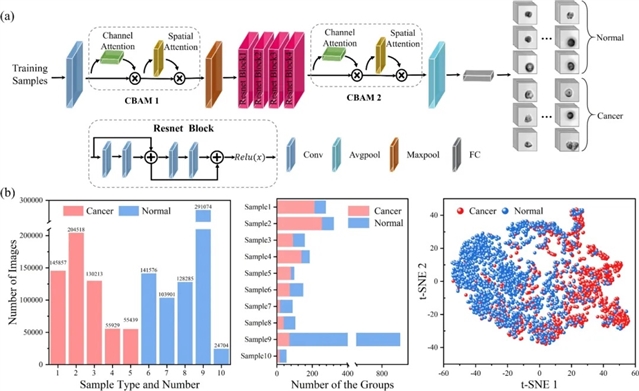
图5:系统利用卷积神经网络以无标签的形式对结直肠中的肿瘤和正常组织进行分类
总结与展望
在本研究中,研究团队协同设计了光学时域拉伸成像系统、三维聚焦微流控芯片及在线数据采集与处理系统,并结合高性能图像分析算法,成功研发出新型智能光流控时域拉伸成像流式细胞仪。该系统首次实现了每秒百万细胞的检测吞吐量,创下了全球成像流式检测的最高纪录,相比现有技术提高了2~3个数量级,将原本仅停留在理论层面的高性能指标转化为现实应用。这一技术突破不仅为成像流式检测领域带来了全新的视角和可能性,也为该技术的实际应用落地提供了坚实的技术基础。
在此基础上,研究团队首次在连续高通量检测条件下实现了稀有事件的精准识别,并成功应用于临床结直肠癌症检测任务,样品分类准确率高达100%,展现出广阔的应用潜力。未来,凭借系统卓越的数据获取能力和与大数据模型的深度融合,该系统有望在多种疾病的精准诊断与预测中发挥关键作用,助力疾病的早期发现与精准治疗。大规模临床应用的实现或将指日可待,为精准医疗的进一步发展注入新动力。(来源:中国光学微信公众号)
相关论文信息:https://doi.org/10.1038/s41377-025-01754-9
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。