在国家重点研发计划等项目资助下,中国科学院南海海洋研究所研究员王晓雪团队在融合型七型毒素-抗毒素(TA)系统的多重调控机制研究方面取得重要进展。相关成果近日发表于《核酸研究》(Nucleic Acids Research)。
毒素-抗毒素系统广泛存在于细菌等原核生物中,在微生物适应不同环境条件过程中发挥重要功能。七型TA系统由王晓雪团队于2020年首次报道,其核心特征在于抗毒素通过酶促反应对毒素进行翻译后修饰。
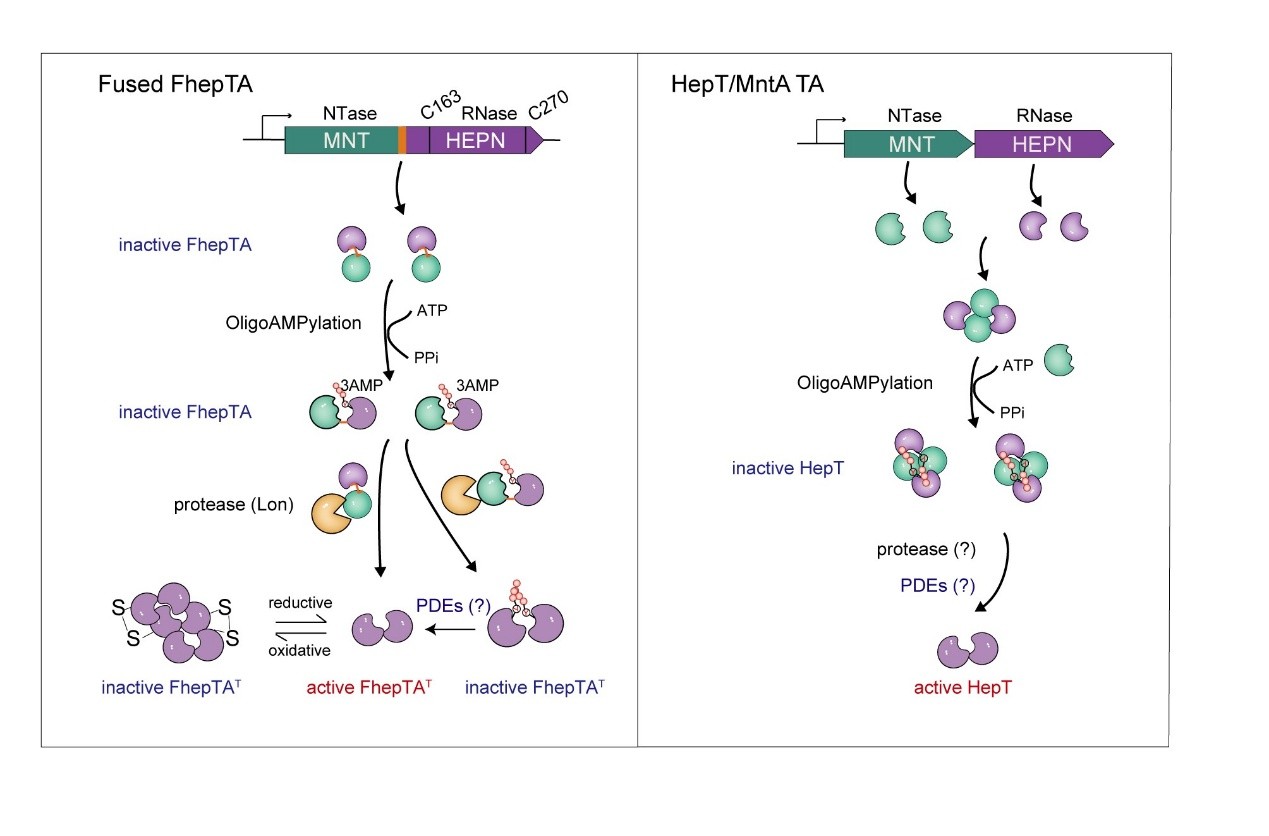 融合型FhepTA与经典HepT/MntA Ⅶ型TA系统中毒素活性调控模式图。研究团队供图
融合型FhepTA与经典HepT/MntA Ⅶ型TA系统中毒素活性调控模式图。研究团队供图
除经典的双顺反子结构外,原核生物基因组中还普遍存在一类特殊的融合型TA系统,其MNT抗毒素结构域与HEPN毒素结构域融合在同一条多肽链中。然而,融合型TA系统的调控机制一直是领域内未解的关键问题:在融合型系统中,MNT与HEPN以1:1的比例存在,系统如何实现对毒素的精确沉默,又如何在环境压力下快速释放毒素活性?
针对上述科学问题,研究团队以海洋希瓦氏菌为研究对象,综合利用生物信息学、生物化学与结构生物学等方法,首次鉴定出一类全新的融合型七型TA系统——FhepTA,并通过体内与体外实验解析了其毒素结构域的多重“沉默-激活”机制。研究表明,FhepTA通过三重精密调控实现毒素的智能开关功能:
第一重,MNT结构域利用ATP为底物,通过分子内自催化反应对HEPN结构域进行三腺苷酸化修饰,为毒素贴上“失活标签”;第二重,MNT结构域通过空间位阻效应直接阻断HEPN结构域的二聚化,从根本上抑制其RNase活性,这是比腺苷酸化修饰更基础、更核心的沉默机制;第三重,HEPN结构域利用其特有的半胱氨酸残基形成氧化还原敏感的二硫键,根据胞内氧化还原状态灵活调控毒素活性。FhepTA在正常生理条件下处于完全沉默状态;在低ATP的还原条件下,MNT结构域被Lon蛋白酶逐步降解,从而精准释放毒素HEPN的活性,实现对RNA水平的代谢调控。
毒素结构域HEPN是一种RNA内切酶(亦可水解真核生物RNA),其与抗毒素结构域之间的柔性连接区为其改造提供了可能。研究团队发现,将该连接区替换为真核病毒蛋白酶识别的序列后,将改造后的蛋白导入真核细胞,可实现毒素结构域在感染细胞中的定向激活,从而靶向清除感染细胞(相关成果已获专利授权)。此外,HEPN毒素结构域精密的调控模式也为其进一步开发为RNA分析及检测工具提供了新的理论基础。
相关论文信息:https://doi.org/10.1093/nar/gkag228
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。