复旦大学类脑智能科学与技术研究院青年研究员肖晓、特聘教授特雷弗·罗宾斯(Trevor Robbins)、教授冯建峰团队发现,海马齿状回在情绪转变中起到关键调控作用,就像一道“情绪闸门”缓和负面情绪,而当“闸门”失效时,兴奋–抑制平衡被打破,抑郁由此出现。3月20日,相关研究成果发表于《科学》。
世界卫生组织和多项流行病学研究显示,全球约20%–30%的成年人正在遭受不同形式的慢性疼痛,其致残率高、病程长,严重影响劳动能力、生活质量和社会参与,被形象地称为“不死的癌症”。在长期疼痛人群中,约一半以上会伴随不同程度的抑郁或焦虑症状。这种疼痛—情绪共病不仅加重患者的主观痛苦,也显著增加了医疗利用率、自杀风险和社会经济负担。理解慢性疼痛如何影响大脑情绪调控系统、以及为何这种影响在不同个体之间存在巨大差异,成为神经科学、医学和公共健康领域共同关注的核心问题。
为解答此问题,研究团队系统整合了大规模人群神经影像数据与啮齿动物慢性神经病理性疼痛模型,从脑结构、功能、神经环路及细胞机制多个层级,系统分析了慢性疼痛向抑郁、焦虑发展的过程。
研究结果显示,大脑中存在一个决定性的“情绪闸门”,而海马是这一“情绪闸门”的核心枢纽。具体而言,慢性疼痛并不会直接导致抑郁或焦虑,是否发展为情绪障碍,取决于大脑情绪调控系统能否维持稳定。在疼痛早期,海马体积短暂增大,功能状态增强;而疼痛持续并伴随抑郁后,海马逐渐萎缩,调控能力下降。这一“先适应、后失衡”的双相变化轨迹,在不同疼痛类型和人群中高度一致,也在动物模型中得到了验证。
机制研究表明,海马中的齿状回是“情绪闸门”的关键节点。在疼痛早期,齿状回内新生神经元及相关信号被激活,表现出对疼痛的适应性和可塑性。而在疼痛维持期,小胶质细胞被激活,进而导致神经环路兴奋-抑制平衡被打破,情绪调控逐渐失败,引发情感障碍症状。
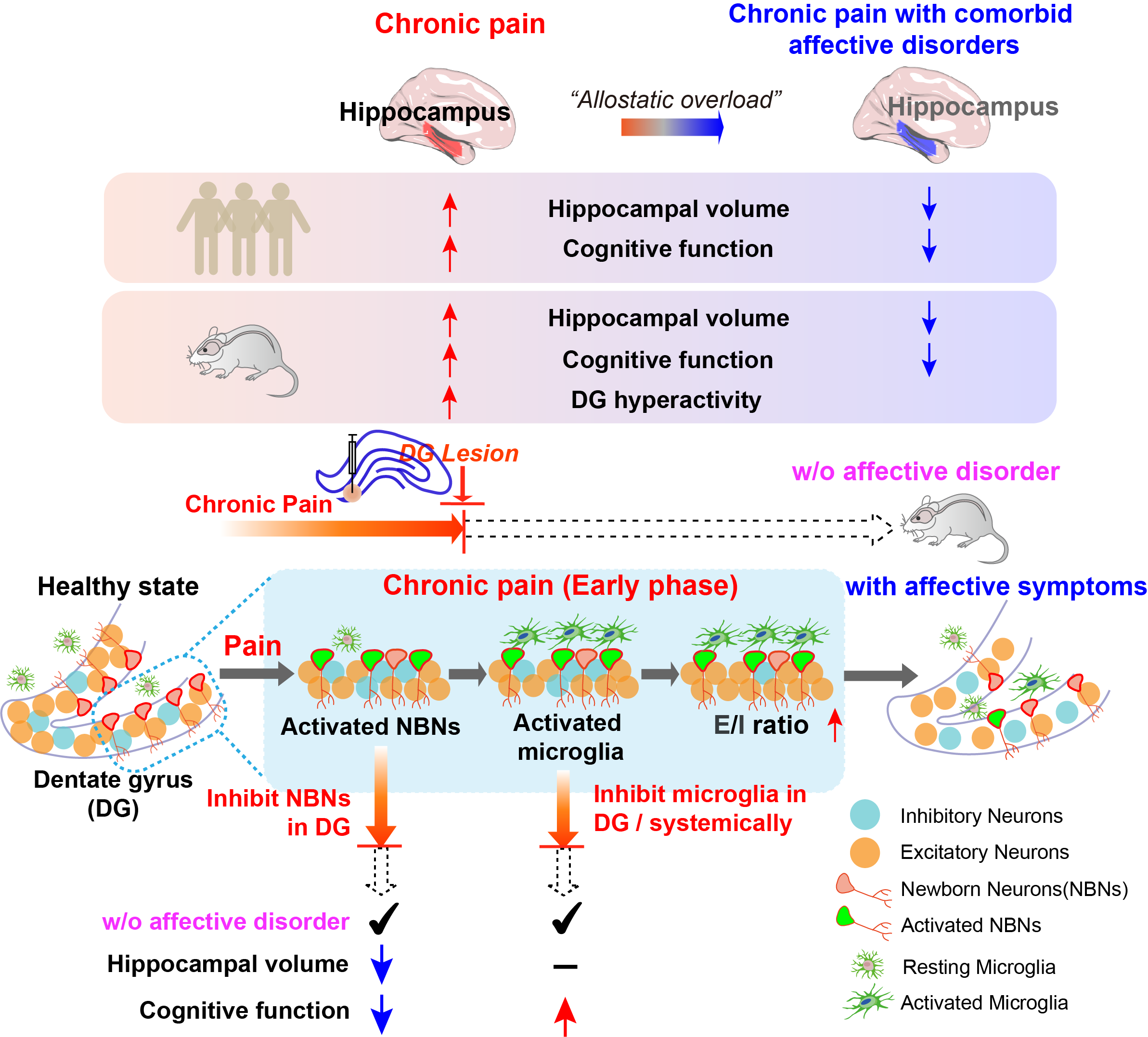 慢性痛早期海马齿状回变化的神经机制示意图。研究团队供图
慢性痛早期海马齿状回变化的神经机制示意图。研究团队供图
研究团队进一步比较了不同干预节点的效果。结果显示,调控小胶质细胞异常激活则可在缓解疼痛相关情绪问题的同时,更好地维持整体功能稳定性,表明小胶质细胞可能是阻断慢性疼痛向情绪障碍转变的更优靶点。
相关论文信息:http://doi.org/10.1126/science.aee6177
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。