|
|
|
|
|
VSV在具有抵抗病毒溶瘤作用的侵袭性PC3前列腺癌细胞中增强组成性NF-κB激活| MDPI Viruses |
|
|
期刊:Viruses
期刊主页:https://www.mdpi.com/journal/viruses
原文链接:https://www.mdpi.com/1999-4915/18/1/67
研究背景:
近年来,溶瘤病毒疗法在肿瘤治疗中展现出独特优势,其中水疱性口炎病毒(vesicular stomatitis virus, VSV)因其对多种癌症的显著抗肿瘤活性备受关注。
前列腺癌是男性常见的恶性肿瘤,晚期患者治疗选择有限,预后较差。临床前研究中,VSV显示出对前列腺癌的治疗潜力,但其抗肿瘤效果在不同细胞系中差异显著。研究表明,源自高度转移性前列腺癌的PC3细胞对VSV具有较强抵抗性,而来自淋巴结转移灶的LNCaP细胞则高度敏感。在许多侵袭性和转移性肿瘤中,转录因子NF-κB呈现组成性激活状态,这种激活参与调控细胞增殖、凋亡抵抗和抗病毒应答。
近日,罗彻斯特理工学院戈斯内尔生命科学学院 Maureen C. Ferran博士及其团队在 Viruses 期刊发表了研究性文章,探讨了NF-κB信号通路在前列腺癌细胞抵抗VSV溶瘤作用中的关键机制,为耐药前列腺癌中靶向NF-κB的治疗策略提供了新见解。
研究结论:
通过对比PC3与LNCaP细胞在VSV感染过程中的反应,研究团队得出以下关键结论:
1.PC3细胞相比LNCaP细胞更能抵抗VSV溶瘤作用
通过细胞活力测定发现,无论感染野生型VSV还是M蛋白突变株(R1),PC3细胞的死亡率均低于LNCaP细胞(图1)。病毒滴度测定进一步证实,PC3细胞中VSV的复制效率远低于LNCaP细胞,表明病毒在PC3细胞中的生命周期受到限制(图2)。
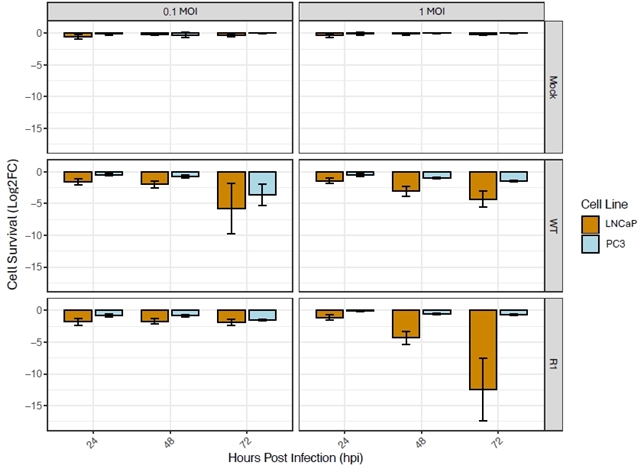
图1. PC3细胞比LNCaP细胞对VSV介导的溶解更有抵抗力。
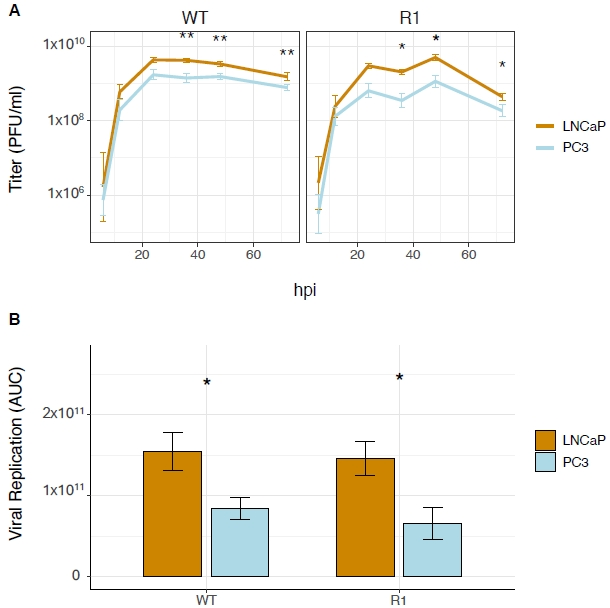
图2. 在相同的MOI下,LNCaP细胞比PC3细胞允许更多的病毒复制。(A)PC3和LNCaP细胞感染两种VSV毒株;(B)使用生长曲线的曲线下面积(AUC)进行直接比较。
2.NF-κB在PC3细胞中呈组成性激活状态
免疫荧光染色显示,在未感染状态下,PC3细胞中NF-κB 已明显向细胞核内转移,而LNCaP细胞中NF-κB 主要滞留于胞浆,且在TNF-α处理或VSV感染的PC3细胞中NF-κB 的核定位都明显高于LNCaP细胞(图3)。进一步检测NF-κB上游调控分子IκB-α发现,PC3细胞中总IκB-α及其磷酸化水平均显著高于LNCaP细胞,提示IκB-α的持续磷酸化导致其降解加速,从而释放NF-κB 入核(图4)。基线时,PC3细胞中的NF-κB 亚基p65总水平高于LNCaP细胞,此外,与VSV感染的LNCaP细胞相比,PC3细胞中的磷酸化p65水平更高(图5)。这些实验表明在PC3细胞中观察到的组成性NF-κB 激活可能是由于IκB-α磷酸化增加和NF-κB p65亚基总表达增加的结果。
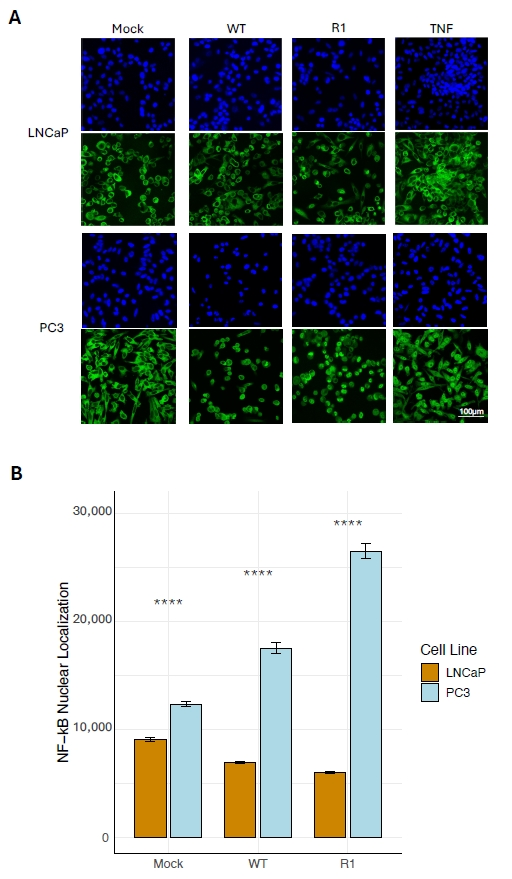
图3. PC3细胞表现出比LNCaP细胞更高的基线和VSV诱导的NF-κB 核定位水平。(A)PC3和LNCaP细胞中NF-κB 定位的免疫荧光(共焦显微镜)图像;(B)通过Image J中自动计数修正总细胞荧光(CTCF)来量化NF-κB 核定位。
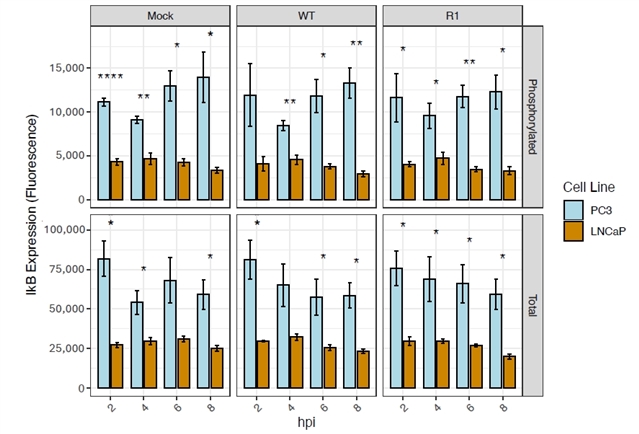
图4. PC3细胞中NF-κB 抑制剂IκB-α的总水平和磷酸化水平高于LNCaP细胞。
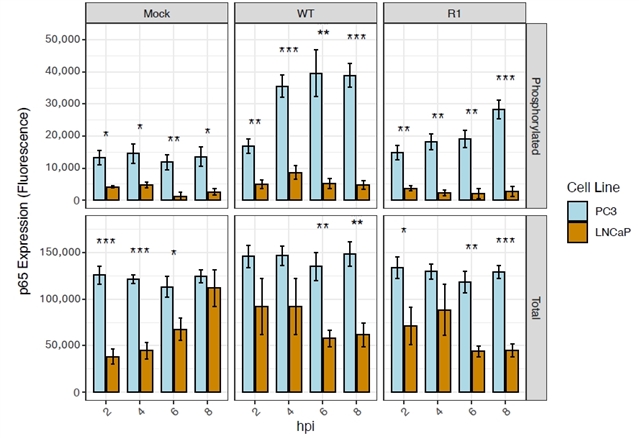
图5. PC3细胞中NF-κB 亚基p65的总水平和磷酸化水平高于LNCaP细胞。
3.VSV感染进一步增强PC3细胞中NF-κB信号通路
在感染VSV后,与LNCaP细胞相比,PC3细胞中所有测试的抗病毒/促炎基因(细胞因子IL 6、IL 12、IL 15、TNF-α、IFN-β和趋化因子CXCL 8)的表达水平都高得多。这表明VSV感染可进一步放大PC3细胞中已活化的NF-κB信号,强化其抗病毒状态(图6)。
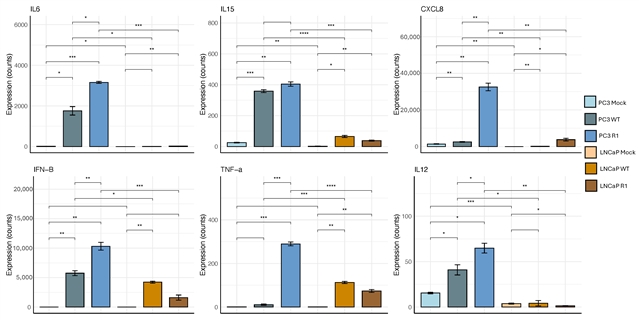
图6. 与LNCaP细胞相比,PC3细胞在响应VSV感染时表达更高水平的代表性抗病毒基因。
4.抑制NF-κB可恢复PC3细胞对VSV的敏感性
为验证NF-κB激活与VSV抵抗的直接因果关系,研究团队使用NF-κB特异性抑制剂Bay11-7082处理PC3细胞。单独使用抑制剂或单独感染VSV均未显著影响PC3细胞存活,但两者联合处理后,样本在所有测试时间点均表现出细胞死亡显著增加,表明协同作用。这一结果证实,阻断NF-κB通路能够有效逆转PC3细胞对VSV的抵抗性,使其恢复对溶瘤病毒的敏感性(图7)。
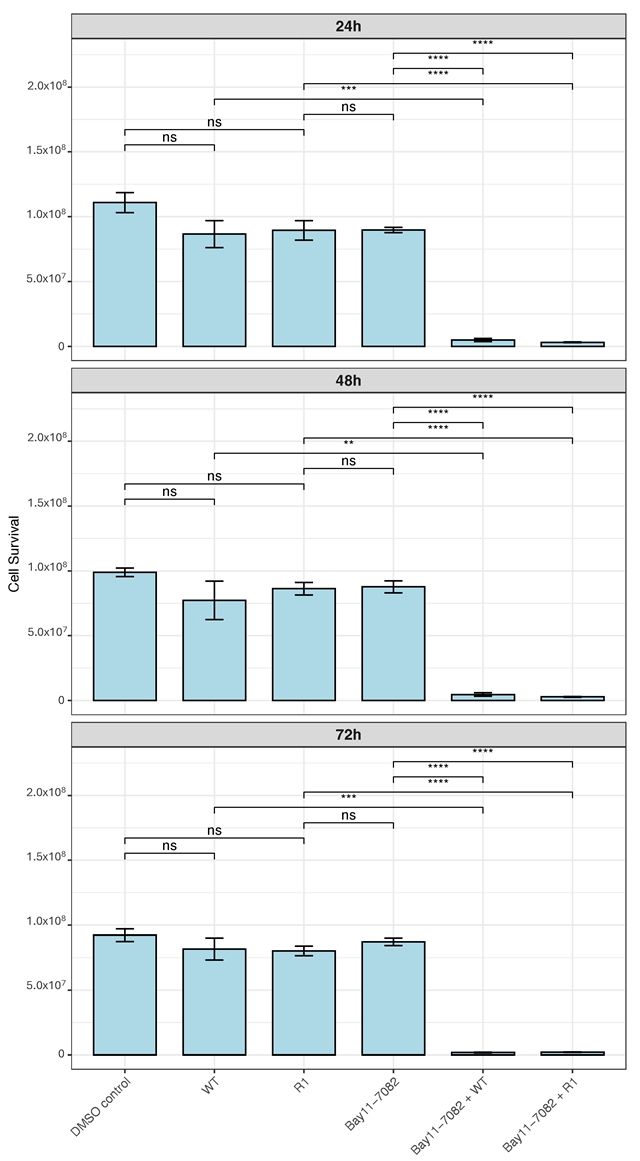
图7. NF-kB抑制可恢复耐药PC3细胞对VSV的敏感性。
研究总结:
本研究系统阐明了NF-κB 信号通路在介导前列腺癌细胞抵抗VSV溶瘤病毒中的作用机制。VSV感染PC3细胞能够导致IκB-α磷酸化增加和NF-κB p65亚基总表达增加,从而增强NF-κB组成性激活并促进下游抗病毒基因高表达,建立了一个不利于病毒复制与细胞裂解的微环境。使用NF-κB抑制剂Bay11-7082可显著逆转PC3细胞的抵抗表型,确证该通路的关键作用。这一发现不仅揭示了肿瘤细胞抵抗溶瘤病毒的潜在分子基础,也为开发联合治疗策略提供了新思路。
期刊简介:Viruses (IF 3.5, CiteScore 7.7, https://www.mdpi.com/journal/viruses) 创刊于2009年,专注于病毒学领域研究。目前被SCIE (Web of Science)、PubMed、Scopus、MEDLINE等重要数据库收录。2024 年其影响因子为 3.5 (JCR 分区病毒学位于Q2),CiteScore 7.7,分区位于病毒学 / 传染病学 Q1)。西班牙病毒学会、意大利病毒学会、加拿大病毒学会等,均与Viruses达成合作,会员享受文章处理折扣。
期刊涵盖领域:Viruses是一本专注于病毒相关研究的开放获取期刊,涵盖诸多关键领域,病毒感染、病毒分类、病毒病原体、类病毒、病毒免疫和抗病毒治疗、噬菌体、病毒结构与基因组、病毒演化和病毒感染动态研究,为国际病毒学研究提供了一个前沿平台。发表原创性研究论文、综述、通讯、会议报告及简讯等。
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。