|
|
|
|
|
免疫衰老与老年综合征:揭示分子机制与健康寿命新洞察 | MDPI Medical Sciences |
|
|
论文标题:Immunosenescence and the Geriatric Giants: Molecular Insights into Aging and Healthspan
论文链接:https://www.mdpi.com/2076-3271/13/3/100
期刊名:Medical Sciences
期刊主页:https://www.mdpi.com/journal/medsci
衰老伴随一系列被称为“老年综合征”的复杂状况,包括虚弱、跌倒、肌少症、认知下降、活动受限及失禁等,这些问题常相互叠加并加重功能退化,其核心驱动力之一是免疫衰老(immunosenescence)。免疫衰老表现为胸腺退化、初始T细胞减少、T细胞耗竭、B细胞类转换受损及自身反应性增加;同时,巨噬细胞、中性粒细胞和NK细胞等先天免疫功能下降,慢性低度炎症(inflammaging)持续加剧系统损伤。NF-κB、mTOR、NLRP3炎症小体等关键通路与氧化应激、线粒体功能障碍及表观遗传变化共同推动免疫功能下降,不仅削弱抗感染和疫苗反应能力,也促进组织退化与多病共存。当前研究聚焦于清除衰老细胞的药物、免疫营养、运动及微生物组干预等策略,以恢复免疫稳态并延长健康寿命。然而,将免疫学机制转化为适用于老年人的临床策略仍具挑战,尤其是微生物组试验标准化及衰老细胞清除疗法的安全性仍需进一步优化。来自印度尼西亚艾尔朗加大学Deasy Fetarayani博士及其团队在Medical Sciences期刊发表了文章,介绍了免疫衰老通过削弱适应性与先天免疫并持续推动全身炎症,成为虚弱、肌少症和认知下降等老年综合征的核心机制,并为延长健康寿命的干预研究提供重要方向。。
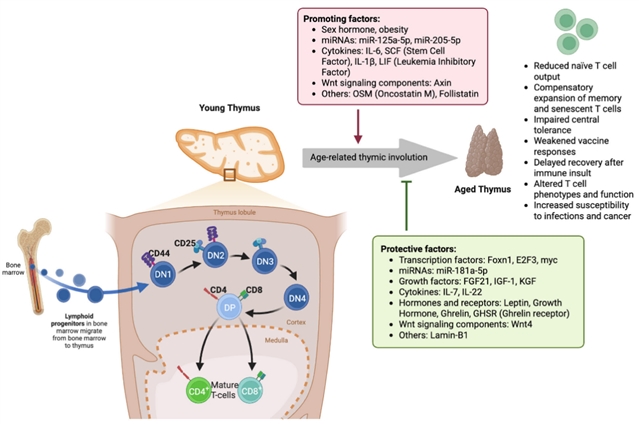
与年龄相关的胸腺退化及其对 T 细胞发育的影响所涉及的分子和细胞机制。在年轻的胸腺中,来自骨髓的淋巴细胞前体细胞进入胸腺皮质,并经历一系列不同的胸腺细胞成熟阶段:双阴性(DN1–DN4)、双阳性(DP),最终发育成为髓质中的成熟 CD4+ 和 CD8+ T 细胞。保护性因子,如转录因子(Foxn1、E2F3、myc)、miR-181a-5p、生长因子(FGF21、IGF-1、KGF)、细胞因子(IL-7、IL-22)和激素(如瘦素、生长激素、胃饥饿素),以及 Wnt4 信号通路和 Lamin-B1,维持着胸腺的结构和功能。相比之下,与年龄相关的胸腺退化是由促进因素驱动的,如性激素、肥胖、miR-125a-5p、miR-205-5p、炎症性细胞因子(IL-6、SCF、IL-1β、LIF)、Wnt 信号通路组件 Axin 以及其他分子,包括 OSM 和 Follistatin。胸腺退化会导致初始 T 细胞输出减少、记忆/衰老 T 细胞的扩增、中央耐受受损、疫苗反应减弱、损伤后 T 细胞恢复延迟、T 细胞表型改变以及感染和癌症易感性的增加。(DN:双阴性胸腺细胞(CD4−CD8−);DP:双阳性胸腺细胞(CD4+CD8+);CD:细胞分化簇;FGF21:成纤维细胞生长因子 21;IGF-1:胰岛素样生长因子 1;KGF:角质形成细胞生长因子;IL:白细胞介素;SCF:干细胞因子;LIF:白血病抑制因子;OSM:癌因素 M;Foxn1:叉头框 N1;E2F3:E2F 转录因子 3;myc:原癌基因 c-Myc;GHSR:胃饥饿素受体;Wnt:无翅/整合信号通路)
研究过程与结果
免疫衰老是老年人虚弱、肌少症、认知下降、跌倒及失禁等“老年综合征”的核心驱动力。适应性免疫首先受到影响,胸腺萎缩导致初始T细胞生成锐减,外周记忆与衰竭T细胞占比增加,自身耐受性下降并提高感染与肿瘤风险。随着年龄增长,T细胞因反复抗原刺激而出现耗竭,表现为PD-1、CTLA-4 等抑制性受体上调、代谢受损及表观遗传重塑。B细胞也随之退化,E47 与 AID 下调导致抗体类别转换受阻,抗体亲和力下降,并因中枢和外周耐受缺陷而更易产生自身抗体,最终削弱疫苗应答。先天免疫同样发生明显退化。老年巨噬细胞因线粒体损伤、代谢重编程与表观遗传异常而吞噬能力下降、趋化受损并偏向炎症性M1表型;中性粒细胞出现迁移力下降、吞噬不足及氧化爆发降低;NK细胞因IL-15信号衰减、功能成熟亚群减少和抑制性受体上调而杀伤力下降。上述变化共同促进慢性低度炎症(inflammaging),由SASP、NLRP3炎症小体、NF-κB持续激活及肠道菌群失衡驱动,进而加速多系统老化。
免疫失衡直接参与老年综合征的发生。IL?6、TNF?α 诱导肌蛋白降解、抑制再生,引发肌少症与虚弱;神经炎症与小胶质细胞过度激活推动认知退化;免疫修复能力下降导致伤口愈合延迟、跌倒风险上升;肠道与泌尿道黏膜免疫衰弱及菌群失衡促发感染、炎症与失禁。针对免疫衰老的新兴干预包括:mTOR抑制剂、抗炎药及衰老细胞清除药物(如D+Q、Navitoclax),可减少SASP并改善免疫功能;免疫营养(维生素D、omega?3、益生菌、多酚等)与微生物组干预(益生菌、益生元、FMT)可降低炎症、强化屏障功能;规律运动能提升T细胞与NK细胞功能、减少慢炎,并改善疫苗反应。这些策略为延长健康寿命提供新的可能。
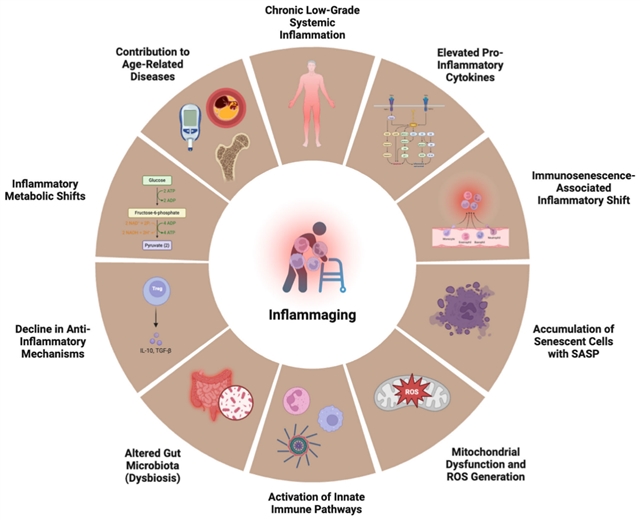
炎症衰老的特征。炎症衰老的核心特征是持续性的慢性低度全身性炎症,这种炎症是由促炎性细胞因子水平升高以及与免疫衰老相关的炎症转变所驱动的——即衰老的免疫细胞会获得促炎性表型。衰老细胞的积累分泌衰老相关分泌表型(SASP),进一步加剧了炎症。线粒体功能障碍和活性氧(ROS)的产生激活先天免疫途径,而与衰老相关的肠道微生物群变化(失调)则促进对微生物产物(如脂多糖(LPS))的全身暴露。同时,抗炎机制的减弱,例如调节性 T 细胞(Tregs)分泌的 IL-10 和 TGF-β 减少,也起到了作用。炎症代谢的转变,包括糖酵解的增加和脂质代谢的改变,支持促炎性免疫细胞的功能。总之,这些过程加速了与年龄相关的疾病的发病和进展,包括心血管疾病、2 型糖尿病、骨质疏松症和神经退行性疾病。
研究总结
尽管对免疫衰老和慢性炎症的认识不断加深,但仍存在多项关键未解问题。首先,免疫老化呈高度异质性:部分老年人维持较强免疫力,另一些却出现明显衰退,其背后的遗传、环境与生活方式因素复杂交织,机制仍不清晰。其次,老年人对疫苗与感染的免疫反应下降,其机制不仅限于T细胞耗竭和抗体减少,个体化疫苗策略及新型佐剂的开发仍处起步阶段。此外,肠道与泌尿道微生物组随年龄显著改变,其如何影响黏膜免疫稳态与系统炎症尚未完全阐明。随着全球老龄化加剧,医疗系统需要从传统的疾病治疗模式转向预防性和再生性策略,包括在临床中纳入免疫衰老评估、发展个体化免疫治疗,以及加强转化研究投入。生活方式干预(如运动、营养与微生物组调控)亦应成为公共卫生重点,以提升免疫韧性并减轻医疗负担。
从基础研究迈向临床应用仍面临监管、经费以及老年群体在临床试验中代表性不足等障碍。许多针对年轻人的治疗未必适用于老年免疫系统,迫切需要开发年龄特异性的药物与临床试验设计。转化老年科学通过靶向细胞衰老、线粒体损伤和免疫紊乱等核心老化机制,有望改善免疫功能并延长健康寿命。基于生物标志物的个体化免疫干预正在兴起,而微生物组治疗的临床验证更需依赖标准化方法、精准分型及控制饮食与抗生素等干扰因素。另一方面,衰老细胞清除(senolytics)在早期临床中展现潜力,但仍需证明其获益是否伴随可接受的安全性,并避免影响组织修复与抗肿瘤机制。总体而言,老龄化深刻重塑免疫系统,引发多系统功能衰退。通过跨学科研究与临床创新,有望开发新型免疫调节策略,提升老年人的健康与生活质量。
Medical Sciences 期刊介绍
主编:Prof. Dr. Antoni Torres, Universidad de Barcelona, Spain
发表关于疾病分子和细胞过程的原始研究、评论文章和简短通讯,以增加对医学基本原理和生物学问题的理解。
|
2024 Impact Factor
|
4.4
|
|
2024 Citescore
|
8.7
|
|
Time to First Decision
|
18.7 Days
|
|
Acceptance to Publication
|
2.8 Days
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。