|
|
|
|
|
脊髓损伤修复中的工程化革新:多模态治疗融合开启临床转化新范式 Engineering |
|
|
论文标题:Frontier Integration in Spinal Cord Injury Repair: Engineering-Driven Mechanistic Exploration and a New Paradigm for Clinical Translation
期刊:Engineering
DOI:https://doi.org/10.1016/j.eng.2025.11.012
微信链接:点击此处阅读微信文章

脊髓损伤(SCI)作为中枢神经系统高致残性创伤,全球年新增病例超57万,患者常面临感觉、运动及自主神经功能的不可逆丧失。传统治疗局限于急性期手术减压、并发症管理及康复训练,难以突破神经再生的核心瓶颈。近日,天津医科大学总医院冯世庆团队在《Engineering》发表文章,通过神经调控、细胞工程、生物材料与精准递送的多模态融合策略,系统性破解SCI修复的复杂难题,为临床转化提供了全新范式。
一、研究背景
脊髓损伤(spinal cord injury, SCI)作为中枢神经系统的创伤性疾病,会导致感觉、运动及自主神经功能不可逆丧失,给患者、家庭和社会带来沉重负担。传统治疗局限于急性期手术减压、并发症管理和康复训练,难以突破神经再生与功能重建的核心瓶颈。这一临床困境根源在于SCI病理机制的极端复杂性,其并非静态损伤,而是一个随时间动态演进的级联反应过程。近年来,随着生物材料、神经工程、细胞分子生物学等学科深度融合,以“主动干预、多模态协同”为核心的工程化治疗策略应运而生,推动SCI治疗向多靶点、时序化调控的再生医学模式深刻转型。
二、病理机制:脊髓损伤微环境失衡是动态性的级联反应
构建脊髓损伤(SCI)的工程化修复策略需首先明晰其病理机制——该机制主要基于本团队之前提出的“脊髓损伤微环境失衡理论”。原发性损伤阶段主要由瞬间机械外力直接导致神经元、胶质细胞死亡及血管破裂,构成不可逆的损伤核心;随之触发的继发性损伤更为关键,这是临床干预的关键窗口,可持续数周至数月。继发性损伤主要分为三期:急性期(数分钟至数天),血–脊髓屏障被破坏,外周免疫细胞浸润引发细胞因子风暴,氧化应激、水肿及兴奋性毒性共同导致二次细胞死亡;亚急性期(数天至数周),炎症反应呈现双面性,巨噬细胞向促进修复的M2表型转化以清除组织碎片,同时反应性星形胶质细胞增殖形成早期胶质瘢痕;慢性期(数月至数年),炎症逐渐消退,成熟质密的胶质瘢痕与纤维化组织形成,构成轴突再生的永久性屏障,且内源性修复能力同步衰竭。这一复杂且序贯的病理进程决定了单一疗法难以奏效,凸显了多靶点、时序化工程干预的必要性。
脊髓损伤后,脊髓微环境的平衡被打破,引发一系列连锁病理生理变化(图1)。这种微环境失衡在不同时间和部位表现为分子、细胞和组织三个层面的异常:分子水平包括神经营养因子及其前体肽、细胞因子、趋化因子等的表达异常;细胞水平包括星形胶质细胞活化、内源性神经干细胞分化紊乱、少突胶质前体细胞及小胶质细胞功能异常、巨噬细胞浸润等;组织水平包括出血与缺血失衡、胶质瘢痕形成、脱髓鞘与再髓鞘化失衡等。基于微环境失衡的脊髓损伤病理机制,核心可概括为神经元内微环境失衡与再生微环境失衡:神经元内微环境失衡表现为凋亡、铁死亡等导致的神经元丢失,以及线粒体供能不足、细胞骨架崩解、mTOR 通路抑制引发的轴突再生失败;再生微环境失衡则由胶质与纤维瘢痕构建的物理化学屏障,M1型免疫细胞主导的炎症风暴,以及脱髓鞘产生的Nogo-A等抑制因子共同构成。这种内外环境的恶性协同,最终抑制内源性修复过程,阻碍神经功能重建。上述各层面失衡均是神经再生与功能恢复的核心障碍,进一步印证了多靶点、时序化工程干预的必要性。
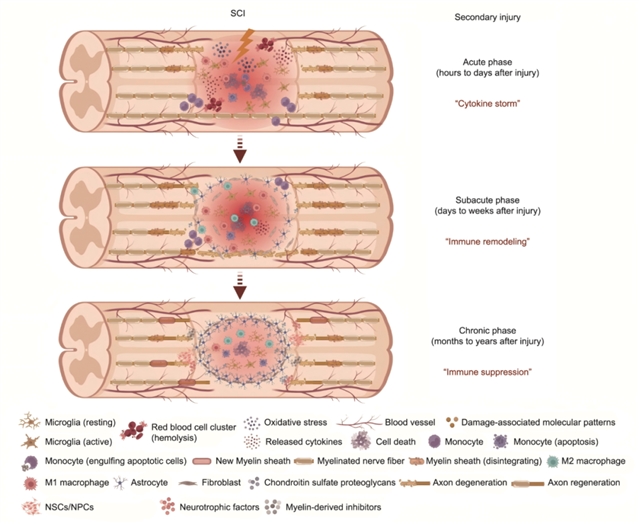
图 1. SCI后继发性损伤阶段的时间病理演变及主要特征。
三、多模态工程化技术整合体系:协同突破修复瓶颈
面对上述病理挑战,融合神经调控、细胞疗法、生物材料与精准递送的工程化策略正从多维度破解SCI修复难题,实现“1 + 1 > 2”的治疗效果(图2)。
1.神经调控技术:神经刺激与调控是SCI工程化治疗的核心,突破了传统“仅修复组织”的局限,而是通过调控神经信号、激活残存环路、以及促进神经重塑,直接靶向功能重建,为长期瘫痪患者带来康复希望。其中,硬膜外脊髓电刺激(ESCS)通过植入电极阵列激活因失去上位输入而“休眠”的脊髓中枢模式发生器,在临床研究中已帮助部分完全性损伤患者恢复自主站立及节奏性踏步。与此同时,非侵入性调控技术,如重复经颅磁刺激(rTMS),可调节大脑皮层兴奋性,改善上肢功能与神经病理性疼痛。此外,低强度脉冲超声(LIPUS)可协同药物或干细胞促进损伤修复,低强度聚焦超声(LIFU)可安全打开血–脊髓屏障,为靶向递送提供新路径。值得注意的是,脑机接口作为前沿交叉技术,可将大脑运动意图转化为外部设备指令,与ESCS联用构建“脑-脊髓”数字桥梁,已在临床中帮助瘫痪患者恢复自主运动控制。
2.工程化细胞疗法:细胞疗法的核心已从单纯移植转向“工程化赋能”,可通过精准改造提升修复效能。借助病毒载体让干细胞过表达神经营养因子或抗凋亡蛋白,将其改造为持续分泌治疗因子的“活体药厂”,大幅提升其在损伤环境下的存活能力与修复效能。而将这类工程化细胞负载于生物材料中移植,通过三维支架提供机械支撑与微环境保护,突破细胞移植中存在的效率低、存活率差的瓶颈。可移植的细胞类型逐渐多元化,诱导的多能干细胞(iPSCs)、神经干细胞(NSCs)、间充质干细胞(MSCs)等经定向分化后,可替代受损神经元、调节炎症微环境。虽然细胞疗法在临床研究中表现出良好安全性,且已初步被证实可改善患者的神经功能,但仍需优化移植效率、解决细胞存活等问题,是SCI修复的核心研究方向之一。
3.智能生物材料:生物材料已演进为更加智能的微环境条件元件,能够为修复提供精准支撑。其中仿生3D打印支架可精确模拟脊髓解剖结构与力学梯度,内部预设的微通道可引导轴突定向生长,实现“结构仿生+功能导向”的双重目标;智能响应系统则能感知损伤局部微环境变化,实现治疗药物的按需精准释放;导电水凝胶可实现无线原位电刺激,协同促进神经再生。此外,纳米靶向系统可穿透生物屏障,将药物特异性递送至活化胶质细胞,直接靶向“源头”;可植入的缓释系统则能在硬膜外腔长期、局部地释放促再生小分子药物,规避全身副作用。
4.外科与分子干预:在外科与分子干预方面,也实现从早期减压向功能重建延伸的理念升级。神经桥接技术通过自体或工程化移植物搭建“轴突再生桥梁”,为轴突再生提供有引导的通道。同时,扩张性硬脊膜成形术可降低椎管内压力,改善脊髓的灌注状态,突破传统减压手术局限。而在分子层面,针对瘢痕形成、炎症反应等关键通路,开发特异性抑制剂(如软骨素酶ABC)与促再生因子(如BDNF、GDNF),结合缓释系统实现长期局部作用。以上这些技术并非彼此孤立,通过有机组合,它们可同时在化学信号和电信号层面协同促进神经再生与环路重组,达到最优的修复效果。
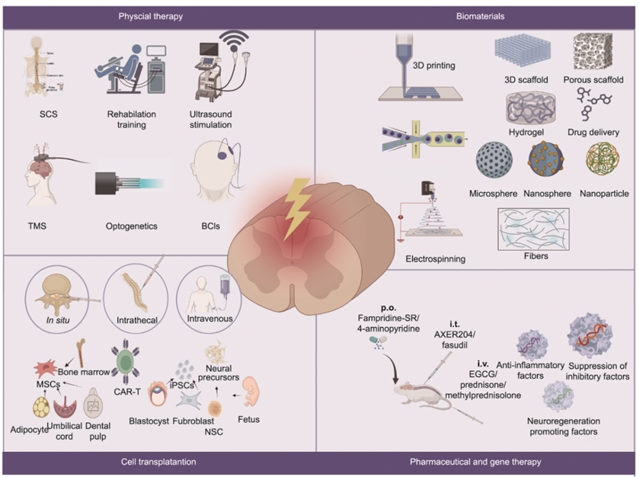
图 2. 新兴临床工程治疗策略。
四、临床前与临床的双重突破
1. 生物材料:由被动填充向智能微环境调控演进
生物材料的研究重心已完成从单纯物理支撑向精准调控病灶微环境的转变。天然水凝胶(如胶原、纤维蛋白)凭借卓越的生物相容性,在早期抑制胶质瘢痕方面表现出色,但其机械强度不足且在体内易降解。为此,研究者开发了GelMA、PLGA等复合材料以兼顾力学强度与生物活性,并利用3D打印技术构建出仿生支架,定向诱导轴突跨越损伤区。在临床转化方面,可吸收聚合物神经脊髓支架(NSS)已通过初步安全性验证,载细胞胶原支架在长期随访中也展现出改善患者独立行走能力及排便功能的潜力。然而,如何实现材料降解速率与组织再生进度的精确匹配,并降低其高昂的制造工艺成本,仍是当前标准化的核心瓶颈。
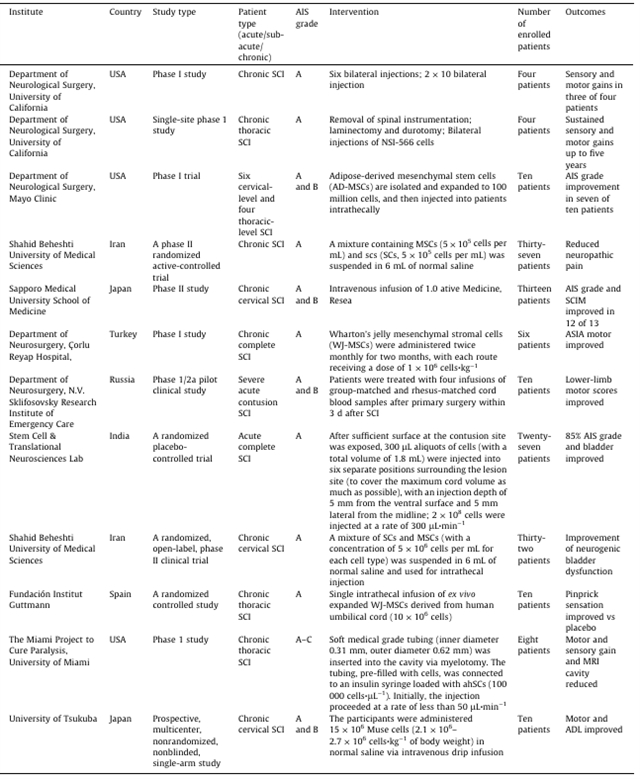
2. 细胞移植:从简单注射向系统整合
细胞疗法正从早期的细胞悬液注射向复杂的组织工程化移植进化。多项I期临床试验证实了自体施万细胞(ahSC)和间充质干细胞(MSCs)经损伤灶或鞘内移植的安全性(表 1)。为了克服因病灶严酷微环境所导致的移植细胞低存活率难题,相关研究通过基因修饰或将细胞锚定于生物材料支架,有效提升了种子细胞的存活率及其定植与整合效率。尽管如此,临床应用中仍需警惕细胞的非定向分化(如异常神经胶质增生)及免疫排斥风险,其在慢性期损伤中的疗效稳定性仍需进一步验证。
3. 神经调控:从粗放刺激向精准闭环刺激的迭代
神经调控技术通常不直接导致轴突的长距离再生,而是利用相关物理刺激激活残余神经环路的突触可塑性。目前,硬膜外脊髓电刺激(ESCS)与深部脑刺激(DBS)正由传统的粗放式刺激向精准电极阵列进化。非侵入性技术同样取得突破,如ARC-EX系统已获FDA批准,显著提升了慢性SCI患者的手部运动功能;同时,脑机接口通过整合AI算法与虚拟现实(VR)技术,正在开启数字化康复的新范式。不过,植入式设备引发的异物反应和信号衰减,以及刺激参数(频率、电压)的个体化标准缺失,依然是限制其广泛应用的主要障碍。
4. 多模态协同:构建“全方位集成”的修复体系
鉴于单一疗法的疗效瓶颈,“药物、材料、细胞、调控”四位一体的深度融合已成为未来主流。具体表现在:① 智能控释:如利用刺激响应型水凝胶,在检测到病理信号(如ROS或MMP)或接收到外部物理信号(如磁场、超声)时,精准释放治疗药物。② 空间引导与生物辅助:采用3D微柱结构引导星形胶质细胞自组装,为神经元生长构建天然生物支架。③ 物理信号强化:结合脉冲电、磁场等物理辅助,通过激活Wnt/β-catenin等信号通路,提升移植干细胞分泌相关神经营养因子的效率。
表 1. 细胞疗法代表性临床试验总结。
五、临床转化挑战与未来展望
尽管临床前研究成果丰硕,但工程化策略迈向广泛应用仍面临严峻挑战。多模态技术协同是突破单一疗法局限的关键,但技术协同对操作精度与协调性要求较高,各组件的最佳介入时机、空间布局与剂量序列仍需海量数据进行优化。损伤的高度异质性还要求治疗方案的个性化,未来需结合患者影像、分子标志物与人工智能预测来定制干预路径。此外,工程化细胞、新型生物材料及植入式设备的长期生物安全性、功能稳定性及伦理问题,必须通过严谨的长期临床试验来验证,并推动建立与之相适应的监管与评估新框架。(图3)
展望未来,SCI修复将依赖于更深度的融合创新。例如:下一代闭环智能神经假体将集成实时传感与自适应刺激,实现真正意义上的与脑机接口技术结合。患者特异性脊髓类器官与器官芯片,将成为个性化药物筛选和疗法预测的强大平台。最终,推动临床医生、工程师与基础科学家的跨学科协作,构建“临床问题反向驱动研发”的转化闭环,加速前沿技术落地。
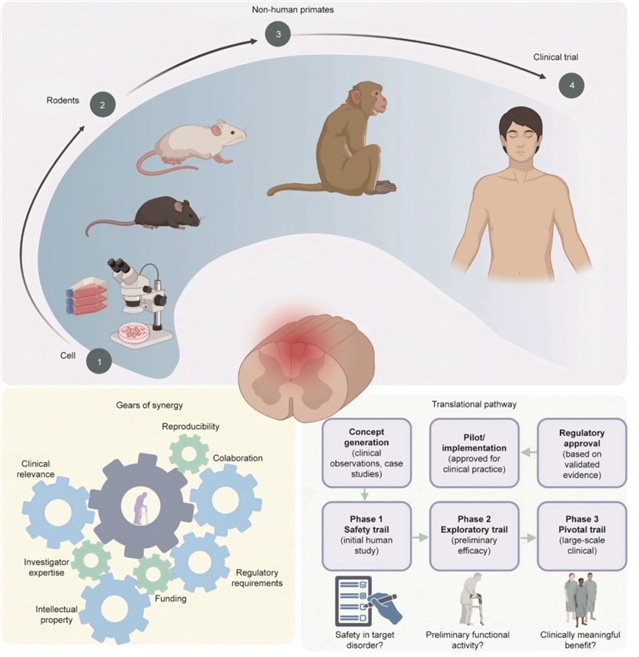
图 3. SCI研究的临床转化路径。
六、结论
SCI修复已步入一个以 “多模态融合”与“主动功能化重建” 为标志的新时期。面对复杂有序的病理级联,单一疗法已显不足,取而代之的是集成神经调控、细胞工程、生物材料与精准医学的系统性策略。尽管仍需通过大规模临床试验验证其长期安全性与标准化方案,但这一跨学科创新范式,已为SCI患者架起了从瘫痪走向功能恢复的坚实桥梁,是中枢神经损伤修复领域的重大突破。
七、作者
第一作者:周密博士,天津医科大学总医院;姚雪研究员,天津医科大学总医院;
通讯作者:冯世庆教授,天津医科大学总医院 山东大学齐鲁第二医院。
论文信息:
Mi Zhou,Xue Yao,Boya Huang,Jie Ren,Haiwen Feng,Shiqing Feng. Frontier Integration in Spinal Cord Injury Repair: Engineering-Driven Mechanistic Exploration and a New Paradigm for Clinical Translation. Engineering, 2025 DOI: 10.1016/j.eng.2025.11.012
撰文︱周密,天津医科大学总医院
姚雪,天津医科大学总医院
审阅︱冯世庆,天津医科大学总医院 山东大学齐鲁第二医院
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。