|
|
|
|
|
Shingrix疫苗接种后神经系统和肌肉骨骼症状持续| MDPI Reports |
|
|
论文标题:Prolonged Neurological and Musculoskeletal Symptoms Following Shingrix Vaccination
论文链接:https://www.mdpi.com/2571-841X/7/4/83
期刊名:Reports — Clinical Practice and Surgical Cases
期刊主页:https://www.mdpi.com/journal/reports
一、引言
重组带状疱疹疫苗(Shingrix)是美国食品药品监督管理局(FDA)于2017年推出的一种两剂加强型重组疫苗,用于预防50岁及以上高风险患者的带状疱疹(带状疱疹)。
带状疱疹的估计终生发病率为10%至20%。该病的死亡率较低,但该病毒会引起疼痛性的囊泡性皮疹。更重要的是,该病毒有可能引发带状疱疹后神经痛,这是一种带状疱疹并发症,影响10–18%的患者,导致严重神经痛,且这些症状可能随着时间缓解,也可能不会。
根据美国疾病控制与预防中心(CDC)的数据,重组带状疱疹疫苗在70岁及以上成年人预防带状疱疹的有效率为97%。CDC报告的副作用中,最常见的包括轻度或中度疼痛、注射部位红肿和积液、疲劳、头痛、肌痛、发热、腹痛、胃肠症状和恶心。此外,可能出现的严重症状还包括过敏反应——皮疹、瘙痒、潮红、积液和过敏性休克。虽然罕见,但神经病变已被识别为重组带状疱疹疫苗接种后的不良事件。
二、病例报告
本病例患者为一名50岁女性,患有克罗恩病史,并因运动损伤引发右膝疼痛,2022年10月在初级保健诊所接种了重组带状疱疹疫苗。在左三角肌接种重组带状疱疹疫苗数小时后,患者出现了全身性类流感症状,包括发烧、全身肌肉痛和关节痛,以及被描述为“比剧烈运动更严重的疼痛”的疲劳。注射后的第二天(第2天),患者出现恶心和食欲减退,同时首次出现双臂及左前大腿(左侧>右侧)的刺痛感和灼烧感。左三角肌注射部位明显肿大、发热且出现红斑,这些症状持续了大约两周才完全缓解。第三天,她的发烧、恶心/食欲减退、肌痛和疲劳都缓解了;但她仍有持续的疼痛,描述为双侧关节(包括肘部、脚踝和膝盖)剧烈的“酸痛”,并且这些受影响的关节有明显肿胀。
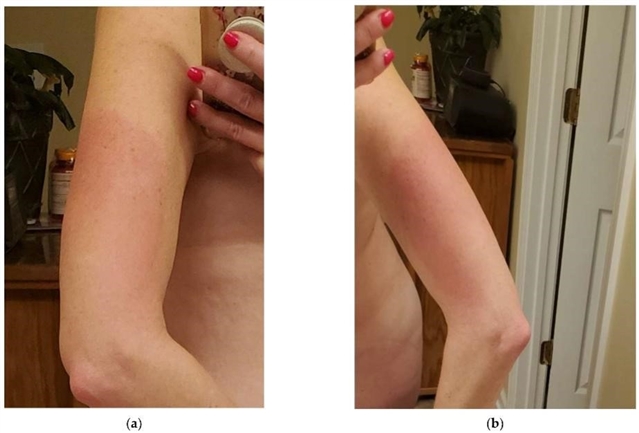
2022年11月至2023年1月期间,患者持续每天关节疼痛和肿胀,尽管每日服用非处方布洛芬,但未见改善。患者还报告双臂间歇性刺痛。患者在此期间被转诊进行神经传导检查,结果显示存在腕管综合征,除此之外,未报告显著发现。2023年1月,患者停止每日服用布洛芬,开始使用局部草药油,同时使用绷带和动能胶带。患者报告每日使用后不适和积液有轻微改善。此后医生建议她去骨科做进一步评估。患者于2023年2月接受了X光检查,未发现异常。医生也在那段时间为患者安排了化验,结果显示炎症指标无异常。2023年4月的重复化验显示她的炎症指标无异常。
截至2023年8月,尽管每日使用草药油,患者仍持续出现左下肢手臂及外侧间歇性刺痛,以及间歇性关节疼痛和积液。患者报告称曾就诊多位医生,但他们无法解释上述疼痛、积液和刺痛发作的原因和复发原因。在出现这些症状后,患者拒绝了她当前医生建议的第二剂加强针,担心这可能弊大于利。
三、讨论
回顾这一复杂病例,凸显了为疫苗接种后长期且难以诊断症状的患者优化护理的若干机会。例如,虽然反复的化验和影像检查在本案中均为阴性,但转诊到风湿科或神经科等专科医生,本可提供对她关节和神经系统症状的进一步专家评估。与主治医生的连续性提升,可能导致更早采用多学科合作。患者报告称一年内多次看过多位医生,但护理几乎没有连续性。患者还承认这些医生不愿接受她症状的确是疫苗所致。
虽然疫苗普遍表现出较强的安全性,但一些研究表明,尤其是Shingrix的神经不良事件可能与AS01佐剂中的QS-21成分有关。有假设认为,疫苗触发的分子模拟可能导致免疫交叉反应,导致某些个体出现类似自身免疫的症状。尽管所有这些疫苗都记录了短期副作用如暂时性反应原性,但疫苗不良事件报告系统(VAERS)或CDC尚未对长期副作用有广泛记录。需要进一步研究以了解潜在的慢性影响。
此病例特殊之处在于,上述患者的症状未被报告为重组带状疱疹疫苗的列明副作用之一。临床试验中报告的最常见不良事件包括注射部位疼痛(78.7%)、肌痛(45.4%)、疲劳(45%)、头痛(38.1%)、寒战(31.9%)、发热(30.5%)和胃肠道症状(26.8%。更重要的是,有经验的试验中未报告长期副作用,这从该患者接种疫苗近一年后症状持续可见一斑。虽然疫苗的初步安全性数据正在广泛审查中,并通过预许可临床试验和短期上市监测获得,但持续监测不良事件对患者群体的益处和风险至关重要。罕见疫苗风险可能只有在接种数百万剂疫苗后才显现,有些不良事件可能在接种后数月甚至数年后才出现。因此,像VAERS这样强大的系统对于持续的安全监测至关重要。医疗服务提供者应密切监测患者接种疫苗后的健康状况,并报告任何可能引起关注的事件。这需要对罕见疫苗相关效应的可能性保持开放态度,即使没有确凿的因果关系。无论病因如何,患者的疑虑和经历都应仔细记录。收集重组带状疱疹疫苗等疫苗的长期数据,有助于进一步了解其安全性。不良事件报告的增加还能加强上市后监测,完善使用指南,识别可能受益于更个性化疫苗推荐的高风险人群。还需要更多研究来确定接种重组带状疱疹疫苗后易发生长期不良反应的患者群体之间的因果关系。展望未来,此病例进一步强调了需要进行更多长期药物警戒和研究,以更好地描述重组带状疱疹疫苗接种后长期副作用的发生率,尤其是在易感亚组中。
必须强调的是,本病例报告强调了重组带状疱疹疫苗接种后引发的令人担忧的不良事件,不应被解读为反疫苗文献。记录和理解安全信号,即使是罕见的,也能提供适当的教育和充分评估其利弊。大量数据压倒性地支持重组带状疱疹疫苗在适当人群中的显著公共卫生优势。然而,保持完整安全档案的透明度同样重要。我们提醒不要基于有限的病例报告做出笼统结论或夸大影响。医疗提供者应继续根据指南推荐接种该疫苗。监测潜在风险并不会降低疫苗的信心或有效性。
四、结论
此案提醒我们,持续监测和研究纵向疫苗结果的必要性。尽管采用标准干预和阴性诊断结果,该患者躯体和神经症状依然持续存在,凸显了医疗提供者对疫苗相关并发症可能性的高度认识。记录和报告个体经历,如本案所示,有助于早期发现罕见不良事件,并有助于完善安全筛查方案,保护弱势患者群体。
Reports—Clinical Practice and Surgical Cases期刊介绍
主编:Prof.Dr. Toshio Hattori, Tohoku University, Japan
Reports—Clinical Practice and Surgical Cases(ISSN 2571-841X)是一个国际同行评审、开放获取的医学期刊,主要发表医学全学科的病例报告。Reports被多个知名学术数据库收录,包括Web of Science的ESCI、PubMed等。
2025 Impact Factor:0.6
Time to First Decision:21 Days
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。