论文标题:Endocrine Disrupting Toxicity of Bisphenol A and Its Analogs: Implications in the Neuro-Immune Milieu
论文链接:http://www.mdpi.com/2039-4713/15/1/13
期刊名:Journal of Xenobiotics
期刊主页:https://www.mdpi.com/journal/jox
研究背景
内分泌干扰物是可模拟、拮抗或干扰机体激素作用的天然或合成物质,因其广泛使用、环境持久性与长期低水平暴露风险而受到公共健康领域关注。双酚A是典型代表,被用于塑料、环氧树脂涂层、热敏纸等多类产品中;其暴露途径包括膳食摄入、皮肤接触和吸入等。欧洲食品安全局在2023年重新评估双酚A风险,将其可耐受每日摄入量下调至0.2ng/kg体重/天,并指出免疫系统是对双酚A暴露最敏感的靶系统之一。与此同时,双酚A替代物双酚AF、双酚F、双酚S被更广泛应用,但其内分泌干扰与免疫、神经相关影响仍存在不确定性。本文旨在以双酚A及其类似物为例,梳理其对免疫与神经系统的潜在不良作用,并从免疫-神经-内分泌网络的互作角度,讨论支架蛋白RACK1作为关键枢纽与筛查工具的意义。
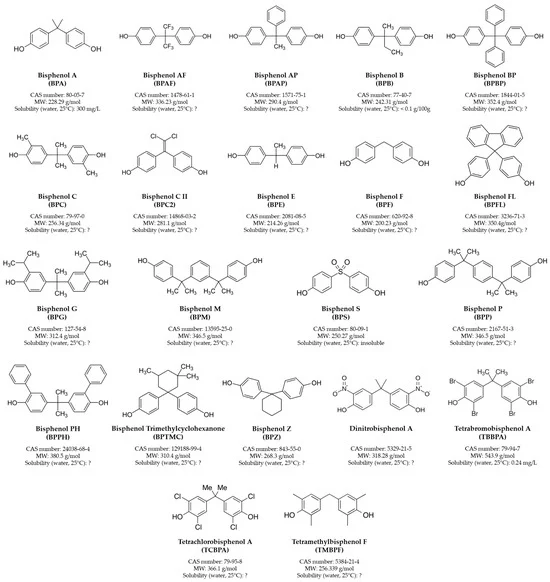
图1. 双酚A及其主要类似物
研究过程与结果
本文为综述性研究,文章整合了流行病学、体内与体外研究证据,概述双酚A及类似物可与多类激素受体相互作用,包括雌激素受体、雄激素受体、甲状腺激素受体、糖皮质激素受体等,导致不同组织、不同细胞类型出现情境依赖性的复杂反应。文中指出,双酚A呈非单调剂量-反应特征,即低剂量暴露同样可能产生生物学效应,从而增加风险评估难度。
在神经系统方面,文献证据提示孕期暴露与儿童神经发育和行为结局相关,且可能与应激反应系统、下丘脑-垂体-肾上腺轴功能紊乱有关。文章进一步总结了与神经退行性病变相关的机制线索,包括氧化应激、炎症反应、蛋白错误折叠以及细胞内钙稳态紊乱等,并提及双酚A可能影响与阿尔茨海默病相关的APP加工通路以及炎症细胞因子释放。
在免疫系统方面,文章归纳了双酚A及类似物对先天免疫和适应性免疫的影响:在巨噬细胞、单核细胞、树突状细胞中可表现为剂量相关的炎症促进或免疫抑制效应;在T细胞分化与细胞因子分泌方面也可产生调节作用。文章强调,免疫效应存在浓度差异与化合物间差异,例如双酚S在部分模型中表现为使免疫细胞更易反应的趋势,而双酚A与双酚AF在较高浓度下可呈免疫抑制相关表现。
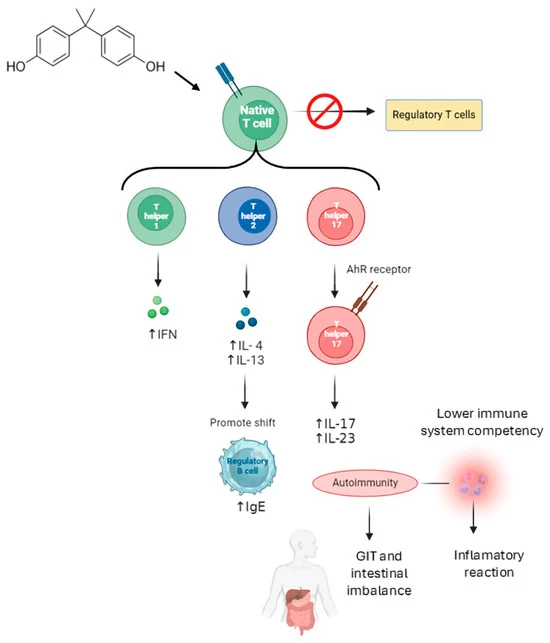
图2. 双酚A(BPA)可能通过激活Th1、Th2和Th17细胞来增强自身免疫反应。芳香烃受体(AhRs)在调节免疫反应中起关键作用,从而导致Th17细胞的产生,Th17细胞在多种自身免疫性疾病中至关重要。
研究总结
本文将双酚A及其常用替代物双酚AF、双酚F、双酚S置于“免疫-神经-内分泌网络”的框架下讨论,核心观点是:这些双酚类物质并非仅影响单一器官或单一激素通路,而可能通过多受体结合与信号交织,在免疫系统与神经系统之间形成相互放大的联动效应。文章提出RACK1(Receptor for Activated C Kinase 1)可作为理解这种联动的关键节点:在免疫细胞中,RACK1作为PKCβII支架蛋白参与细胞活化、CD86表达以及TNF-α、IL-8等炎症介质释放;其转录受糖皮质激素与雄激素调控,并与GRα/GRβ比例、剪接因子等机制相关。在神经系统中,RACK1与应激相关的HPA轴、糖皮质激素信号以及BDNF表达调控存在联系,提示其可能连接应激反应、神经可塑性与炎症状态。基于既往体外数据,文章进一步讨论了双酚A、双酚AF、双酚S对RACK1表达的不同影响及其潜在受体机制,提出以RACK1为中心的系统毒理学模型,用于解释双酚介导的神经炎症、氧化应激与免疫功能异常如何在网络层面耦合。文章同时指出,当前关于双酚类似物(尤其双酚AF)在部分健康结局上的一致性证据仍不足,而免疫系统研究也存在结果不一致现象,提示未来需要结合人群研究与机制研究,并采用系统毒理学方法,将多层级分子变化与功能结局进行整合,以提升对双酚类内分泌干扰风险的解析与筛查能力。
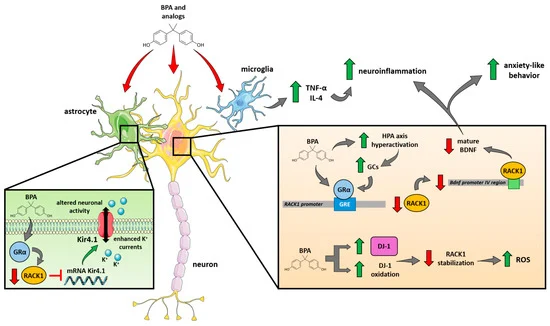
图3. 以RACK1为中心枢纽的毒理学模型提议,用以解释双酚介导的对INEN的不良影响。在神经元水平上,BPA可以直接(通过GRα激动作用)和间接(通过HPA轴过度激活导致的糖皮质激素分泌增加)引起RACK1下调,导致成熟BDNF产生减少,这与焦虑样行为和神经炎症增加相关;同时,BPA诱导的DJ-1表达增加和氧化作用有助于减少RACK1的稳定性,导致ROS清除能力下降和氧化应激增加。在小胶质细胞中,BPA刺激TNF-α和IL-4的产生和释放,从而促进并加剧神经炎症。最后,在星形胶质细胞中,BPA可能激活GRα并降低RACK1表达;RACK1水平下降,本来RACK1有助于下调Kir4.1 mRNA,RACK1下降导致Kir4.1表达增加,从而增强K?电流并改变神经元活动。
JoX 期刊介绍
主编:François Gagné, Aquatic Contaminant Research Division, Canada
期刊主题涵盖异型生物质毒素、异型生物质药理学、环境有害异物、内分泌干扰物、氧化应激、抗生素、生物标记物、纳米粒子、塑料微粒、农药、除草剂。期刊现已被Scopus、ESCI (Web of Science)、PubMed等数据库收录。
|
2024 Impact Factor
|
4.4
|
|
2024 CiteScore
|
6.0
|
|
Time to First Decision
|
22.7 Days
|
|
Acceptance to Publication
|
3.9 Days
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。