|
|
|
|
|
蛋白质变体的困惑:理论数量巨大,为何实际检测到的很少? | MDPI Proteomes |
|
|
论文标题:Puzzle of Proteoform Variety—Where Is a Key?
论文链接:https://www.mdpi.com/2227-7382/12/2/15
期刊名:Proteomes
期刊主页:https://www.mdpi.com/journal/proteomes
一个基因只对应一种蛋白质——这是教科书给我们的印象。但真实情况要复杂得多:一个基因可以通过可变剪接产生多种mRNA,每种mRNA翻译出的蛋白质还可以经历数十种翻译后修饰。这些不同形式的蛋白质被称为“蛋白质变体 (proteoforms)”。
理论上,蛋白质变体的数量可以极其庞大。有估算认为,每个细胞类型中可能存在超过100万种不同的蛋白质变体。但实验检测到的,却远少于这个数字。这种理论预测与实验观测之间的巨大差距,成为当前蛋白质组学领域一个颇具挑战性的科学问题。
俄罗斯科学院生物医学化学研究所的Stanislav Naryzhny教授,在本文中对这个问题进行了深入探讨, 并尝试从理论与实验两个层面解释这种差距产生的原因。
一、什么是蛋白质变体?
2010年,Neil Kelleher提出了“proteoform”一词,用于指代由单个基因产生的所有可能的蛋白质分子形式,包括遗传变异、可变剪接RNA转录本和翻译后修饰所带来的结构差异。这一概念为描述蛋白质复杂性提供了更加精确的框架。
随着研究的发展,这一术语现已取代早期的“protein species”,并成为该领域的标准用语。
简单来说,一个基因可以产生多种蛋白质变体,就像一棵树可以长出不同形态的枝叶,而这些差异共同构成了蛋白质功能多样性的基础。
二、理论计算与实际检测的巨大差距
文章指出,如果考虑所有可能的翻译后修饰组合,蛋白质变体的理论数量是惊人的。以磷酸化为例,一个蛋白如果有10个磷酸化位点,每个位点可以处于磷酸化或非磷酸化状态,理论上就有210=1024种可能的磷酸化变体。再加上其他修饰类型(乙酰化、糖基化、泛素化等),组合数量会呈指数级增长。
然而,实际通过质谱等技术检测到的蛋白质变体数量远低于此。这种理论与现实的差距意味着什么?
作者提出,似乎存在严格的调控机制,控制着翻译后修饰的产生和维持。虽然理论上蛋白质变体的复杂程度可以极高,但细胞实际实现的只是其中一小部分。这些调控机制可能涉及修饰酶的活性、底物可及性、蛋白质降解系统等,但目前我们对它们知之甚少。
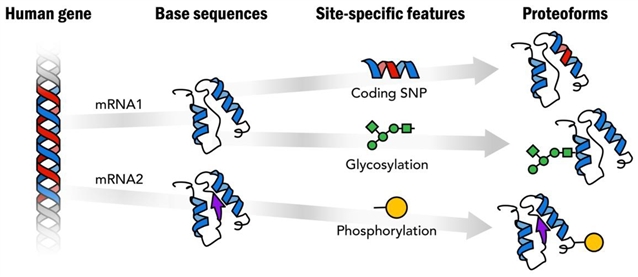
图1. 蛋白质变体是由单个人类基因产生的不同的蛋白质形式。
三、现有的检测方法及其局限
为了检测蛋白质变体,研究者主要依赖两种质谱技术策略。
自上而下法(top-down MS):直接测量完整蛋白质的分子量,可以明确识别翻译后修饰的组合状态,避免酶解过程中信息的丢失。这种方法对于鉴定完整的修饰模式非常有效,但对质谱仪的分辨率和样品纯度要求较高,且对高分子量蛋白的分析仍有挑战。
自下而上法(bottom-up MS):先将蛋白质酶解成肽段,再通过液相色谱-质谱联用分析肽段,最后推断原始蛋白质的修饰状态。这种方法灵敏度高、通量大,是目前的主流手段。结合二维凝胶电泳(2DE)预分离,可以进一步提高变体覆盖范围。
文章指出,二维凝胶电泳可以根据等电点和分子量分离不同修饰状态的蛋白质,是研究蛋白质变体的经典工具。但它耗时耗力,且对极端分子量或疏水蛋白的分离效果有限。
作者强调,两种方法各有优劣,更重要的是它们互为补充。自上而下法提供整体修饰组合的“全景”,自下而上法则能深入解析修饰位点。结合使用可以获得更全面的蛋白质变体图谱。
四、个体差异与蛋白质变体
文章还提出了一个值得关注的观点:不同个体之间,同一蛋白质的翻译后修饰谱可能存在差异。
作者在摘要中写道:一个蛋白质可能根据修饰位点数量有多种变体,但由于个体调控系统的差异,同一蛋白质在不同生物体中的翻译后修饰谱略有不同。
这一观点提示,蛋白质变体谱可能是个体化表型的分子基础。如果确实如此,那么传统的生物标志物研究——通常检测蛋白质的总量——可能会错过真正关键的变异信息。真正与疾病相关的,可能不是某个蛋白的“多少”,而是它的“哪种形式”。
五、降解组:被忽视的变体来源
文章还提到了一个常被忽视的蛋白质变体来源:降解组(degradome)。
蛋白质在细胞内不断被合成和降解。当蛋白质被蛋白酶体降解时,会产生大量多肽片段。这些片段有些可能具有生物活性,有些可能作为抗原被递呈,它们本身也是蛋白质变体的一种形式。
文章指出,降解组的研究还处于早期阶段,它可能是蛋白质变体多样性的一个重要组成部分,但目前我们对它的了解还非常有限。
六、结语
蛋白质变体的研究正处于从“发现”走向“解析”的关键阶段。理论预测与实验检测的巨大差距提醒我们,细胞内存在精密的调控网络在控制着蛋白质的最终形式。揭开这些调控机制,不仅能深化对细胞功能的理解,也可能为疾病诊断和治疗提供全新的视角。
正如文章标题所问的:“Puzzle of Proteoform Variety—Where Is a Key?”——解开蛋白质变体之谜的钥匙,或许正隐藏在未来的蛋白质组学研究之中。
Proteomes 期刊介绍
主编:Jens R. Coorssen, Brock University, Canada; Matthew P. Padula, The University of Technology Sydney, Australia
期刊专注于蛋白质组分析的各个方面,特别关注蛋白质组在蛋白质形式(proteoforms)、功能性生物学单元以及标准氨基酸序列水平上的定量和表征。目前已被Scopus、ESCI (Web of Science)、PubMed等数据库收录。
2024 Impact Factor: 3.6
2024 CiteScore: 7.2
Time to First Decision: 28.6 Days
Acceptance to Publication: 5.6 Days
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。