|
|
|
|
|
中山大学戴宗教授课题组:表面酶聚合结合Cu2+增敏技术的microRNA超灵敏电化学检测 | MDPI Targets |
|
|
论文标题:Attomole Electrochemical Detection of MicroRNAs Based on Surface-Initiated Enzymatic Polymerization Coupled with Copper Enhancement
论文链接:https://doi.org/10.3390/targets1020007
期刊名:Targets
期刊主页:https://www.mdpi.com/journal/targets
研究背景
miRNA是一类内源性的具有调控功能的非编码RNA,参与生命活动各个层次的调节,还与恶性肿瘤等重大疾病的发生与发展密切相关。建立快速和高灵敏的miRNA检测方法,在肿瘤诊断和临床医学等方面具有重要的理论意义和实用价值。
中山大学生物医学工程学院戴宗教授课题组在 Targets 期刊发表了“Attomole Electrochemical Detection of MicroRNAs Based on Surface-Initiated Enzymatic Polymerization Coupled with Copper Enhancement”文章,该检测体系包括二组微粒,一组是发夹探针标记的磁性微球 (Magnetic Beads, MB),另一组是链酶亲和素和RNA或DNA引物修饰的聚苯乙烯微球 (Polystyrene microspheres, PS)。待测miRNA和MB温育杂交后,发夹探针的茎部被打开,通过生物素–亲和素 (biotin-avidin) 作用连接捕获PS微球,后者表面修饰的大量RNA或DNA引物可分别被Poly(A) 聚合酶或末端转移酶聚合延伸,硫酸消化后,用示差脉冲伏安法 (DPV) 检测腺嘌呤的电化学信号,可实现miRNA的灵敏检测。进一步通过在测定体系中加入Cu2+,可使腺嘌呤的电化学响应信号进一步增强。因此,基于微球富集、聚合酶扩增、铜离子增强等三重信号放大策略,miRNA的检出限低至120 aM (S/N=3),该方法应用于生物样品的检测,结果令人满意。
本文亮点
(1) 微球富集、聚合酶扩增及Cu2+增敏三重信号放大技术实现miRNA的超灵敏电化学检测;
(2) 方法可应用于多种微量肿瘤标志物的检测,有望为肿瘤或其他疾病的早期诊断提供新技术。
图文导读
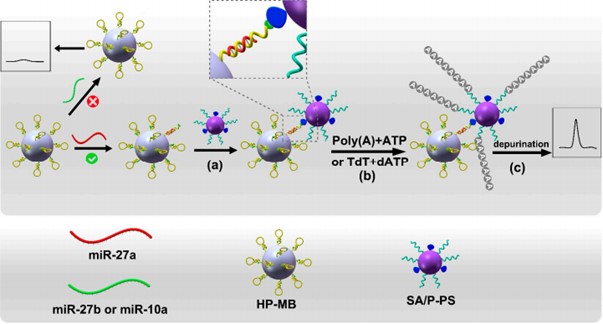
图1为miRNA的电化学检测方法原理:(a) 靶标miR-27a被HP-MB捕获后与SA/P-PS连接;(b) 对引物进行表面扩增;(c) 扩增产物去嘌呤化后进行电化学检测。

图2为TEM图:(A) HP-MB磁珠;(B) SA/P-PS微球;(C) 100 nM miR-27b处理的HP-MB和SA/P-PS;(D)1 nM miR-27a靶标处理的HP-MB和SA/P-PS。
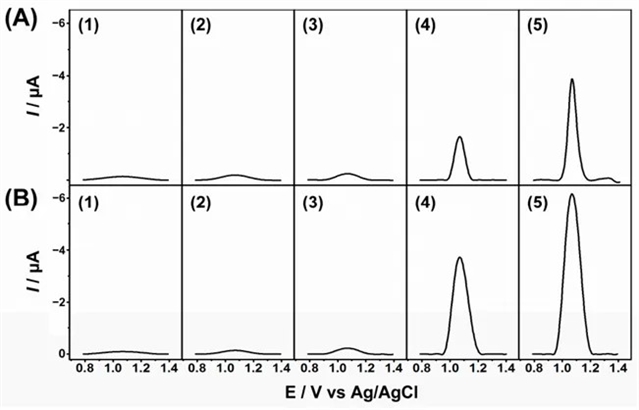
图3为:(A) PAP扩增后的电化学信号;(B) TdT扩增后的电化学信号,其中所加待测物分别是PBS 空白 (1), 250 fM miR-10a (2), 250 fM miR-27b (3), 120 fM miR-27a (4) and 250 fM miR-27a (5)。
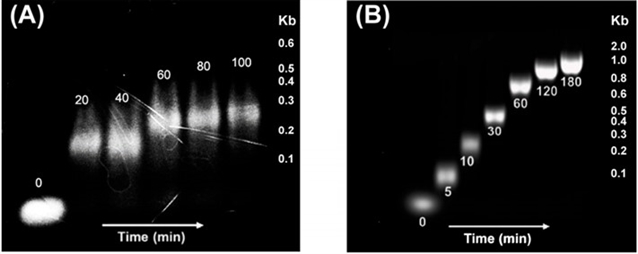
图4为琼脂糖凝胶电泳。(A) 由PAP催化的RNA和 (B) 由TdT催化的DNA在不同时间下的扩增结果。
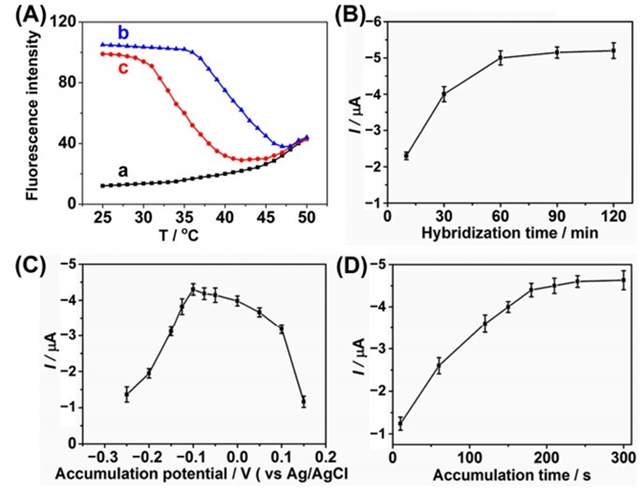
图5为 (A) FAM-DABCYL分子信标的熔链曲线,(a) 不存在靶标;(b) 250 fmmiR-27a靶标;(c) 250 fm miR-27b;(B)杂交时间的影响;(C)富集电位的影响;(D)富集时间的影响。
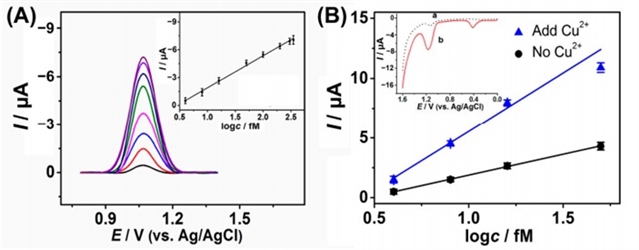
图6为 (A) 浓度为4、8、16、50、100、200、300和350fM (1~8) 的miR-27a的SWVs (插图为峰值电流与浓度对数之间的线性关系);(B) 在不存在/存在2 mg·L-1 Cu2+的情况下,浓度为4、8、16和50 fM的miR-27a的峰值电流图 (插图为在 (a) 不存在和 (b) 存在2 mg·L-1 Cu2+情况下,在基于TdT的SIEP后,16 fM miR-27a的DPV)。
总结与展望
本研究基于三重信号放大技术 (微球富集、聚合酶扩增及Cu2+增敏技术) 建立了一种超灵敏、无标记的miRNA电化学检测方法,在优化实验条件下,检测限低达120 aM。该检测方法无需复杂的PCR扩增即可实现高灵敏度检测,可应用于多种微量肿瘤标志物的检测,有望为人类肿瘤或其他疾病的早期诊断提供新技术。
作者简介

戴宗 教授
中山大学生物医学工程学院
博士生导师、国家基金委优秀青年基金获得者。2004年获南京大学化学博士学位,2004–2007年在法国南特大学和美国亚利桑那州立大学博士后研究。在JACS、Angew Chem,Adv Mater、Nucleic Acids Res 等期刊发表研究论文90余篇,授权国家发明专利15件;为广东省生物医学工程学会传感技术分会副主任委员,广东省食品营养与安全快速检测仪器工程技术研究中心专家咨询委员会委员,Biomedical Analysis 副主编,Targets 编委,《中国化学快报》《高等学校化学学报》青年编委。
研究方向:生化分析与生物传感、体外诊断。

许宇智 助理研究员
中山大学附属第七医院
硕士生导师。2018年获中山大学分析化学理学博士学位,2018–2020年在中山大学化学学院从事博士后研究。已主持包括广东省自然科学基金面上项目 (2项)、博士后科学基金面上资助、深圳市医学研究专项资金SMART项目、深圳市基础研究面上项目等7项基金。已发表SCI期刊论文35篇,其中以第一/通讯 (含共同) 作者身份发表SCI论文15篇 (含中国科学院一区刊物11篇),包括Adv Mater (2篇),TrAC Trends Anal Chem,Anal Chem (5篇),Chin Chem Lett (3篇)等。申请中国发明专利3件,其中授权1件。
研究方向:生化分析与生物医学传感、纳米医学。
Targets 期刊介绍
主编:Huangxian Ju, Nanjing University, China
期刊主要发表靶向识别与治疗相关领域的高质量论文,包括化学测量科学、生命科学、材料科学、药学、临床诊断学、分子医学和生物医学等。
|
Time to First Decision
|
28.4 Days
|
|
Acceptance to Publication
|
3.9 Days
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。