导读
随着肿瘤发病率的持续上升,影像引导下经皮穿刺活检(Image-guided percutaneous needle biopsy,PNB)被认为是疑似癌症诊断的金标准,它有助于确定疾病分期和转移肿瘤的主要位置,其精准性和效率直接影响治疗决策。然而,传统PNB依赖超声/CT影像导航,存在问题:难以实时区分肿瘤与健康组织,假阴性率高达25%;无法获取组织代谢状态,限制了个性化治疗方案的制定。
什么是“影像引导下经皮穿刺活检”?
影像引导下经皮穿刺活检(PNB)是通过超声、CT或MRI等影像技术实施导航,将穿刺针经皮肤刺入体内,获取肿瘤组织样本的微创诊断技术。医生在屏幕上观察针尖位置,引导其到达目标区域后,利用粗针(大于等于1毫米)切取组织条,或细针(小于1毫米)抽取细胞,用于病理学检查。
然而,这种"盲视下的精准"存在局限:患者呼吸、麻醉状态下的无意识移动会使针尖偏移目标;影像仅显示解剖结构,无法识别肿瘤内部的坏死、炎性或高代谢活性区域,导致25%的假阴性率。
光学技术对于体内评估生物组织灌注和代谢参数具有高度敏感性,光学技术的突破性进展为PNB带来了革新机遇。光学PNB是一种有前景的方法,通过选择样本提取区域并获取针尖处血管变化及生物组织代谢信息,提高诊断效率。
近期,俄罗斯奥廖尔国立大学的Viktor V. Dremin团队,在Light: Advanced Manufacturing上发表了题为Optical percutaneous needle biopsy in oncology的文章,介绍了光学PNB的发展,并且详细分析了漫反射光谱(DRS)、荧光光谱(FS)及其多模态融合在光学穿刺针活检中的进展,通过集成光纤探针与标准穿刺针,实现了肿瘤组织识别、代谢状态评估及术前导航,有望显著提升诊断效率。
什么是“漫反射光谱(DRS)与荧光光谱(FS)?
DRS:通过分析组织对光的散射和吸收特性,量化血红蛋白、血氧饱和度等参数,反映组织微循环和结构变化。例如,肿瘤区域因血管异常常显示血氧饱和度降低。
FS:基于内源性荧光团(如NADH、FAD)的自发荧光,揭示细胞代谢状态。NADH荧光强度增加常指示缺氧,是肿瘤代谢标志。时间分辨FS进一步通过荧光寿命区分游离与蛋白结合NADH,提升诊断精度。
多模态光学系统设计与集成
文章重点介绍了两种核心光学诊断系统:荧光与漫反射光谱(FS/DRS)系统和时间分辨荧光光谱(TRFS)系统。前者通过紫外(365 nm)和可见光(450 nm)激光激发内源性荧光团(如NADH、FAD),并结合宽带光源分析组织散射特性;后者专注于NADH荧光寿命测量,以区分游离与蛋白结合状态,反映细胞代谢 状态。系统均采用Y型多光纤探针,兼容标准穿刺针,实现光传输与信号采集的双向功能。
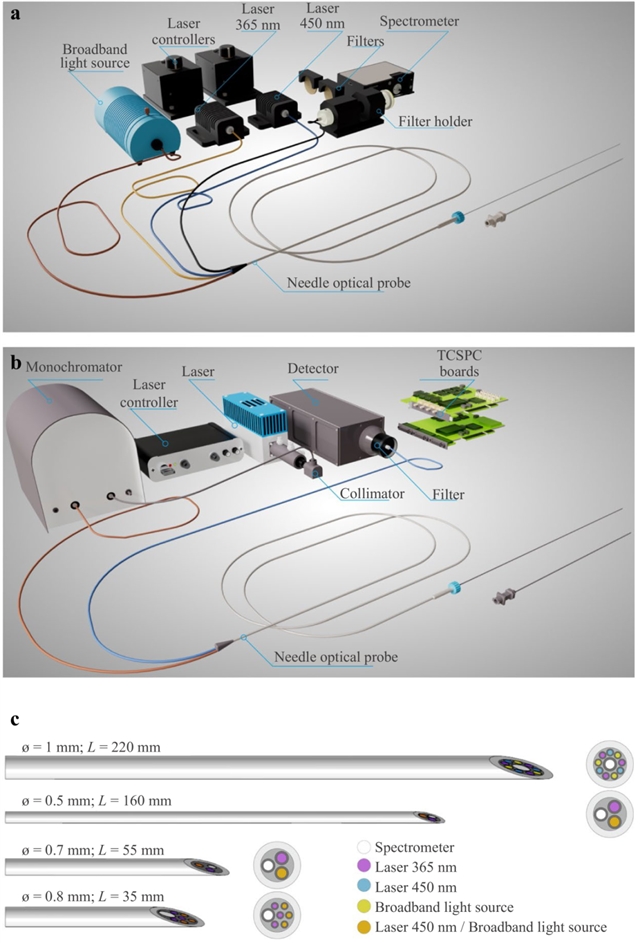
图1:术中光学诊断系统
探针设计注重小型化与可消毒性,适应不同器官(如肝脏、胰腺、乳腺)的解剖需求。
光学系统校准
为确保光学信号的可靠性,研究团队通过标准溶液测试了系统的浓度响应曲线。对于NADH荧光,而对于FAD,在0.5 mM及以上浓度时,信号强度会逐渐增加,随后出现停滞;胆红素在0.3 mM以上则因浓度淬灭导致信号衰减。时间分辨系统进一步验证了MF445滤光片可有效屏蔽FAD干扰,专用于NADH寿命测量(420 ps),且寿命参数在生理浓度范围内不受影响,突出了其对蛋白结合状态的敏感性。
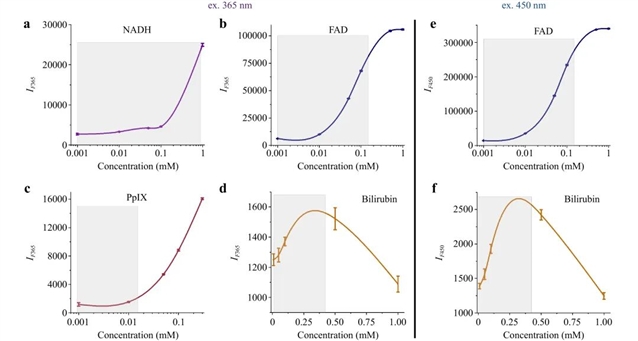
图2:不同浓度下内源性荧光团的荧光强度
临床应用:乳腺癌代谢状态评估
在21例乳腺肿瘤患者(13例恶性、8例良性)的临床试验中,FS/DRS系统通过365 nm激发荧光和漫反射光谱,揭示了恶性肿瘤的显著低氧特征:组织饱和度(StO2)低于良性组(p<0.05),且恶性区域荧光强度更高,反映NADH积累和胶原降解。
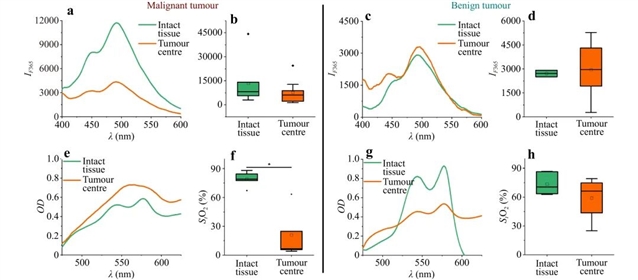
图3:乳腺癌肿瘤代谢状态光谱对比
肝脏活检导航
针对肝脏PNB,FS/DRS多模态系统实现了肿瘤与健康实质的实时区分。FS数据显示肿瘤区域荧光峰值红移(因胆汁滤光效应),DRS结合神经网络计算的StO2在肿瘤中更高(源于动脉血供为主)。
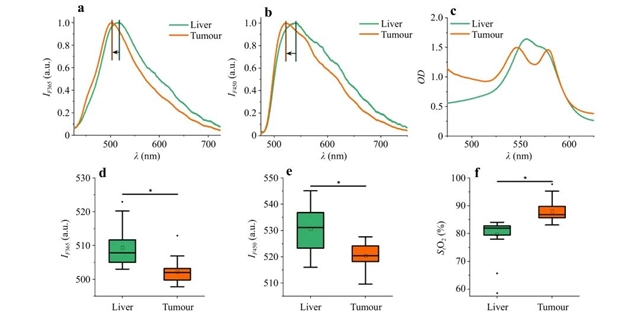
图4:肝脏健康与肿瘤组织光谱特征
总结
光学经皮穿刺活检结合现有检查技术,可以提高治疗性肿瘤病理形态术前诊断的效率。通过多模态光谱技术,为肿瘤诊断提供了实时、在体功能学评估的新维度。未来,随着探头微型化和算法精准化,该技术有望成为术中标准辅助工具,提升肿瘤早期诊断和治疗策略个性化水平。(来源:先进制造微信公众号)
相关论文信息:https://doi.org/10.37188/lam.2025.072
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。