对绝大多数动物而言,睡眠不可或缺。人类一生要花费约1/3的时间用于睡眠,而睡眠不足会导致多种健康问题,例如引发炎症或慢性免疫系统疾病。动物实验表明,长时间睡眠剥夺会导致其个体死亡。然而,哺乳动物的睡眠如何调控免疫系统,睡眠不足又如何带来负面的健康影响,其机制尚未厘清。
2023年11月27日,北京生命科学研究所/清华大学生物医学交叉研究院张二荃实验室在Cell上在线发表了题为Prolonged sleep deprivation induces a cytokine storm-like syndrome in mammals的研究论文。该研究发现小鼠长时间睡眠剥夺将导致严重细胞因子风暴,并且揭示了睡眠剥夺导致外周免疫反应的神经分子机制——脑源PGD2/DP1信号通路。
在此研究课题中,张二荃实验室研究人员首创了一套适用于小鼠的定名为“Curling Prevention by Water”(CPW)的睡眠剥夺系统(图一),通过脑电图/肌电图(EEG/EMG)记录实验组小鼠和对照组小鼠的睡眠/觉醒情况,确认该系统可以持续剥夺小鼠95%以上的睡眠。该系统相较于传统的实验动物转杆睡眠剥夺系统(Stand Alone Sleep Deprivation,SASD),可以在不引入更多环境刺激和保证实验通量的基础上极大提高睡眠剥夺效率,从而帮助研究人员可以观察到长时间睡眠剥夺后对哺乳动物带来的生理后果。
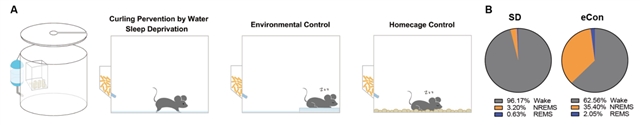
图一 Curling Prevention by Water睡眠剥夺系统
哈佛医学院的Rogulja实验室于2020年在Cell上发表以果蝇为研究对象,研究睡眠剥夺对动物产生的生理后果。他们发现睡眠剥夺的果蝇在肠道中积累了大量活性氧(ROS),从而显著缩短了睡眠剥夺果蝇的寿命。尽管他们也在睡眠剥夺的小鼠中发现,其肠道ROS含量相较于对照组小鼠显著上升,但并未发现睡眠剥夺会导致小鼠死亡,因而高等的如哺乳动物中是否存在类似的现象、其可能的作用机制仍不明确。
本实验中,张二荃实验室研究人员发现小鼠肠道ROS的积累与小鼠在睡眠剥夺后免疫反应强度相关,这说明了ROS产生在免疫激活反应的下游,而非上游;更重要的是,为小鼠提供N-乙酰半胱氨酸(NAC)和硫辛酸(lipoic acid)等抗氧化剂,并不能缓解小鼠睡眠剥夺致死的现象,这些都说明不能把果蝇睡眠剥夺致死的机制简单地推广到小鼠:虽然哺乳动物中长时间完全地睡眠剥夺也会致死,但致死原因与肠道ROS积累无关(既非充分也非必要条件)。
研究人员应用CPW系统对小鼠进行长时间睡眠剥夺时发现,对小鼠进行4天连续睡眠剥夺后,高达70%以上小鼠会死于严重的多器官衰竭。在睡眠剥夺过程中,小鼠血液中的促炎性的细胞因子(如IL-6和IL-17A)和趋化因子(如CXCL1和CXCL2)迅速积累,并将中性粒细胞从骨髓招募到循环系统中,从而导致小鼠出现中性粒细胞增多症。随着促炎性的细胞因子与趋化因子的持续性积累,小鼠出现由细胞因子风暴诱发的多器官功能障碍综合征(multiple organ dysregulation syndrome,MODS),最终导致小鼠的死亡。
睡眠不足导致的炎症反应,一般都会被解释为免疫力下降,进而招致的外界细菌或病毒感染。但为了厘清到底是免疫能力减弱,还是反过来的免疫反应过强导致的个体死亡,研究人员做了以下实验:一是在睡眠剥夺过程中,为小鼠提供抗细胞因子风暴药物能够缓和睡眠剥夺导致的免疫反应并延长小鼠的存活时间。二是将野生型小鼠替换为免疫缺陷品系(M-NSG)小鼠。如果是因为免疫力弱而由外界病原体感染导致死亡的话,M-NSG小鼠预期应该会更快地死亡。但事实上,对这种小鼠进行长达一周的睡眠剥夺都不会有个体死亡。
以上实验说明了不睡觉导致的死亡真正原因是免疫系统的过度激活(这与引发人体新冠重症的“细胞因子风暴”类似)。
除此之外,为了研究睡眠剥夺如何调控免疫反应,研究人员首先探究睡眠剥夺如何影响大脑神经系统的功能。研究人员发现睡眠剥夺导致的免疫反应并非通过大脑向外周的直接神经投射进行调控,而是通过大脑产生的特定分子释放到外周循环系统进而诱发的。睡眠剥夺后,小鼠的血脑屏障的主动外排(active efflux)活动持续显著增强。血脑屏障的主动外排活动由ABC转运受体介导,而这其中,通过药物和抑制ABCC家族转运受体能够缓和睡眠剥夺小鼠体内的免疫反应并且延长睡眠剥夺小鼠的存活时间。因而,研究人员推断睡眠剥夺导致的免疫反应由ABCC转运受体的某种底物介导;在睡眠剥夺过程中,随着血脑屏障主动外排活动从大脑转运到外周,进而引起免疫反应。
应用北京大学李毓龙实验室最新开发的GRAB(GPCR activation-based)探针,研究人员发现,睡眠剥夺后PGD2(前列腺素D2)在大脑内积累显著增加。同时,研究人员还应用UPLC-MS质谱检测到循环系统中PGD2相对稳定的代谢物Tetranor-PGDM含量也显著增加。为进一步验证PGD2在睡眠剥夺后的转运情况,研究人员使用3H标记的PGD2进行了小鼠活体血脑屏障主动外排指数BEI(BBB Efflux Index)检测,发现睡眠剥夺后PGD2转运到外周循环系统的速度明显提高。
研究人员使用遗传学手段验证PGD2在睡眠剥夺导致的免疫反应中发挥的核心作用:分别对脑内PGD2合成酶(包括全身敲除的Ptgds-/-、和应用脑内嵌合基因敲除技术获得的PtgdsBKO),以及将由脑内PGD2 efflux出来的特异性转运受体Abcc4-/-小鼠,进行睡眠剥夺,发现这些遗传突变鼠都能够显著降低诱发的炎症反应和延长小鼠存活时间。最后,研究人员发现静脉注射PGD2受体(DP1)激动剂能够诱发正常小鼠出现与睡眠剥夺小鼠类似的中性粒细胞增多症;同时,在睡眠剥夺过程中,如果为小鼠提供DP1拮抗剂,则能显著缓和小鼠因睡眠剥夺导致的炎症反应。这些结果也印证了睡眠剥夺导致的免疫激活反应依赖于从脑源的PGD2到外周器官DP1的信号通路(图二)。
该研究不仅为解释和解决睡眠不足导致的健康问题奠定了基础,而且有助于深入理解睡眠如何与其他生物学过程相互作用,从而进一步阐释睡眠的功能与意义。
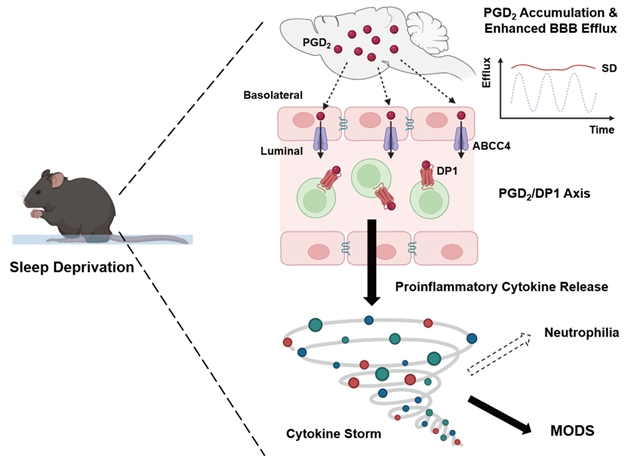
图二 睡眠剥夺导致细胞因子风暴的通路模型
张二荃实验室的桑迪、林可腾,以及北京大学李毓龙实验室的杨旖旎为本文的共同第一作者,张二荃博士为通讯作者。其他作者还包括张二荃实验室的冉光地和陈晨,李毓龙实验室的李柏翰,罗敏敏实验室已毕业博士生卢立辉,他们在各项实验操作中做出了重要贡献;北京生命科学研究所的刘清华博士、李祺博士、马燕博士,北京大学李毓龙博士、刘志博博士、崔希洋博士,北京脑科学与类脑研究所的罗敏敏博士,新桥医院的吕胜青博士等也参与了此项课题。
本课题的研究经费受中国科技部、国家自然科学基金委、北京市政府和清华大学支持。(来源:科学网)
相关论文信息:https://doi.org/10.1016/j.cell.2023.10.025