北京时间3月4日, 国际学术期刊《自然》以Research Article形式在线发表了上海交通大学医学院上海市免疫学研究所苏冰教授课题组的研究工作——"MAP3K2-regulated intestinal stromal cells define a distinct stem cell niche”。该研究首次发现肠道干细胞底部存在一类被称为MRISC的新型肠道间质细胞(图1)。该研究结合单细胞测序、ATAC测序、报告基因小鼠、体外肠道类器官共培养体系、以及肠道间质细胞原位注射等技术,系统揭示了MRISC细胞在肠道炎症和损伤过程中通过特异调控肠道干细胞微环境的Rspo1-WNT信号参与肠道上皮组织损伤修复的作用和机理,为肠道修复和再生及疾病临床治疗研究提供了新思路。
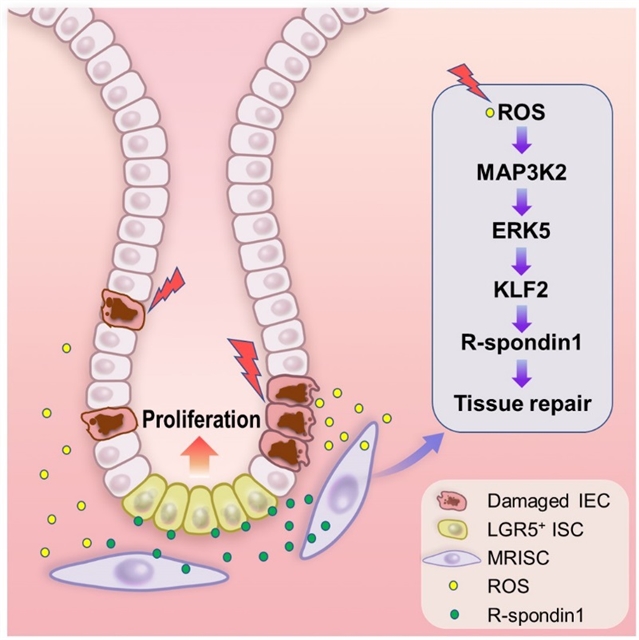
图1. Working model。肠道干细胞底部的MRISC肠道间质细胞通过感受炎症损伤诱导的ROS信号,激活MAP3K2-ERK5-KLF2信号通路,上调R-spondin1表达,从而提高肠道干细胞的Wnt信号,促进其增殖加强其修复肠道上皮损伤的功能。
炎症和损伤通常能迅速激发肠道干细胞增殖促进组织修复再生。肠道间质细胞是肠道微环境组分中的重要成员,在FGF、TGF-β、Hedgehog与PDGF等信号调控下肠道间质细胞可分化为多种复杂群体,它们通过与淋巴细胞、髓系细胞、上皮细胞、和神经细胞的相互作用,协同调控肠道稳态以及上皮干细胞的功能。借助谱系示踪技术,肠道间质细胞的功能异质性正在逐步得到阐明:不同的肠道间质细胞群体通过不同生长因子与细胞因子的分泌可有效调节肠道稳态与上皮结构完整性。然而,至今仍然不清楚这些新发现的肠道间质细胞群体在肠道稳态维持与疾病条件下,如何精细调控肠道功能。
肠道间质细胞长期以来被认为是一类相对简单缺乏异质性的功能细胞。它们都表达CD140a、Col1a2、Vimentin等少数几个标志物,目前仍然缺乏精细研究其组织空间分布和亚群的工具。近年来单细胞测序技术快速发展,揭示了肠道间质细胞是一大类认知较少、异常复杂且具高度异质性的间质细胞(Cell,2018)。Foxl1+特洛细胞(Nature,2018)及CD81+滋养细胞(Cell Stem Cell,2020)的发现,提示肠道可能存在多种分化不同且功能特异的肠道间质细胞亚群。目前领域里对不同肠道间质细胞亚群的特征、空间分布、它们在组织损伤修复中的潜在功能、以及调节的细胞和分子机制仍知之甚少。因此对新型肠道间质细胞亚群的身份鉴定,上游刺激信号的发现,以及中下游转录和表观遗传调控通路的阐明已成为间质细胞领域最基础和重要的科学问题。肠道上皮发育分化依赖于肠道微环境中的Wnt-BMP对冲信号的浓度梯度,但Wnt激活剂R-spondins梯度形成的调控机制仍然不清楚。尽管已知肠道间质细胞是R-spondins的主要来源,但肠道“干细胞巢”(Stem Cell Niche)中R-spondins的细胞来源仍有诸多争议。同时,R-spondin1蛋白的转录、翻译以及释放的调控机理也不明了。
苏冰教授课题组的这项研究首先发现,进化保守的Thr/Ser蛋白激酶MAP3K2对DSS诱导的小鼠肠炎能通过维持损伤肠道中Lgr5+干细胞的数量和功能起到关键的保护作用。MAP3K2是一个多器官组成性表达的丝/苏氨酸蛋白激酶。在分子机制上,研究人员发现Map3k2通过响应DSS诱导的损伤信号上调R-spondin1的表达,介导MAPK信号与Wnt信号之间的互作;并确认肠道间质细胞是肠道炎症损伤信号上调R-spondin1表达的关键细胞。为了精确确定受MAP3K2调控的肠道间质细胞的特征和功能,研究人员利用单细胞测序技术发现并分离得到一群带有CD90+CD81+CD34+CD138-特征的肠道间质细胞,并命名为MRISC。通过肠道类器官共培养以及肠道原位细胞注射实验,课题组成功证明了MRISC具有对肠道干细胞特异的调节功能。并通过构建全新的Rspo1-tdTomato报告基因小鼠,揭示MRISC定位于肠道“干细胞巢”的下方(图2)。
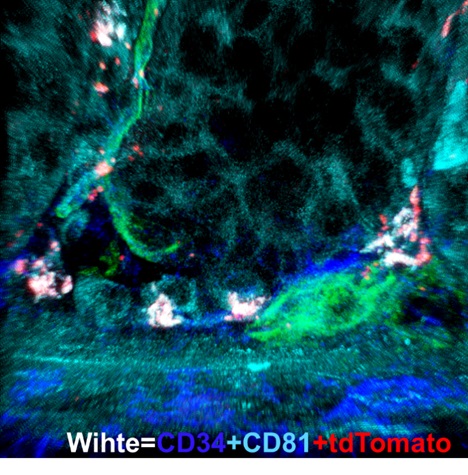
图2. MRISC位于肠道干细胞Niche底部。图片是Rspo1-tdTomato小鼠结肠通过免疫荧光染色的方法显示MRISC(CD34+CD81+tdTomato+)(白色)位于肠道隐窝干细胞底部。
为进一步研究MAP3K2特异调控新型肠道间质细胞MRISC中R-spondin1表达的分子机制并探索其表观遗传的特征,研究人员获取了不同肠道间质细胞的ATAC-Seq数据,揭示MRISC有着与其他间质细胞非常不同的表观遗传调控特征(图3),并发现MRISC的核心转录调控因子KLF2直接受MAP3K2信号调控。后续的体外实验进一步发现了“活性氧(ROS)-MAP3K2-ERK5-KLF2”这一全新的诱导R-spondin1产生分子通路。通过同人肠道单细胞测序数据的比较分析,研究人员也找到了与小鼠MRISC对应的人的MRISC细胞,并猜测其同样可能参与调控肠道炎症。
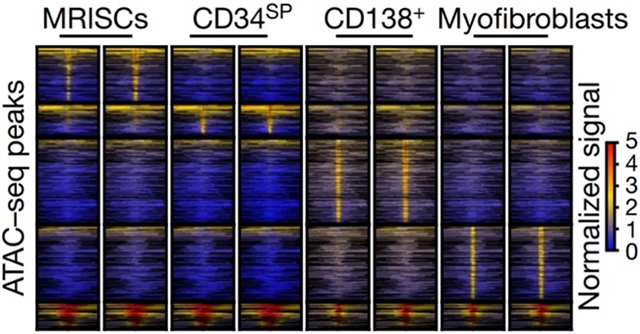
图3. MRISC具有独特的表观遗传特征。图片显示小鼠结肠MRISC,CD34SP,CD138+,Myofibroblast间质细胞ATAC-seq的热图结果,显示同其它肠道间质细胞比较MRISC具有独特的染色体开放区域。
本文借MRISC的发现对以上皮干细胞微环境为靶点的炎症性肠病治疗方案具有重要的指导意义,同时,新建立的间质细胞示踪模型也将极大促进肠道微环境研究领域的发展。但更为重要的是,通过对MRISC以及其它肠道间质细胞亚群的鉴定,让我们意识到间质细胞可能就像CD4+T淋巴细胞一样,包含诸如参与I、II、III型免疫反应的效应T细胞,调节性T细胞以及滤泡辅助性T细胞等多个辅助性CD4+T细胞亚群,这些CD4+T细胞亚群的发现推动了T细胞领域近四十年的深入研究。与此相类似的是,髓系中的巨噬细胞亚群,尤其是近年来,针对胚胎来源组织驻留和成体骨髓来源巨噬细胞在各主要器官迥然不同的组织分布与调节功能的研究正如火如荼的开展。因此,MRISC以及其它主要间质细胞亚群标记系统的建立必将极大推动间质细胞在免疫、神经、肿瘤、代谢、衰老等生命科学重要过程中功能的阐释;而人体内相对应的间质细胞主要亚群的发现和鉴定将同样推动其在人类疾病如肠道肿瘤、食物过敏等炎症诱导疾病中作用的解析。
这项研究是苏冰教授团队通力协作的成果,也是苏冰教授离开耶鲁大学回国后加入上海交通大学医学院开展的第一个课题。课题组伍宁波博士和孙宏翔博士是该论文的共同第一作者。(来源:科学网)
相关论文信息:https://doi.org/10.1038/s41586-021-03283-y