4月14日,记者从香港科技大学获悉,该校科研人员与北京大学化学与分子工程学院教授邹鹏团队合作,研发出一种名为CarGAP的新型化学-光遗传学工具。该工具利用维生素B12与绿光(570 nm)协同作用,实现对间隙连接通道的可逆、精准调控,为细胞间直接通讯提供了高时空分辨的操控手段。相关成果发表于美国《国家科学院院刊》。
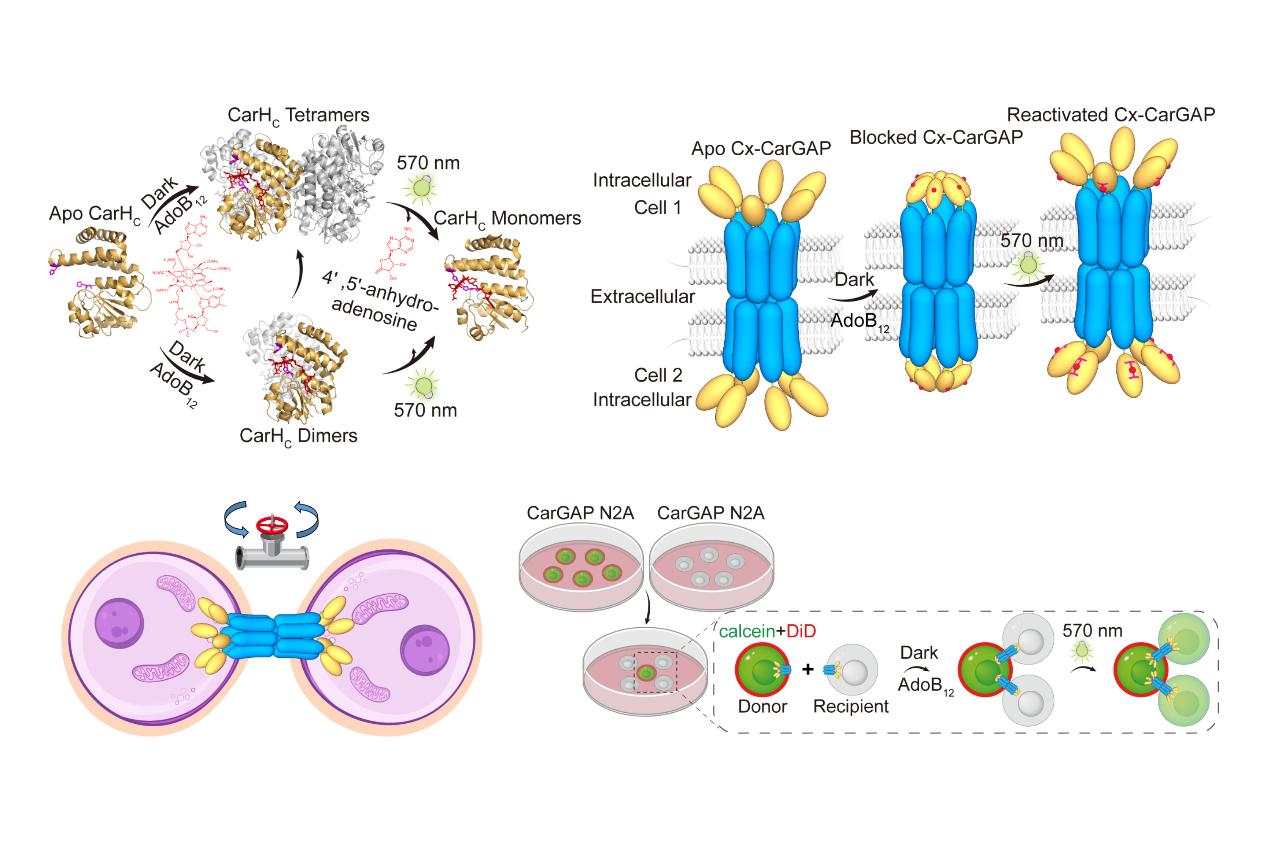 哺乳类动物细胞中Connexin CarGAP的设计原理。研究团队供图
哺乳类动物细胞中Connexin CarGAP的设计原理。研究团队供图
间隙连接是细胞间直接传递离子、第二信使及小分子的关键通道,广泛参与心跳节律、神经活动等核心生理过程。其功能异常与心血管疾病、发育障碍及癌症等密切相关。传统研究方法中,基因敲除不可逆且缺乏时效性,化学抑制剂则特异性不足且可能产生细胞毒性。因此,构建一种可逆、低副作用、时空精准的调控系统,成为细胞与神经生物学领域的重要需求。
研究团队将间隙连接蛋白(包括脊椎动物中的连接蛋白connexins与无脊椎动物中的innexins)与来自细菌的CarHC光敏维生素B12结合域融合,构建了CarGAP系统。在黑暗条件下,添加维生素B12(AdoB12)可诱导CarHC结构域寡聚化,从而物理性封闭通道;而570 nm绿光照射则促使寡聚体解聚,恢复通道开放。该设计实现了“维生素关闭、光照开启”的双模态可逆控制。
研究团队在多个层面验证了CarGAP的功能:在哺乳动物细胞中,成功调控了荧光染料及免疫信号分子2′3′-cGAMP的细胞间传递,并借助远红电压探针NAVI-Cy5,光学记录了光照后细胞间电耦合的恢复过程。在活体果蝇卵巢模型中,CarGAP可阻断干细胞与微环境细胞间cAMP信号分子的流动,并在光照后恢复其传递,进而影响干细胞行为与卵子发育。
论文共同通讯作者、香港科技大学教授孙飞表示,CarGAP实现了对细胞间基础通讯模式的远程精准操控,结合维生素B12的高生物兼容性与光遗传学的时空精准性,为研究胚胎发育、神经环路及肿瘤微环境中的细胞协同行为提供了有力工具,亦对理解疾病机制与推动再生医学研究具有重要意义。
相关论文信息:https://doi.org/10.1073/pnas.2518037122
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。