上海交通大学基础医学院、上海市免疫学研究所Svetoslav Chakarov团队联合国内外科研团队,首次揭示定居于独特组织微环境的巨噬细胞具有协调脂肪组织稳态的全新功能,阐明了其在调控肥胖易感性中的关键作用。8月29日,相关研究在线发表于《科学》。
肥胖过程中的脂肪组织扩张取决于脂肪干细胞(ASCs)的精准调控。尽管肥胖脂肪中炎症性巨噬细胞的作用已被充分阐释,但常驻巨噬细胞亚群如何影响瘦体状态下ASC分化的机制尚未阐明。
研究人员发现了一类稀有的CD209b+LYVE1+隔膜巨噬细胞(sATMs),它们特异性定位于白色脂肪组织(WAT)的小叶隔膜内——这是一个富含胶原蛋白与透明质酸的微环境,同时也是CD26+多能ASCs的聚集区域。这类巨噬细胞主要源于胚胎发育阶段,并能长期维持其生态位特性。
通过一系列创新的小鼠敲除模型和巨噬细胞特异性TGFβ1基因敲除,研究人员证明sATMs对于维持ASCs的白色成脂命运至关重要。敲除sATMs导致产热性米色脂肪细胞分化显著增加、葡萄糖代谢改善,并对高脂饮食诱导的肥胖产生保护作用。从机制上讲,sATMs向CD26+ ASCs传递TGFβ1信号,促进其向白色脂肪细胞谱系定向。该信号的缺失会重编程干细胞命运,增强产热作用,并提升全身能量消耗。
本研究揭示脂肪隔膜不仅是结构分隔带,更是一个空间受限的调控性生态位,免疫细胞与祖细胞在此发生精密相互作用。这一发现与再生组织中类似的生态位范式形成呼应,揭示了亚组织水平巨噬细胞在指导局部干细胞命运方面具有更广泛的生物学功能。
重要的是,这些发现在人类生物学中同样得到验证。通过运用单细胞RNA测序(scRNA-seq)、CODEX多重成像技术和抗体谱分析,研究人员鉴定出具有相似表型与空间定位的人类隔膜巨噬细胞(hsATMs)。这些巨噬细胞与人类CD26+ ASCs紧密相邻,并表现出活跃的TGFβ1信号传导活动,这表明存在一种进化保守的调控机制,可能主导着人类脂肪组织可塑性及代谢健康的维持。
本研究有望为增强能量消耗、促进白色脂肪组织米色化、防治肥胖及相关代谢疾病开辟新的治疗途径。人类体内保守存在的隔膜巨噬细胞-干细胞功能单元的证实,进一步强化了这一发现的转化医学价值。
?
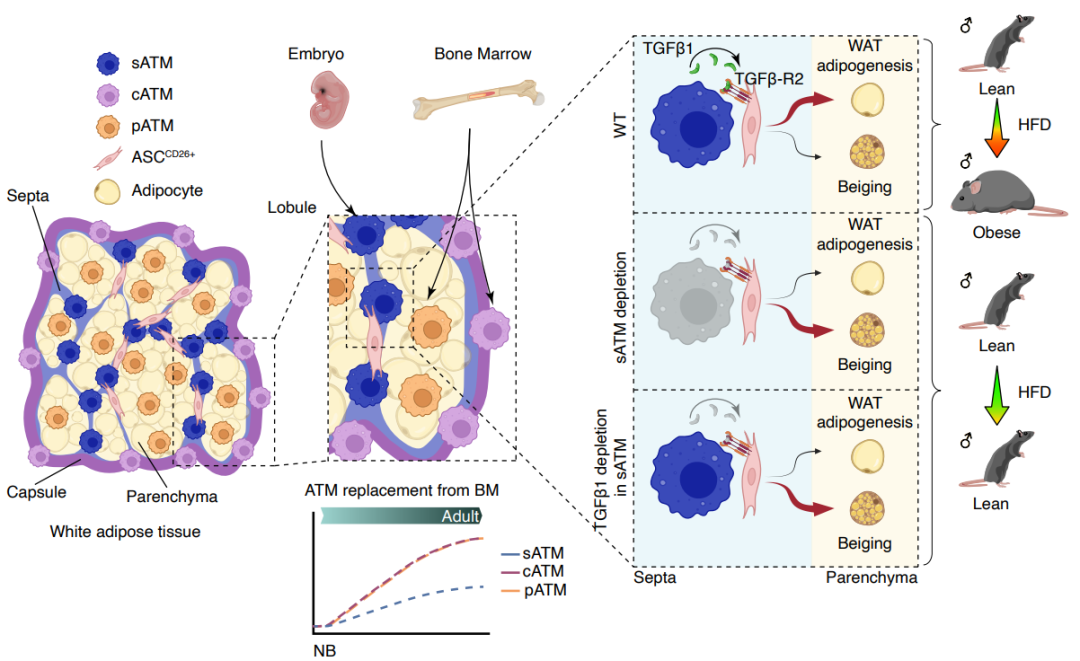 论文插图
论文插图
?
相关论文信息:https://doi.org/10.1126/science.adg1128
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。