近日,来自南昌大学第一附属医院、复旦大学、摩方精密、昆明医科大学等联合研究团队,成功研发出一款新型类器官培养平台,可用于培养厘米级肿瘤或器官源。该类器官芯片由摩方精密面投影微立体光刻(PμSL)技术3D打印制备,内部集成微米级仿生微血管网络,并引入灌注装置以模拟血流动力学特征,在实现营养液持续供给与全浸没培养的同时,有效克服了类器官因营养获取不足导致的尺寸受限难题。这一研发成果不仅使体外构建大尺度肿瘤及正常组织模型成为可能,还为药效毒理评估与类器官标准化生产提供了创新解决方案。
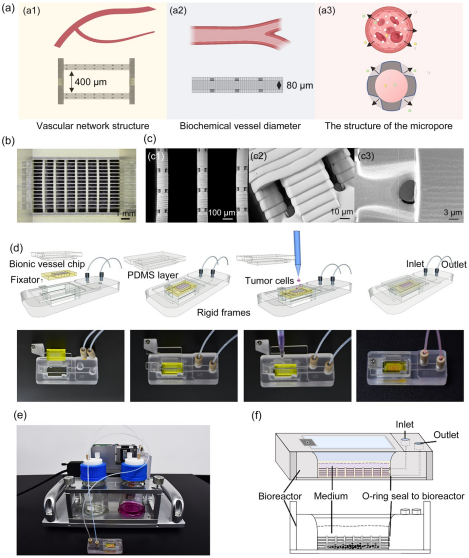
图.利用摩方微纳3D打印技术制造带有血管的类器官芯片
类器官(Organoid)和器官芯片(Organs-on-chips)作为体外培养的微型器官模型,近十年已在药物测试和疾病研究中崭露头角。然而其发展始终受制于一个致命缺陷——缺乏血管网络,从而导致营养无法渗透至核心区域,无法模拟真实器官的代谢功能。
当然,更深层的问题在于制造工艺。微流控芯片的通道精度需达到10微米以下才能模拟毛细血管,但光刻等传统技术难以构建三维分支网络。而普通3D打印通常卡在50微米关口,细胞生长的空间囚笼由此形成。
01技术突破,微纳3D打印重构生命通道
微纳3D打印技术的出现,使微纳尺度制造跨入新纪元。摩方精密开发的microArch? S230A微纳3D打印系统,具备2微米超高光学精度,支持生物相容性树脂材料打印,能够实现中空管状网络的直接成型。以自研毛细血管器官芯片结构为例,整体尺寸为18 mm(L)x10 mm(W)x5 mm(H),结构内部共5层流道,每层有14行平行通道(尺寸为25μm),且每条通道上均有间隔300 μm的梯形界面小孔,孔径尺寸为7-10 μm,可进行细胞培养的舱内尺寸为10 mm(L)x6 mm(W)x2 mm(H)。

可有效解决器官芯片血管化网络构建、跨器官代谢模拟等关键制造难题,为构建具备临床预测价值的器官芯片提供更多可行性方案。
02创新应用,三大科研场景的重构
·3D打印血管化类器官芯片
为解决类器官技术缺乏复杂血管网络而导致的氧气及必需营养物质输送受限问题,来自南昌大学第一附属医院、复旦大学、摩方精密、昆明医科大学等联合研究团队成功开发出可培养厘米级肿瘤或器官源类器官的新型培养平台。相关成果以“Vascularized organoid-on-a-chip for centimeter-scale organoid cultivation”发表于著名期刊《Bio-Design and Manufacturing》上。
研究为模拟生理相关性更强的毛细血管网络,类器官芯片采用中空管状结构设计,单管道内径80μm、壁厚20μm,相邻通道间距400μm。每根通道周向均匀分布四组宽度<10μm的狭缝,沿管道轴向以300μm为间隔周期性排布。装置入口与出口直径均为0.75mm,整体由摩方精密microArch? S230 (光学精度:2μm)超高精度3D打印系统一体化成型制备而成。
研究团队成功构建了肺癌类器官、子宫内膜癌类器官和肾脏类器官,并实现体外培养周期突破30天,同时将组织尺寸扩展至厘米级。同时,精确复现药物反应机制,为新型基因治疗策略提供了创新平台,有望加速基因疗法临床转化并提升治疗效益。
论文链接:https://doi.org/10.1631/bdm.2400424
·乳腺癌细胞外渗检测芯片
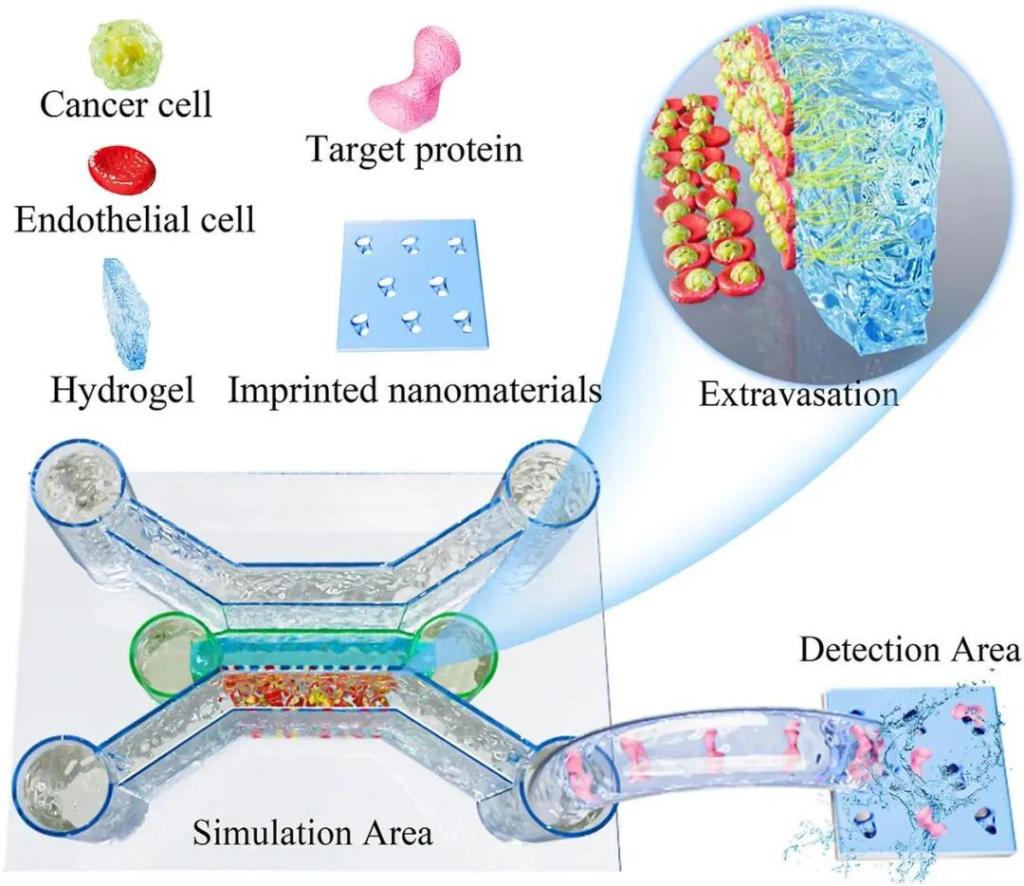
中国东南大学王著元教授团队提出了一种将3D打印器官微流控芯片与基于SERS的蛋白质印迹纳米材料(SPIN)相结合来研究体外外渗过程。该芯片由胶原凝胶通道和血管通道组成,其中依次注射人静脉内皮细胞和乳腺癌细胞以诱导外渗。实验团队通过比较两种乳腺癌细胞亚型 (MCF-7 和 MDA-MB-231),成功地通过荧光成像观察到了两种细胞之间外渗能力的差异。同时,由于分子印迹技术的高特异性和表面增强拉曼散射 (SERS) 的高灵敏度,SPINs 被用于实时分析复杂生物液中几种癌症分泌物(白细胞介素-6 和白细胞介素-8)的浓度。此外,实验模型表明,治疗药物对分泌物的下调可以抑制乳腺癌的外渗。
研究团队利用摩方nanoArch? P150(精度:25μm)3D打印系统制备模具后经翻模得到微流控芯片(通道高度为300、600μm,注射口直径为4mm),这种微流控模型将为癌症转移的基础研究,评估潜在药物的治疗效果提供新思路。
DOI:10.1002/adhm.202302104
·高精度3D打印微流控芯片的载药微球制造工艺
北京大学南昌创新研究院(以下简称“北大南昌院”)与重庆摩方精密科技有限公司联合共建的精密增材制造技术联合实验室(以下简称“实验室”),携手北京某研究院,在基于高精度3D打印微流控芯片技术的载药微球制备领域取得了重要技术突破。实验室利用摩方精密超高精度微纳3D打印系统,研发出了高通量、高均匀度载药微球制备的微流控芯片。
实验室自主设计研发出一款高通量、双乳化微流控芯片,该芯片采用模块化架构,由多个集成化微流控单元构成。每个微流控单元基于水包油包水(W/O/W)双乳化模板,可实现单乳化向双乳化体系的高效转化,精确制备W/O/W型微球,在药物递送系统和生物分析等领域具有重要应用价值。
为满足不同规模的生产需求,实验室还创新性地开发了多通道梯度化芯片系列,包括单、12、48、96及204通道等多种规格。其中,单、12通道芯片适用于实验室小规模探索性研究;48、96通道芯片可满足中等通量制备需求;204通道芯片则支持高通量规模化生产(图3)。这种梯度化的通道设计确保了实验精度,同时显著提升了制备效率,为微球的批量化生产搭建了稳固的技术平台。

可定制化设计微流控芯片
03未来挑战,生命蓝图的精密重绘
根据Markets And Markets统计显示,全球器官芯片市场到2029 年将达到631,073,000 美元。该市场的增长主要受到多种因素的推动,例如越来越重视无动物药物测试,以及制药和生物技术公司越来越多地采用器官芯片技术进行药物发现和开发。然而,由于当前器官芯片技术的可扩展性有限且通量低,该技术的使用仅限于临床前药物开发阶段。随着生物工程、材料工程、机械工程等多学科的融合,将进一步攻坚器官芯片制造技术,加速科技成果向产业化落地。
另外,政策支持同步加码,2021年,中国 “十四五” 重点研发专项便将 “类器官芯片关键技术” 列为核心攻关方向。今年4月,美国FDA新规计划逐步取消传统动物实验,转而采用实验室培养的类器官和器官芯片技术测试药物安全性。全球政策的转向不仅印证了芯片在模拟人体生理环境方面的科学公信力,更揭示了其在现代医学研究中的基础设施地位。摩方精密高精度微纳3D打印技术,正通过构建高通量、高精度、高性能生物芯片的制造能力,为疾病治疗、组织工程及新药开发等前沿领域持续输送创新动力。
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。