·首次成功构建了小鼠肝脏的高精度时空图谱,探索了肝脏的空间分子特征与损伤修复中的分子机制,为未来肝脏疾病的治疗提供了新思路。
在所有的器官中,肝脏可能是最“神秘”的一个。它不仅是最大的实体器官,包含最多的血液,具备器官中最强的再生能力,还担负着代谢、合成、消化、免疫等多种功能。
古代人曾认为肝代表着欲望、感情冲动和生命力本身。而在现代科学家们眼中,肝的生理机制则是在基因的引导下,多样的细胞进行功能性分化、表达与合作的结果。对于这些复杂的机制还有太多未解之谜。
随着基因测序、计算机等科学技术的发展,人们有望通过更加精准和深入的观测技术来探索这些谜题。2024年4月16日,杭州华大生命科学研究院与中国科学院分子细胞科学卓越创新中心主导,联合吉林大学、广州医科大学第五附属医院、山西医科大学、上海科技大学等国内外机构,在国际期刊《自然·遗传学》(Nature Genetics)发表了两篇研究成果,首次成功构建了小鼠肝脏的高精度时空图谱,探索了肝脏的空间分子特征与损伤修复中的分子机制,为未来肝脏疾病的治疗提供了新思路。
在华大自研的名为Stereo-seq时空组学技术的帮助下,研究人员们在纳米级分辨率上将肝脏细胞的空间信息与细胞基因等分子信息相结合,对肝脏进行了深层透视和建模。在其中的一项研究中,研究者们对小鼠的正常肝脏和70%切除之后的肝脏展开研究,揭示了小鼠稳态肝脏中的细胞类型、基因表达和微环境信号的空间特征,以及部分肝切除后对应的时空动态变化如何协调准确的肝再生。
在肝脏的不同区域中存在不同类型的细胞,它们在基因引导下分化,行使着不同的功能,并通过一系列机制相互协作。研究团队在肝脏的门静脉-中央静脉轴上解析了不同类型肝细胞的基因功能分布特征,并识别出一系列具有区域化分布的基因。
除此之外,团队还首次发现肝脏中存在约50-200微米的免疫微结构,对其进行定位并解析其中的免疫细胞组成,发现主要由T细胞和单核细胞组成。研究团队推测其可能是肝脏免疫响应的特殊机制,可协助肝脏抵御外源细菌或抗原。
在另一项研究中,研究人员们则在相同技术的帮助下观察胆汁淤积损伤后肝脏在自我修复时的分子过程。胆汁淤积是由于胆汁分泌及排泄障碍引起的,严重时可能导致胆囊炎、肝硬化、肝衰竭等系列疾病的发生。在发生这种损伤后,肝脏中的门静脉区肝细胞会重编程为肝祖样细胞(LPLC),为肝细胞的增殖作出贡献。在本研究中,科学家们观察了该过程中的损伤响应和微环境信号的时空动态变化特征。
现代科学如何理解肝脏功能?这两项研究将如何加深我们对肝脏疾病的认识?小鼠肝脏与人类肝脏有何区别?时空组学技术到底是什么?为回答这些问题,澎湃科技记者采访了研究团队中的多名研究者。

杭州华大生命科学研究院团队成员(左起)许江山、郝世杰、郭鹏程在做实验。受访者供图

中国科学院分子细胞科学卓越创新中心团队成员(左起)申屠欣怡、惠利健研究员、南海涛和吴柏华。受访者供图
【对话】
基因与细胞视角下的肝脏
澎湃科技:本次研究主要关注肝脏的哪些方面?
许江山(肝脏稳态-肝切除-再生时空图谱论文共同第一作者、杭州华大生命科学研究院副研究员):肝脏是人体内最重要的代谢器官之一,参与蛋白质、脂肪和碳水化合物等物质的代谢和调节。它具有解毒功能,能够清除体内的有害物质和代谢产物。此外,肝脏还能合成许多重要的生物活性物质,如白蛋白、胆固醇、胆汁酸和凝血因子等。
肝脏由其基本结构单元肝小叶组成,每个肝小叶类似于一个立体正六边形结构,中央静脉位于正六边形的中心,外周门静脉、肝动脉和胆管共同位于正六边形的外周顶点,血流从外围顶点流向中心。伴随着血流而来的氧气以及营养物质逐步被肝细胞吸收和代谢,形成了其独特的氧气和营养物质连续梯度分布现象,即肝脏分区(Liver zonation)。这一分区实际上也是肝脏细胞行使功能分工的基础,比如在中央静脉附近的肝细胞主要负责解毒功能,而周围的门静脉附近的肝细胞则主要负责白蛋白合成,这一分工也保证了肝脏功能的高效行使,同时也带来了疾病对不同区域肝细胞的易感性。
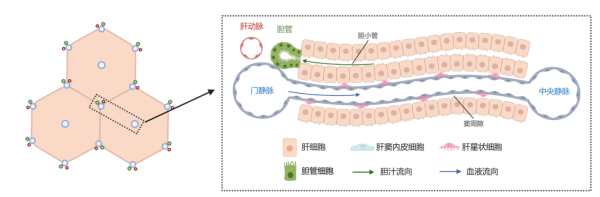
肝脏的基本结构。受访者供图
在本研究中,利用华大特有的时空组学技术Stereo-seq,我们精细解析了肝脏在稳态、损伤和再生情况下这一功能分区的时空动态,包括肝脏中的细胞类型组成及其空间分布情况、基因表达空间信息,判别哪些基因表达具有肝脏分区特征,并在此基础上探索了内在的基因网络和微环境特征。
澎湃科技:文章提到动物肝脏在组织稳态和扰动期间的协调响应机制尚不清楚,这为我们理解很多疾病造成了障碍。能否介绍一下已知理论中细胞之间大概是如何通讯并协同的?基因在里面发挥什么样的作用?为什么说理解这些现象能够加深我们对疾病的认知?
许江山:细胞间的通讯一般指的是细胞所处的微环境特性,包括了细胞通过分泌信号分子(如激素、生长因子)、直接接触(如巨噬细胞吞噬),或通过分泌细胞外基质间接参与微环境。
这些微环境因素和细胞相互作用,影响了细胞的功能和行为,比如信号分子可以扩散到周围细胞,并与细胞表面的受体相互作用,触发一系列信号传导途径,从而影响周围细胞的基因表达。不同的基因表达模式可以导致细胞的不同状态和功能,进而影响整个组织和器官的功能。
理解细胞间通讯和协同对于我们认知疾病非常重要。例如,在肝炎和肝纤维化中,炎症和纤维化信号的紊乱可以导致肝细胞和非肝细胞之间的通讯紊乱,进而导致炎症反应的持续激活和纤维化的过度沉积。类似地,在肝癌中,肝细胞和周边免疫细胞之间的通讯紊乱可能影响肿瘤的生长和转移。
澎湃科技:研究使用的是小鼠的肝脏,请问小鼠肝细胞与人类肝细胞相似吗?为什么不直接研究人体肝组织?
郝世杰(文章共同第一作者、杭州华大生命科学研究院博士研究生):肝脏从脊椎动物的共同祖先进化而来,当然也是哺乳类动物保守的器官,因此小鼠肝脏和人类肝脏的细胞组成和转录组特征是很相似的。
但人体研究受限于性别、饮食、年龄等个体差异,较难从中得到普适性规律。并且损伤、再生的相关研究也难以在人体上展开,因此,我们第一步先使用小鼠这一可控的模式动物进行研究。下一步,我们也会将研究拓展到人类肝脏的各种退行性状况,如肝疾病(如脂肪肝、纤维化)或衰老等情况。
空间组学技术:基因信息与空间信息的整合
澎湃科技:能否介绍一下空间组学技术以及本研究所使用的Stereo-seq技术?研究中所产生的图谱花了多长时间绘制?主要反映了什么信息?
上官顺成(肝脏稳态-肝切除-再生时空图谱论文共同第一作者、深圳华大生命科学研究院生化工程师):空间组学技术是一种用于研究组织或细胞内基因表达的方法,它结合了空间信息和转录组学分析。传统的转录组学技术通常只提供基因表达的整体信息,而无法提供细胞或组织内基因表达的空间分布信息。而空间转录组学技术通过将组织或细胞固定在其原始位置上,从而提供了基因表达的空间定位信息。这一技术的发展为研究人员提供了一种更全面、更准确地理解基因表达的方法。
本研究使用的Stereo-seq技术,使用的是华大自主研发的时空芯片。芯片上布满了数以亿计规则阵列式排布的DNA纳米球,每个纳米球之间相距500纳米(过去同类方法的精度在10 μm),每个球上都带有自己独特的标签,用来标注特定的空间位置信息。研究人员用带有位置信息的芯片,去结合新鲜组织冷冻切片,经过一系列步骤,将细胞中的基因捕获并扩增成核酸文库,并进行测序。再经过时空云平台的数据处理步骤,就能够将捕获的细胞实时基因表达信息和芯片上的空间位置信息一一对应,即得到了文中肝脏组织切片的时空转录图谱。
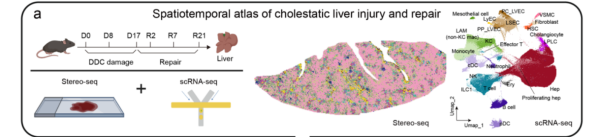
肝脏损伤和修复过程中的时空组学图谱。受访者供图
在本项研究中,数据的生成只花了短短不到1个月的时间,但是其中的生物学意义的解读花了较长的时间。这或许也是未来的趋势,生成数据的速度远超常规解读能力的发展,这可能是为什么我们需要人工智能的辅助。这些图谱以前所未有的数据深度与广度,解析了肝脏在稳态、损伤及再生中的时空变化。
澎湃科技:未来该技术有何发展方向?可以应用于别的器官吗?有什么局限?
赖毅维(文章共同通讯作者、杭州华大生命科学研究院副研究员):进一步,我们期望基于现有的研究,联合国内外肝脏领域的专家,一方面是把新的组学技术方法,应用到临床的肝脏代谢性疾病、癌症、衰老等问题上,去解决切实的临床问题,寻找疾病治疗和促进肝脏修复的新方法;另一方面则是围绕肝脏研究,发展新的检测技术,把目前的空间转录组学拓展到更全面的空间多维组学信息,并借助深度学习等全新的人工智能技术,最终构建数字化的肝脏模型。
该技术实际上已经运用于多个器官,比如我们利用时空组学技术Stereo-seq,与蒲慕明院士领衔的中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)合作,构建了食蟹猴全脑皮层的3D图谱;也正在与金凤实验室合作,期望在传统的病理学基础上,结合Stereo-seq发展数字病理学。未来,我们也希望能将这一技术从仅用于转录组分析,发展到可以同时捕获更多维度的信息。
“透视”肝脏:“高清相机”下的结构与机制
澎湃科技:能否介绍一下在肝脏稳态时空图谱中的多项新发现?
赖毅维:我们不但对肝细胞的基因梯度分布特征,也对内皮细胞、星状细胞做梯度分布的基因做了全面的鉴定,找到了大量未被报导具有这一特征的基因。
比如,在肝细胞中我们发现乙肝病毒的受体NTCP,在中央静脉周围的肝细胞中具有非常高的表达特征,这也解释了为什么乙肝病毒更多累积在中央静脉附近的肝细胞中。这也为我们设计针对肝脏疾病的治疗方法提供了参考。
澎湃科技:研究还首次发现肝脏中的一种免疫微结构,能否介绍一下?
郭鹏程(文章共同第一作者、杭州华大生命科学研究院博士后):我们认为这一微结构实际在过去不断地被观测到,但囿于形态学的观察,过去的研究并未能够总结其真实的特征。
借助时空组学技术Stereo-seq,我们不但发现这一在肝脏中随机分布的免疫微结构主要由T细胞和单核细胞组成,也发现这些细胞具有响应干扰素γ的下游基因特征。因此,我们猜测这一结构的存在能够维持肝脏快速响应外源病原体感染的能力,使得肝脏能够快速清除病原体。我们挖掘了过去的研究,发现类似的免疫微结构也在皮肤、结直肠中被鉴定发现。但其真正的功能及作用机制仍有待研究。
澎湃科技:研究还分析了肝脏内各种细胞在肝脏再生过程中的协调过程,并发现了一个炎症诱导调节因子TBL1XR1。能否介绍一下?
郭鹏程:TBL1XR1是一个转录因子(能够以序列特异性方式结合DNA 并且调节转录的蛋白质)的辅助因子,目前认为这个因子参与肝脏的脂肪分解代谢调控,它的功能丧失会导致严重的脂肪肝,也被证明与肝癌的发生存在关联。
在我们的研究中我们发现,TBL1XR1会在肝切除后被激活,如果我们干扰这个因子的激活,肝脏再生就会被抑制。因此我们认为TBL1XR1是一个促进肝再生至关重要的调控因子。这也为临床上通过调控TBL1XR1促进肝再生从而达到治疗肝脏疾病或肝癌提供了新的靶点。
澎湃科技:在胆汁淤积这项研究中,研究者发现胆管细胞在区域性损伤、肝细胞再生中担任信号“枢纽”。能否介绍一下这个疾病,并描述这些过程?
吴柏华(胆汁淤积损伤与再生时空图谱论文共同第一作者、中国科学院分子细胞科学卓越创新中心惠利健研究团队博士研究生):临床上胆汁淤积性疾病主要包括原发性胆汁性胆管炎(PBC)与原发性硬化性胆管炎(PSC)、胆道闭锁等。其主要的特点是在门静脉区域胆管细胞和肝细胞的损伤,伴随着免疫细胞的浸润以及纤维化,可逐渐发展至肝硬化、肝衰竭甚至死亡。胆汁淤积性疾病的发病机制目前尚不明确,临床有效治疗方案有限,因此迫切需要研究胆汁淤积症的发病机制,以确定新的治疗靶点。
胆汁淤积性疾病通常有着显著的门静脉区域多种免疫细胞和基质细胞的聚集,如此复杂多样的细胞聚集在门静脉区会强烈地影响微环境的损伤响应,如导致细胞杀伤和促进纤维化,从而加速胆汁淤积损伤。那么究竟是什么细胞主导了门静脉区域的免疫组分的重塑呢?
我们通过犹如一台“高清照相机”的高分辨空间组学技术,把损伤区域细胞的成分、表达都一一“拍”了下来。令我们意外的是,相比于传统在损伤下活跃的细胞类型,如巨噬细胞、成纤维细胞和肝窦内皮细胞胆管细胞等,胆管细胞在塑造门静脉区域的免疫细胞组分中起着更加突出的作用。具体来说,我们发现胆管细胞分泌一系列趋化因子,强烈吸引免疫细胞过来,同时影响着损伤区域中LAM(脂质相关巨噬细胞)的成熟。
除此之外,我们的数据也揭示了不同亚型的类肝前体细胞(LPLCs)。那么什么是LPLC呢?在之前的工作中,研究人员发现胆汁淤积损伤下的肝细胞会重编程为LPLC,这种状态的肝细胞具有部分肝祖细胞的特点,能够分化成肝细胞或胆管,这种属性转变是重要的,能够贡献肝脏再生。
但是什么因素使得一部分LPLC变成肝细胞,一部分变成胆管细胞呢?在我们组学鉴定的两类LPLC中,我们发现,LPLC2在表达谱上与胆管细胞相似。在空间上,我们又一次利用“高清照相机”捕捉到,与LPLC1相比,LPLC2在位置上更接近胆管区域,这暗示了LPLC2和胆管细胞之间可能存在相互作用。进一步分析发现,胆管细胞强烈地表达了与肝细胞向胆管转变相关的TGF家族因子。这就提示了胆管细胞与LPLC2向胆管谱系转变高度相关。
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。