|
|
|
|
|
iMicroCare十年合作,从最“小”处呵护健康 |
|
|
世界广袤,除了目之所及的山山水水、鱼虫花鸟,指缝间、鼻息处、每一寸肌肤、每一丝空气中,都存在万万千千的微生物。它们穿越数亿年时光,静静地生活,却深刻影响、改变、甚至塑造着我们的世界。
随着基因测序技术的发展,人们对微生物的研究进入组学与大数据时代。微生物组这一创新研究领域的进展,在人类健康护理、疾病诊治、工农业生产、生态保护环境治理、生物安全保障和生物资源等方面带来了革命性的变化。
中国科学院青岛生物能源与过程研究所(以下简称青岛能源所)单细胞中心于2010年开始布局微生物组相关研究,并与宝洁公司在基于人体共生菌群的“亚健康”诊断方法和“精准护理”策略等方面开展合作,取得了具有国际声誉和重要影响的研究成果。
双方在2016年6月共同启动为期五年的“皮肤、口腔及居住环境微生物组联合科学研究计划”——iMicroCare。该研究计划于2021年已启动第二期,旨在扩大微生物组指导下的家庭和个人护理产品研发方面的合作,宣传和推广微生态精准健康的理念。
创新引领,开发微生物组测序新技术
微生物无处不在,体格小且数量惊人。如何采集看不见的微生物,并进行下一步的分析,是开展微生物组研究的首要环节。
在iMicroCare支持下,研究人员开发了GermRadar病原雷达,集样品采集与数据分析于一体,能够提供环境、人体微生态健康评估的系统解决方案,实现多靶标、多指数的病原微生物检测。
“针对口腔和皮肤菌群,我们系统研究了不同部位菌群的结构和功能变化,通过分析微生物与宿主的互作模式,建立了基于微生物的新型患病风险评估、疾病诊断预警方法,并提出了通过早期精准护理,预防疾病的解决方案。”宝洁公司新加坡研发中心刘吉泉说。
技术的革新往往会带来颠覆性的成果。在微生物组研究中,微生物群落的物种解析主要依赖于扩增子测序和鸟枪法宏基因组测序。
针对这两种核心测序手段的瓶颈,研究人员联合开发了名为2bRAD-M的“简化宏基因组测序技术”,可对人体肠道、宫颈癌切片、室内环境中痕量、高度降解、严重污染的菌群样本进行种水平的细菌、古菌和真菌鉴定。这种技术有望作为一种共性的新手段,服务于人体与环境中“困难”菌群样品的高效解析。

2bRAD-M技术能高效地分析低生物量、高度降解或污染严重的微生物组(单细胞中心供图)
仪器突破,从单细胞精度解析微生物组的代谢功能
新方法、新技术与新仪器是微生物组科学发展的核心驱动力量。
“微生物组研究的思路目前正从监测菌群‘结构’向监测菌群‘功能/状态’转变、从细胞‘群体’精度向‘个体’精度转变。”单细胞中心主任徐健说。
元基因组手段能够全面地研究自然状况下微生物群落的结构和组成,却难以分辨与验证群落中细胞个体功能。单细胞功能分选、测序和培养技术能从根本上突破这一核心局限性。
“拉曼组”,是单细胞中心前期提出的创新概念,是指特定时空状态下,一个细胞群体的单细胞拉曼光谱的集合。
对于一个菌群,一个“元拉曼组”相当于单细胞精度、可快速、低成本测定与监控的“代谢表型组”,其变化可“全景式”地反映和表征其在代谢层面的“状态”与“功能”。进而,针对各种人体(胃粘膜、尿液等)或环境(土壤)菌群,运用其发明的RACS-Seq系统,单细胞中心首次建立了精确到一个细菌细胞的原位代谢功能以及对应高质量基因组(覆盖度可达99%)的解析能力,从而能够从最精准的水平回答菌群中“谁,在干什么”。

针对菌群的特定状态,元拉曼组揭示单细胞精度的代谢表型组(单细胞中心供图)
“元拉曼组与微流控的结合,让菌群中单个细胞的代谢功能分选以及后继的测序或培养成为可能,”单细胞中心研究员马波表示,“单细胞中心自主研发的CAST-R、FlowRACS、RACS-Seq、EasySort系列单细胞分析仪器,在快速、深入地解析和挖掘人体微生物组功能方面,具有突出的特色与优势。”
目前,这些仪器正通过青岛星赛生物科技有限公司进行产业化推广。

微生物组单细胞分析仪器系列(单细胞中心供图)
数据科学,赋能人体微生态健康监测新模态
测序技术的飞速发展与测序成本的持续降低,使得微生物组数据呈现井喷式增长。深入挖掘微生物组数据背后蕴含信息,能够更清晰地了解微生物组与共生环境/宿主之间精妙的互作关系,发挥菌群在人类健康、环境保护、工业生产方面的巨大潜力。
在微生物群落的结构和功能变化的分析中,联合研究团队提出多项指标参数,可支撑基于菌群的慢性疾病或生态灾害诊断。
徐健表示:“牙龈炎的菌群指数MiG、婴幼儿龋发病风险的菌群指数MiC、皮肤菌群健康指数MiSH、室内微生态环境指数MiBE、条件致病菌指数MIP等的提出,揭示了不同健康状态下人体/环境微生物组的显著不同,为相关疾病的监控、防治和相关护理品的评价、开发提供了崭新的思路。”
知其然,更要知其所以然。
宝洁公司和单细胞中心的联合攻关小组以牙龈炎发病过程为模式,开展了涵盖牙龈菌斑元基因组、元代谢组以及人体唾液细胞因子反应等一系列的动态多组学研究。
“我们发现在停止刷牙后的24—72小时内,牙龈即进入一个前所未知的亚健康(SoH)状态。在该状态下牙龈尚没有临床症状,但牙龈菌斑菌群结构、菌群代谢物组和唾液细胞因子却已发生急剧、显著的规律性变化。停止刷牙的第28天,牙龈菌斑菌群与健康牙龈菌斑相比老化了将近一岁。”刘吉泉说,“这项研究说明长期而持续有效的日常口腔护理,对于延缓牙龈衰老、保持牙周健康、促进全身健康,具有非同寻常的意义。”
对此,宝洁公司北京创新中心口腔微生物及临床部门技术总监王莉江也表达了同样的观点。
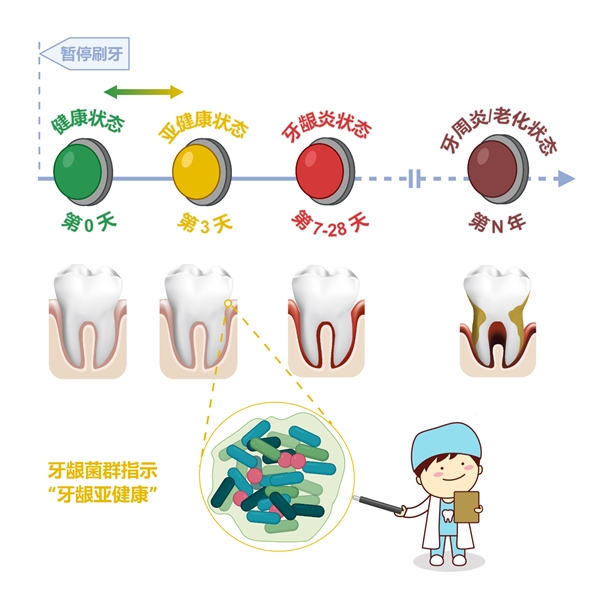
牙龈菌群指示“牙龈亚健康”状态(单细胞中心供图)
“面对海量的微生物组数据,为了实现大规模‘群落对群落’式的微生物组搜索和数据挖掘,我们开发了微生物组搜索引擎(MSE,http://mse.single-cell.cn)。”单细胞中心助理研究员荆功超表示,“MSE就像百度一样,输入微生物组数据,点击“回车”键,大规模、全局性的微生物组比对与搜索轻松实现。”
MSE在回答“是否健康”和“哪种风险”这两个问题上的准确率均超过80%,显著高于目前常用的机器学习算法,有效降低“漏诊”和“误诊”概率,并且在跨研究、跨测试人群、跨测序平台、样品污染等因素影响下的适应性和抗干扰能力等方面具有显著优势。
“目前MSE主要基于元基因组数据,元拉曼组不仅直接刻画菌群的代谢功能,且时空分辨率更高,因此基于这一新数据类型的MSE有望带来一系列全新的应用。”徐健补充道。
应用拓展,推动微生态服务人体与室内环境的精准健康
在口腔(牙龈)护理研究中,研究人员通过检测牙龈炎康复、发展、再康复过程中牙菌斑菌群结构和功能变化,发现根据MiG可以诊断牙龈炎的严重程度。这种非侵害性的诊断方法不依赖于牙医的主观判断。
同时,在口腔(牙齿)护理研究中,通过分析龈上牙菌斑和唾液中的菌群分布,利用MiC可在临床症状尚未出现时,提早六个月预测婴幼儿龋齿的发病,准确率达81%。同时,提出“口腔菌群年龄OMA”这一概念,可用于监测和预警儿童龋齿风险。
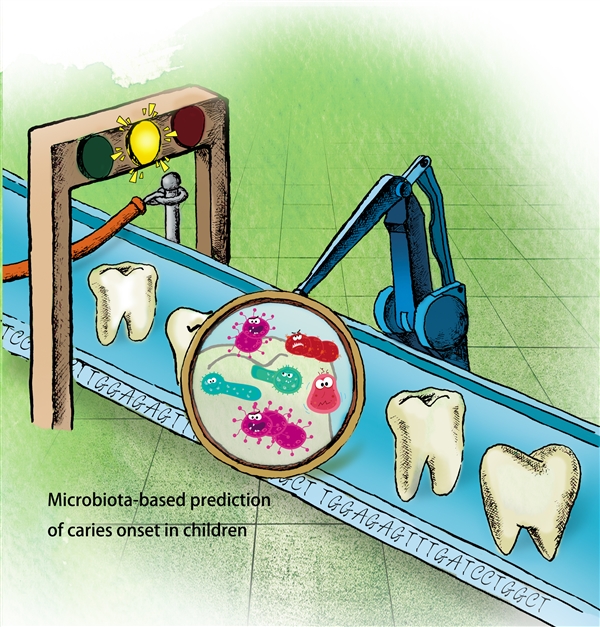
口腔菌群可预测新发性婴幼儿龋病(单细胞中心供图)
在皮肤护理研究中,研究人员通过采集全身多个部位的皮肤菌群,发现利用MiSH可以量化评价儿童皮肤健康状态,并指导特应性皮炎的精准护理和个体化用药。
基于MiSH开发的皮肤菌群健康在线数据库,将从微生态健康的角度,支撑业界的皮肤状态评估、皮肤护理产品评价和皮肤精准用药。
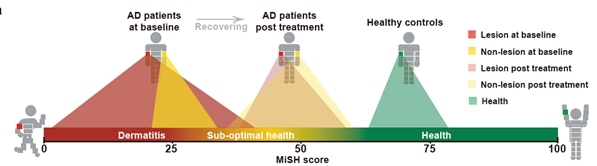
皮肤菌群健康指数MiSH可以量化评价儿童皮肤健康状态,并指导儿童湿疹(特应性皮炎)的精准护理和个体化用药(单细胞中心供图)
在由青岛能源所和宝洁集团舒肤佳家庭卫生研究院共同发起的室内环境评价研究中,研究人员通过采集室内菌群,发现利用MiBE可以诊断室内环境的致病菌存在状态,预警疾病风险,并提示室内环境的宜居性和清洁策略。此外,利用MIP可以评估菌群的总体风险程度,并推断出由条件致病菌所引起的疾病和人体易感器官等信息。
“最近,我们利用2bRAD-M技术首次在种水平分辨率上绘制幼儿园室内环境的微生物图谱,能为特定人群的疾病预防、健康管理等提供指导性意见。”宝洁公司新加坡研发中心Tzehau Lam说。

青岛能源所与宝洁公司合作描绘幼儿园微生物图谱(宝洁公司供图)
十年合作初心不改,专注微生态研究助力健康生活。
宝洁公司与青岛能源所在中科院—宝洁创新合作框架iMicroCare支持下,将持续推进全球水平的新一代微生物开放式创新平台建设,不断拓展在人体微生物组功能快检、环境微生物组与人体健康、元拉曼组技术、微生态大数据挖掘等领域的合作研究,共同为人类健康护理事业的发展贡献科学力量。
发表论文:
-
TzeHau Lam, Dillon Chew, Helen Zhao, Pengfei Zhu, Lili Zhang, Yajie Dai, Jiquan Liu*, Jian Xu*. Species-resolved metagenomics of kindergarten microbiomes reveal microbial admixture within sites and potential microbial hazards. Frontiers in Microbiology 2022, 13:871017. PubMed
-
Zheng Sun#, Xudong Liu#, Gongchao Jing, Yuzhu Chen, Shuaiming Jiang, Meng Zhang, Jiquan Liu, Jian Xu and Xiaoquan Su*. Comprehensive understanding to the public health risk of environmental microbes via a microbiome-based index. Journal of Genetics and Genomics 2022, S1673-8527(22)00002-9. PubMed
-
Zheng Sun#, Shi Huang*#, Pengfei Zhu, Lam Tzehau, Helen Zhao, Jia Lv, Rongchao Zhang, Lisha Zhou, Qianya Niu, Xiuping Wang, Meng Zhang, Gongchao Jing, Zhenmin Bao, Jiquan Liu, Shi Wang*, Jian Xu*. Species-resolved sequencing of low-biomass or degraded microbiomes using 2bRAD-M. Genome Biology 2022, 23(1):36. PubMed
-
Min Liu#, Pengfei Zhu#, Lei Zhang#, Yanhai Gong, Chen Wang, Lu Sun, Lili Wang, Rongze Chen, Yuli Mao, Xiaoting Fu, Lili Zhang, Teng Xu, Yuetong Ji, Quanjiang Dong, Bo Ma, Jianzhong Zhang*, Jian Xu*. Single-cell identification, drug susceptibility test, and whole-genome sequencing of Helicobacter pylori directly from gastric biopsy by Clinical Antimicrobial Susceptibility Test Ramanometry. Clinical Chemistry 2022. PubMed
-
Xiaoyan Jing#, Yanhai Gong#, Teng Xu#, Yu Meng, Xiao Han, Xiaolu Su, Jianmei Wang, Yuetong Ji, Yuandong Li, Zhongjun Jia, Bo Ma*, Jian Xu*. One-cell metabolic phenotyping and sequencing of soil microbiome by Raman-Activated Gravity-Driven Encapsulation (RAGE). mSystems 2021, 6(3):e0018121. PubMed
-
Shi Huang*, Tao He, Feng Yue, Xiujun Xu, Lijiang Wang, Pengfei Zhu, Fei Teng, Zheng Sun, Xiaohui Liu, Gongchao Jing, Xiaoquan Su, Lijian Jin, Jiquan Liu, Jian Xu*, Longitudinal multi-omics and microbiome meta-analysis identify an asymptomatic gingival state that links gingivitis, periodontitis and aging. mBio 2021, 12:e03281-20. PubMed
-
Tao He*, Shi Huang, Feng Yue, Lijiang Wang, Jiquan Liu, Jian Xu. A randomized, controlled comparison of a stannous-containing dentifrice for reducing gingival bleeding and balancing the oral microbiome relative to a positive control. American Journal of Dentistry 2021, 34(4):222-227. PubMed
-
Teng Xu#, Yanhai Gong#, Xiaolu Su#, Pengfei Zhu, Jing Dai, Jian Xu*, Bo Ma*. Phenome-genome profiling of single bacterial cell by Raman-activated Gravity-driven Encapsulation and Sequencing. Small 2020, 16(30):e2001172. PubMed
-
Xiaoquan Su*, Gongchao Jing, Zheng Sun, Lu Liu, Zhenjiang Xu, Daniel McDonald, Zengbin Wang, Honglei Wang, Antonio Gonzalez, Yufeng Zhang, Shi Huang, Gavin Huttley, Rob Knight*, Jian Xu*. Multiple-Disease detection and classification across cohorts via microbiome search. mSystems 2020, 5(2):e00150-20. PubMed
-
Zigang Xu, Xiaoyan Liu, Yueqing Niu, Chunping Shen, Kate Heminger, Laurie Moulton, Amy Yu, Tina Allen, Lesheng Zhang, Feng Yue, Jiquan Liu, Ying Xu, Helen Zhao, Lijuan Li, Tom Cambron, Jian Xu, Ed Smith, Karl Wei*. Skin benefits of moisturising body wash formulas for children with atopic dermatitis: A randomised controlled clinical study in China. Australasian Journal of Dermatology 2020, 61(1):e54-e59. PubMed
-
Zheng Sun#, Shi Huang#, Pengfei Zhu, Feng Yue, Helen Zhao, Ming Yang, Yueqing Niu, Gongchao Jing, Xiaoquan Su, Huiying Li, Chris Callewaert, Rob Knight, Jiquan Liu, Ed Smith, Karl Wei, Jian Xu*. A microbiome-based index for assessing skin health and treatment effects for atopic dermatitis in children. mSystems 2019, 4(4):e00293-19. PubMed
-
Yuehui He#, Xixian Wang#, Bo Ma*, Jian Xu*. Ramanome technology platform for label-free screening and sorting of microbial cell factories at single-cell resolution. Biotechnology Advances 2019, 37:107388. PubMed
-
Xiaoquan Su*, Gongchao Jing, Daniel McDonald, Honglei Wang, Zengbin Wang, Antonio Gonzalez, Zheng Sun, Shi Huang, Jose Navas, Rob Knight*, Jian Xu*. Identifying and predicting novelty in microbiome studies. mBio 2018, 9(6):e02099-18. PubMed
-
Jian Xu*, Bo Ma, Xiaoquan Su, Shi Huang, Xin Xu, Xuedong Zhou, Wei Huang, Rob Knight*. Emerging trends for microbiome analysis: from single-cell functional imaging to microbiome big data. Engineering 2017, 3(1):66-70. Link
-
黄适, 滕飞, 杨芳, 朱鹏飞, 苏晓泉, 马波, 徐健*. 基于微生物组的口腔“亚健康状态”检测. 生命科学[J]. 2017, 29(7): 660-668. Link
-
Shi Huang#, Zhen Li#, Tao He, Cunpei Bo, Jinlan Chang, Lin Li, Yanyan He, Jiquan Liu, Duane Charbonneau, Rui Li*, Jian Xu*. Microbiota-based signature of gingivitis treatments: A randomized study. Scientific Reports 2016, 6:24705. PubMed
-
Fei Teng#, Tao He#, Shi Huang, Cun-Pei Bo, Zhen Li, Jin-Lan Chang, Ji-Quan Liu, Duane Charbonneau, Jian Xu, Rui Li*, Jun-Qi Ling*. Cetylpyridinium chloride mouth rinses alleviate experimental gingivitis by inhibiting dental plaque maturation. International Journal of Oral Science 2016, 8(3):182-190. PubMed
-
Fei Teng#, Fang Yang#, Shi Huang#, Cunpei Bo, Zhengjiang Zech Xu, Amnon Amir, Rob Knight, Junqi Ling*, Xu Jian*. Prediction of early childhood caries via spatial-temporal variation of oral microbiota. Cell Host & Microbe 2015, 18(3):296-306. PubMed
-
Shi Huang#, Rui Li#, Xiaowei Zeng, Tao He, Helen Zhao, Alice Chang, Cunpei Bo, Jie Chen, Fang Yang, Rob Knight, Jiquan Liu, Catherine Davis, Jian Xu*. Predictive modeling of gingivitis severity and susceptibility via oral microbiota. The ISME Journal 2014, 8(9):1768-1780. PubMed
-
Shi Huang#, Fang Yang#, Xiaowei Zeng, Jie Chen, Rui Li*, Ting Wen, Chun Li, Wei Wei, Jiquan Liu, Lan Chen, Catherine Davis, Jian Xu*. Preliminary characterization of the oral microbiota of Chinese adults with and without gingivitis. BMC Oral Health 2011, 11:33. PubMed
更多详情,请访问:http://www.single-cell.cn/info/1034/2124.htm
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。
|