|
|
|
|
|
上海有机所在不对称1,5-共轭加成反应研究中获进展 |
|
|
中国科学院上海有机化学研究所天然产物有机合成化学重点实验室何智涛课题组致力于不对称催化合成和生命小分子修饰等领域。近期,该课题组在《德国应用化学》上,在线发表了题为Umpolung Asymmetric 1,5-Conjugate Addition via Palladium Hydride Catalysis的研究论文。该工作利用钯氢催化策略,发展了一类新颖的极性反转的1,5-共轭加成反应,突破了过往所认为的只有底物电性匹配的1,6-加成才具有可行性的观念。
近年来,过渡金属催化的不对称η3-取代已成为构建手性片段的重要手段。前期,何智涛课题组围绕该领域相继发展了一系列不对称催化转化策略(J. Am. Chem. Soc. 2021, 143, 7285.;Nat. Commun. 2021, 12, 5626.;Nat. Synth. 2022, doi.org/10.1038/s44160-022-00176-4)。以此为基础,该课题组进一步拓展相关的策略应用范围。不同于经典的亲核性1,6-共轭加成反应,不饱和羰基化合物的亲核1,5-共轭加成反应由于底物电性上的不匹配,需要克服巨大的反应能垒,因而被认为是不可行的过程。同时,反应面临着多种竞争性的副反应,包括1,2-加成、1,4-加成和1,6-加成等。因此,如何实现区域选择性和立体选择性的1,5-加成反应是亟待解决的难题。何智涛课题组设想了一种钯氢催化的极性反转的策略,即通过钯氢催化剂和烯烃发生迁移插入,形成π-烯丙基钯中间体,并串联亲核试剂的烯丙基取代,从而有望实现该1,5-加成历程。
研究利用钯氢催化的1,5-共轭加成并结合分子间的[3+2]环化,可高效地构建出一系列光学活性的多取代四氢呋喃环骨架。同时,通过发展钯/有机催化协同控制模式,研究实现了1,5-共轭加成/分子内[3+2]环化的串联历程,一步构建了手性的二氢呋喃环片段。课题组进一步利用非共轭的不饱和酯为底物,实现了迁移1,5-共轭加成反应,进一步证实了该策略的可行性和普适性。
研究工作得到国家自然科学基金、上海市科学技术委员会、上海有机所、中科院天然产物有机合成化学重点实验室的支持。
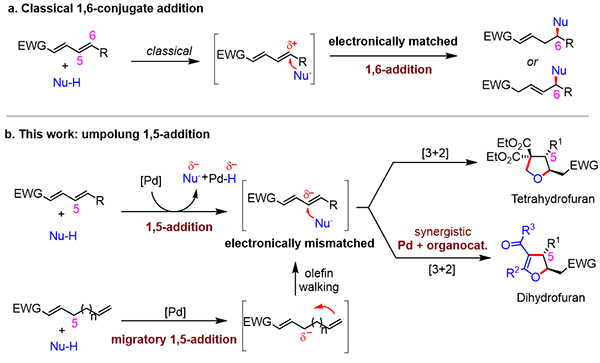
图1.极性反转的1,5-加成反应
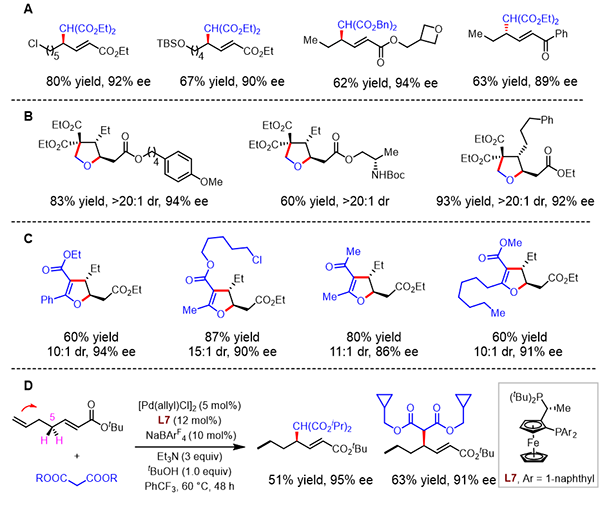
图2.底物范围
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。