中国科学院广州生物医药与健康研究院研究员刘兴国团队与广州医科大学副教授项鸽团队研究发现调控线粒体趋核分布的关键因素,并揭示了线粒体趋核分布通过激活Wnt/β-catenin信号通路,而调控间充质-上皮转化(MET)的新模式。相关成果4月17日发表于《干细胞报告》(Stem Cell Reports)。
“该研究的发现进一步扩展了线粒体重塑,特别是线粒体的亚细胞定位变化在多能干细胞获得进程中的重要作用。”论文共同通讯作者刘兴国对《中国科学报》表示。
多能干细胞的发现是现代医学的大事件,对于基础和临床研究都具有划时代的意义。从上个世纪多能干细胞诞生以来,人们已经通过观察认识到,与体细胞相比,早期发育的卵子和各种多能干细胞,都有一个共同的特征:细胞核周围有明显的线粒体分布。然而,核周分布的线粒体对于干细胞的命运决定有何作用,这一世纪谜题一直没有答案。
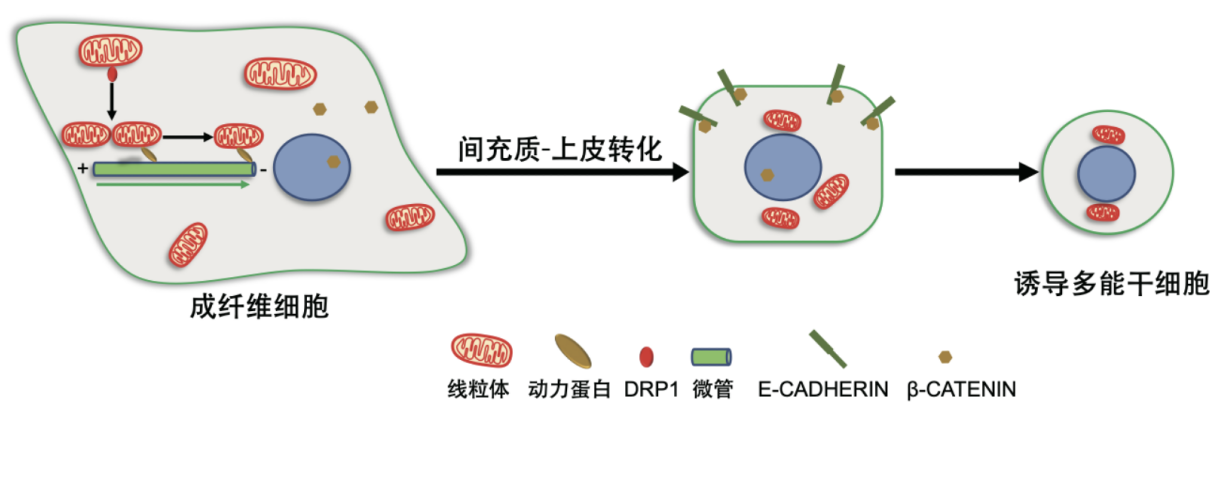
线粒体趋核运输通过调控MET影响干细胞多能性获得。研究团队供图
?
研究团队在国家重点研发计划、国家自然科学基金等项目的资助下,首先发现在三因子(Oct4、Sox2、Klf4)诱导的体细胞重编程早期第三天开始,线粒体呈现趋向细胞核周围运输,并一直维持趋核分布。同时发现三个转录因子中,只有Oct4可以介导线粒体趋核。Oct4是多能干细胞的标志,它在多能干细胞中的高表达可以激活干细胞多能性维持所必须的编码蛋白和非编码RNA。随着干细胞的分化,Oct4的表达水平会迅速下降。
研究团队的发现表明,Oct4是介导体细胞重编程中线粒体趋核运输的关键因子,暗示ESCs(胚胎干细胞)中的线粒体趋核分布也离不开Oct4的调控作用。转录组测序结果也表明,SKO(Yamanaka因子Sox2/Klf4/Oct4三因子)和Oct4单因子都可以激活线粒体趋核运输相关复合物的活性,从而激活了线粒体的趋核运输。基于此,团队通过RNA干扰抑制了线粒体趋核运输关键亚基Dynein的活性,发现体细胞重编程被抑制了。
此外,Drp1介导的线粒体分裂也会影响线粒体的趋核分布。初步研究表明,线粒体趋核分布调控了MET标志蛋白E-cadherin的表达,从而调控了MET的顺利进行。进一步研究表明,线粒体趋核主要是通过激活了Wnt/β-catenin信号,β-catenin不是通过进入细胞核发挥作用,而是通过直接调控了MET的关键蛋白E-cadherin的稳定性而参与了MET的进行,从而最终调控多能性获得。
该研究揭示了在体细胞重编程进程早期,线粒体会呈现趋核分布,这对于体细胞重编程的顺利进行不可或缺。线粒体的趋核分布主要是通过激活了Wnt/β-catenin信号通路而上调了β-catenin的蛋白表达量,上调的β-catenin可以通过提高MET标志蛋白E-cadherin的稳定性进而参与了MET的调控。
MET和上皮-间充质转化在胚胎发育、组织再生和癌症转移发挥作用,所以线粒体趋核调控MET具有广泛的发育和病理意义。该研究发现了线粒体趋核调控MET的新机制,丰富了线粒体重塑调控多能性获得的新功能,有望为线粒体重塑调控细胞命运的理论创新提供参考。(来源:中国科学报 朱汉斌)
相关论文信息:https://doi.org/10.1016/j.stemcr.2025.102474