|
|
|
|
|
PanDrugs:根据个体基因组特征优化肿瘤治疗的新方法 |
|
|
论文题目:PanDrugs: a novel method to prioritize anticancer drug treatments according to individual genomic data
期刊:Genome Medicine
作者:Elena Piñeiro-Yáñez et al.
发表时间:2018/5/31
数字识别码:10.1186/s13073-018-0546-1
原文链接:https://genomemedicine.biomedcentral.com/articles/10.1186/s13073-018-0546-1?utm_source=Other_website&utm_medium=Website_links&utm_content=DaiDen-BMC-Genome_Medicine-Medical_Genetics-China&utm_campaign=BMCF_USG_BSCN_DD_GM_PanDrugs
近日在Genome Medicine上发表的一篇文章展示了一种新的开放性工具,可用于评估癌症患者的基因组谱,以明确是否有治疗干预的机会。 文章作者希望这种新方法将有助于在医院环境中推广预防医学。

肾脏肿瘤中肿瘤细胞(粉色)的彩色电镜照片
© DAVID MCCARTHY / SCIENCE PHOTO LIBRARY
根据癌症基因组数据中确定最合适的治疗方法是癌症个体化治疗的主要挑战之一。 医生和研究人员面对的是长长的肿瘤特异性基因组变异清单,其中大多数突变在临床上是“无作用的”——即其生物学作用未知或与肿瘤生物学无关。 另外,即便某些基因突变真的对于肿瘤发生、生长和存活是必不可少的,但目前的治疗方法可能也无法对该突变进行处理。
因此我们需要新的生物信息学方法来解读基因组突变,评估其临床相关性和相关药物的可行性,并根据询证依据提供最优的个体化肿瘤治疗方案以辅助临床决策。
PanDrugs简介
我们开发了基于数据的PanDrugs,该工具可用于评估癌症患者的基因组谱,根据生物学和临床相关性明确是否有治疗干预的机会,根据其生物学和临床相关性以及治疗干预的机会。 该方法会扫描自带数据库(PanDrugsdb),并根据患者的基因组信息列表返回最佳候选药物和可靶向治疗的基因。
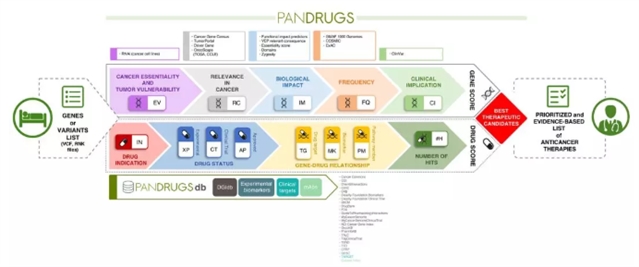
该图片由原文作者提供
PanDrugs的药物和靶基因筛选各有一个评分,这两个评分整合了各种临床,生物学和药理学数据,以提供个性化的抗肿瘤治疗。 基因评分(GScore)主要依据支持基因临床意义的证据水平及其与肿瘤的生物血相关性;药物评分(DScore)则主要评估患者对药物反应和治疗的合适性。
与目前的工具相比,PanDrugs的另一个独特功能是扩大了最佳治疗搜索范围。 换句话说,PanDrugs除了返回直接治疗靶点(例如,有助于疾病表型且有针对性药物的基因),还会返回生物学标志物(例如可预测患者对药物反应的基因,但基因本身的产物并非药物靶点)。
此外,PanDrugs还中还包括一个系统生物学知识层,可自动检查生物信号通路从而将癌症候选疗法从单个基因列表扩展到整个通路。 这种新颖的“通路成员”策略扩展了癌症患者的治疗选择,并为个性化医疗开辟了新的途径。 在这篇文章中,我们应用这一策略来展示无可靶向治疗基因的前列腺癌,乳腺癌和结直肠癌患者如何从目前的临床治疗中受益。
PanDrugs数据库本身也是一个极有价值且可以公开访问的资源。 这个数据库是目前最大的药物—靶点组合公共储存库,包括已非常成熟的靶向治疗药物和目前处于临床前期的药物。 当前版本的PanDrugsdb整合了24个主要数据库,纳入了超过56,000个药物—靶点组合。 PanDrugs和PanDrugsdb都对公众开放,可在 http://www.pandrugs.org上获得。
转化应用
PanDrugs可对肿瘤患者的基因分子谱进行分析以辅助临床决策制定,在医疗机构中还能和其他基因分析软件一并使用。PanDrugs在我们机构已经广泛用于分析患者测序数据并提出治疗方案 - 这是 PanDrugs应用于临床的一个例子,在我们发表在Genome Medicine上的文章中有详细描述。
此外,PanDrugs还被系统地应用于TCGA项目的7,069名患者,涉及20多种不同的肿瘤。 完整的结果可以在PanDrugs网站上查看。
PanDrugs的未来
个体化肿瘤治疗仍处在发展初期。 想要推广个体化肿瘤治疗,医院需要快速、可重复、操作简单且低成本的计算机方法检测基因突变,解释这些突变的生物学和临床效应,根据患者的基因组情况选择治疗方案, 同时通过病历资料进行临床评估。
PanDrugs是第一个能够系统推断新的靶向治疗的工具,其依据是多种基因标志物、分子信号通路和药理学依据构成的科学体系。
尽管PanDrugs可有效辅助计算机临床决策,但因为缺乏大量纵向精确医学研究及相关病史资料这种方法的使用仍受到限制。此类研究有助于验证药物建议并进一步调整计算机算法,纳入更多的考量因素,例如给药方式、联合治疗、药物变化、药物副作用等。 我们仍需开发更有效的抗肿瘤药物和预测肿瘤耐药性的方法来进一步改善肿瘤治疗。
如今,在医院里推广精准医学仍面临重大挑战, 但PanDrugs无疑为预测治疗结局的生物学指标应用于临床提供了桥梁。
文章作者还想感谢PanDrugs用户提供宝贵的反馈意见是他们能进一步完善这一工具。 他们还鼓励癌症研究人员和医生试用PanDrugs,并给予反馈意见使PanDrugs更接近日常临床实践。
摘要:
Background
Large-sequencing cancer genome projects have shown that tumors have thousands of molecular alterations and their frequency is highly heterogeneous. In such scenarios, physicians and oncologists routinely face lists of cancer genomic alterations where only a minority of them are relevant biomarkers to drive clinical decision-making. For this reason, the medical community agrees on the urgent need of methodologies to establish the relevance of tumor alterations, assisting in genomic profile interpretation, and, more importantly, to prioritize those that could be clinically actionable for cancer therapy.
Results
We present PanDrugs, a new computational methodology to guide the selection of personalized treatments in cancer patients using the variant lists provided by genome-wide sequencing analyses. PanDrugs offers the largest database of drug-target associations available from well-known targeted therapies to preclinical drugs. Scoring data-driven gene cancer relevance and drug feasibility PanDrugs interprets genomic alterations and provides a prioritized evidence-based list of anticancer therapies. Our tool represents the first drug prescription strategy applying a rational based on pathway context, multi-gene markers impact and information provided by functional experiments. Our approach has been systematically applied to TCGA patients and successfully validated in a cancer case study with a xenograft mouse model demonstrating its utility.
Conclusions
PanDrugs is a feasible method to identify potentially druggable molecular alterations and prioritize drugs to facilitate the interpretation of genomic landscape and clinical decision-making in cancer patients. Our approach expands the search of druggable genomic alterations from the concept of cancer driver genes to the druggable pathway context extending anticancer therapeutic options beyond already known cancer genes. The methodology is public and easily integratable with custom pipelines through its programmatic API or its docker image. The PanDrugs webtool is freely accessible at http://www.pandrugs.org.
阅读论文原文,请访问https://genomemedicine.biomedcentral.com/articles/10.1186/s13073-018-0546-1?utm_source=Other_website&utm_medium=Website_links&utm_content=DaiDen-BMC-Genome_Medicine-Medical_Genetics-China&utm_campaign=BMCF_USG_BSCN_DD_GM_PanDrugs
期刊介绍:Genome Medicine publishes research and reviews that describe important advances in the application of genetics, genomics and multi-omics to understand, diagnose and treat disease. Areas covered include, but are not limited to: precision medicine, novel methods and software, cancer genomics, disease genomics and epigenomics, immunogenomics, infectious disease, microbiome and systems medicine.
2016 Journal Metrics
Citation Impact
8.898 - 2-year Impact Factor
8.265 - 5-year Impact Factor
1.426 - Source Normalized Impact per Paper (SNIP)
(来源:科学网)
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。