|
|
|
|
|
科学家开发新型金属纳米颗粒疗法调节肠道微环境治疗炎症性肠病 |
|
|
3月27日,国家纳米科学中心聂广军、赵瑞芳联合首都医科大学陈汉清团队,在Matter期刊上发表题为"Oral nanoparticle therapy for inflammatory bowel disease by Paneth cell regulation and mucus layer remodeling"的研究成果。
该研究设计了一种新型钨包锌的金属纳米颗粒(W@ZnNPs),通过重塑肠道屏障功能、调控微生物群落和调节免疫反应三重作用机制,为炎症性肠病(IBD)治疗提供了可行的治疗策略。
论文通讯作者为聂广军、赵瑞芳、陈汉清,第一作者为覃裕婷、王泽铭。
IBD作为全球性健康挑战,包含克罗恩病和溃疡性结肠炎两种主要类型,其发病率在新兴工业化国家持续攀升。该疾病以肠道慢性炎症为特征,伴随屏障损伤、菌群失调和免疫紊乱等病理改变,现有疗法主要依赖免疫抑制,但无法有效解决疾病根源问题。据统计,克罗恩病患者缺锌比例高达51%,锌代谢障碍与疾病进展形成恶性循环,这使得开发针对病理机制的新型疗法迫在眉睫。
研究团队提出的创新疗法聚焦于肠道稳态的三大核心要素:潘氏细胞、杯状细胞和肠道菌群。潘氏细胞作为肠道免疫哨兵,通过分泌抗菌肽维持微生态平衡;杯状细胞构建的粘液屏障则是抵御病原入侵的首道防线。在IBD病程中,这两种细胞的数量和功能均出现受损,导致屏障破坏和菌群失调。基于此,研究团队设计了一种具有双重功能的金属纳米颗粒W@ZnNPs,巧妙整合锌对上皮细胞的关键作用与钨的微生物调控能力。
W@ZnNPs在胃酸环境中具有高稳定性,实现炎症肠段的靶向释放;其次利用表面特性增强黏液层粘附,促进与肠道菌群的局部相互作用;最后通过控制释放机制实现锌、钨的时空协同递送。动物实验显示,W@ZnNPs可显著增加潘氏细胞数量,恢复其溶菌酶等抗菌肽分泌功能;同时促进杯状细胞增殖,重建结构完整的粘液屏障。在微生物调控方面,钨组分展现出精准的抗菌谱调节能力。通过选择性抑制肠杆菌科等兼性厌氧菌的过度增殖,成功将结肠炎小鼠的菌群多样性指数恢复至健康水平。这种选择性调控避免了传统抗生素的广谱杀伤效应,为维持菌群稳态提供了新的思路。
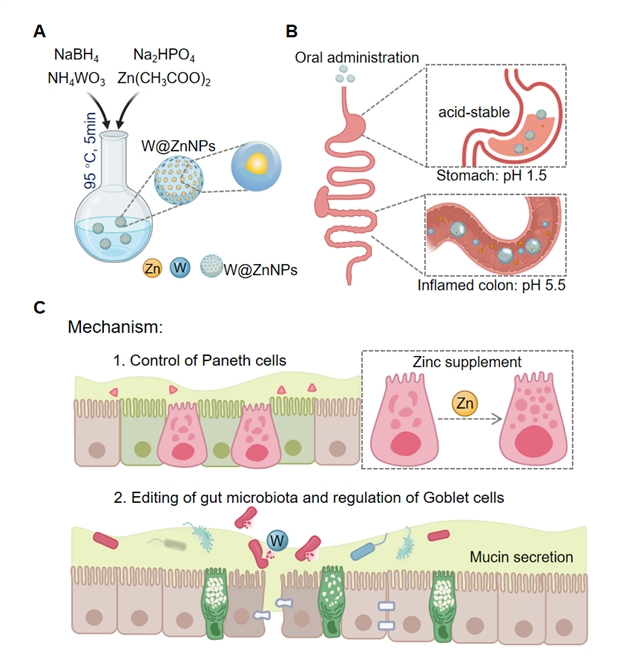
图1:W@ZnNPs预防和治疗炎症性肠病的机制示意图。
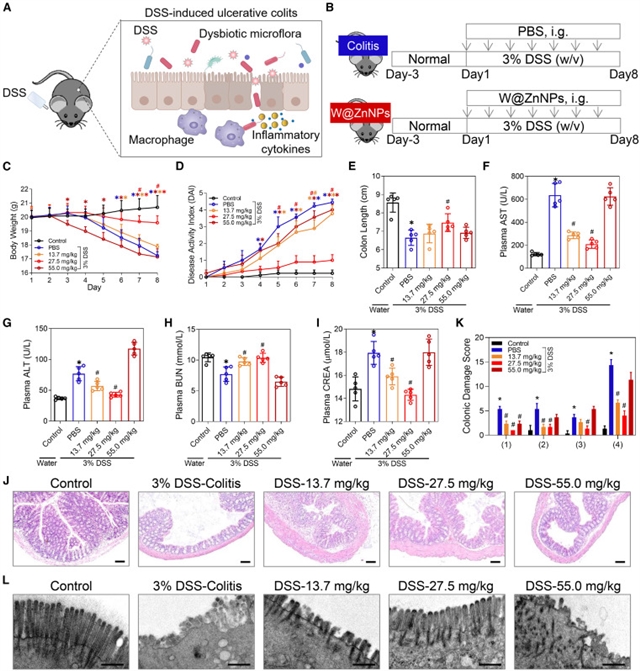
图2:DSS诱导的小鼠急性结肠炎的治疗效果。
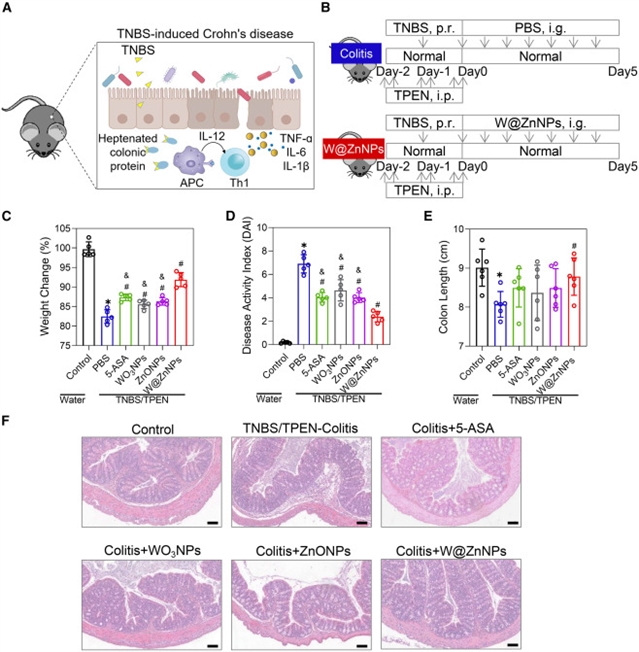
图3:TNBS/TPEN诱导的小鼠结肠炎疗效比较。
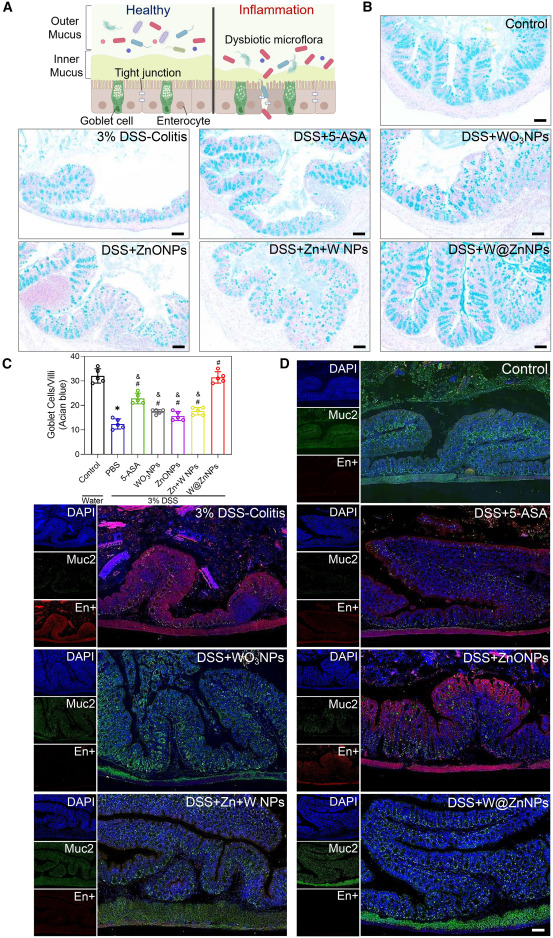
图4:恢复杯状细胞功能抑制肠菌易位。
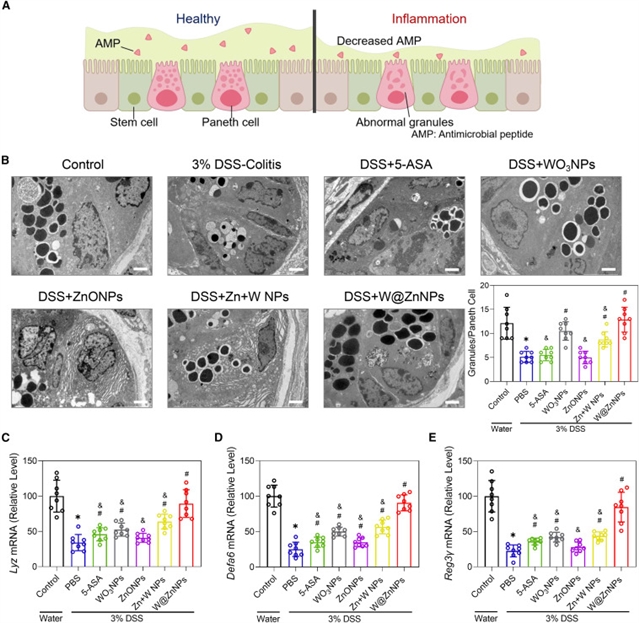
图5:增强潘氏细胞抗菌肽分泌能力。
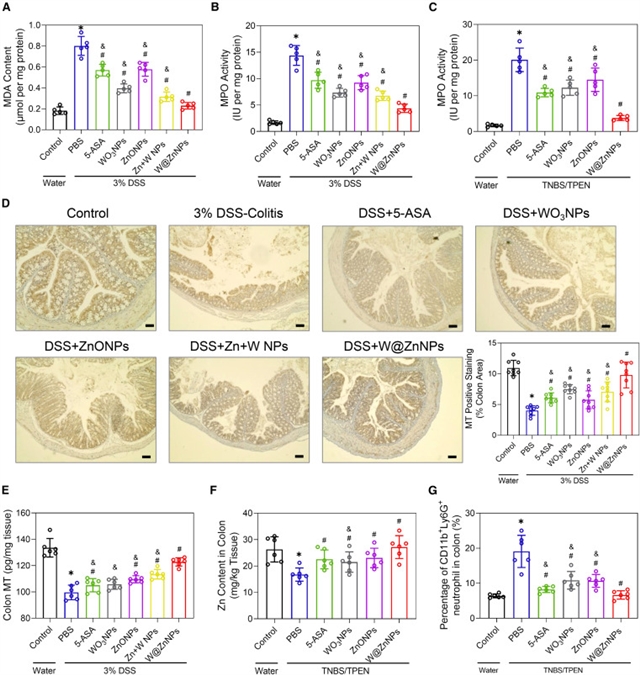
图6:调节锌稳态缓解氧化应激。
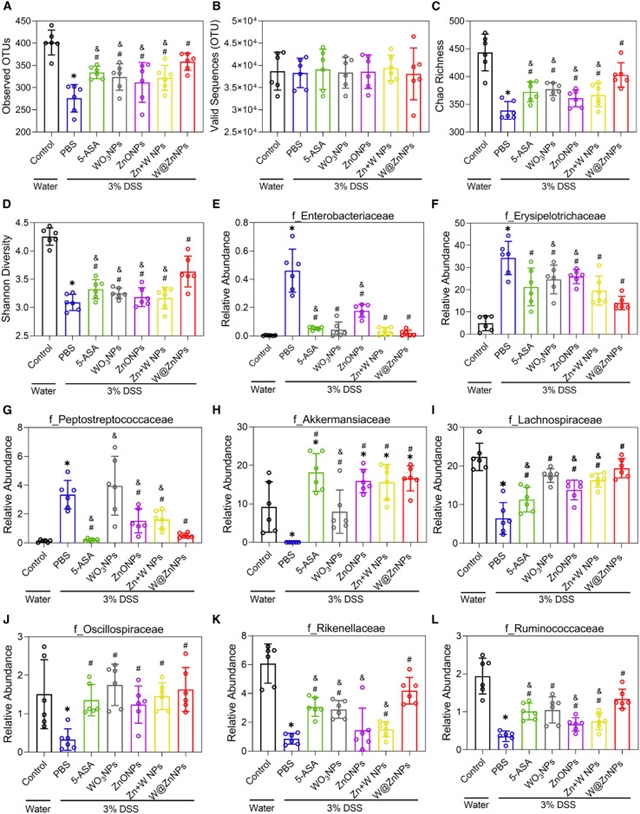
图7:重塑肠道微生态改善炎症。
该研究通过构建金属纳米颗粒的双重递送系统,突破单一元素治疗的局限性,建立“细胞-菌群-免疫”多重调控体系,实现IBD病理机制的根源性干预,具有临床转化潜力。(来源:科学网)
相关论文信息:https://doi.org/10.1016/j.matt.2025.102084